名校
1 . 分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液均为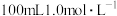 的稀硫酸(假设反应过程中溶液体积不变),乙中
的稀硫酸(假设反应过程中溶液体积不变),乙中 为电流表。
为电流表。
(1)反应过程中能量转化的主要形式:甲为___________ ;乙为___________ 。
(2)以下叙述中,正确的是___________(填字母)。
(3)如图所示为两装置中产生氢气体积随时间的变化图像,其中表示甲的曲线是___________ (填“ ”或“
”或“ ”),若经过5min甲中产生气体体积为224mL(标准状况),下列能够正确表示该反应速率的是
”),若经过5min甲中产生气体体积为224mL(标准状况),下列能够正确表示该反应速率的是___________ (填字母),若要加快甲中反应的速率,可以采取的方法是___________ (任写两种)。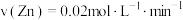 B.
B.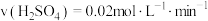
C. D.
D.
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,则铜电极为___________ (填“正极”或“负极”,下同), 离子移向
离子移向___________ , 电极的电极反应式为
电极的电极反应式为___________ ,当外电路中转移 电子时,消耗负极材料的质量为
电子时,消耗负极材料的质量为___________ g(保留三位小数)。
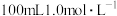 的稀硫酸(假设反应过程中溶液体积不变),乙中
的稀硫酸(假设反应过程中溶液体积不变),乙中 为电流表。
为电流表。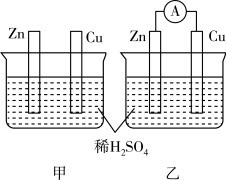
(1)反应过程中能量转化的主要形式:甲为
(2)以下叙述中,正确的是___________(填字母)。
| A.甲中锌片是负极,乙中铜片是正极 | B.两烧杯中铜片表面均有气泡产生 |
| C.两烧杯中溶液pH均增大 | D.两烧杯中发生的反应相同 |
(3)如图所示为两装置中产生氢气体积随时间的变化图像,其中表示甲的曲线是
 ”或“
”或“ ”),若经过5min甲中产生气体体积为224mL(标准状况),下列能够正确表示该反应速率的是
”),若经过5min甲中产生气体体积为224mL(标准状况),下列能够正确表示该反应速率的是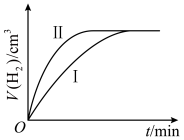
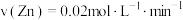 B.
B.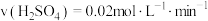
C.
 D.
D.
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,则铜电极为
 离子移向
离子移向 电极的电极反应式为
电极的电极反应式为 电子时,消耗负极材料的质量为
电子时,消耗负极材料的质量为
您最近一年使用:0次
名校
2 . 电池的充放电效率和续航时间限制了新能源汽车的使用,部分科学家开始将目光投向纸电池。一种纸电池由植入了电极和电解液的纤维素纸构成,其中纤维素纸起到隔离物的作用,电极分别是加入纤维素中的碳纳米管和覆盖在纤维素制成的薄膜上的金属锂,而电解液为六氟磷酸锂溶液。下列说法错误的是
| A.加入纤维素中的碳纳米管为电池的正极 | B.每有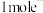 转移,负极质量减轻7g 转移,负极质量减轻7g |
| C.电池放电时六氟磷酸根向锂电极移动 | D.该电池的能量转化效率可以达到100% |
您最近一年使用:0次
2024-06-18更新
|
31次组卷
|
2卷引用:山西省部分学校2023-2024学年高一下学期5月质量检测化学试题
解题方法
3 .  、
、 和
和 是氮的重要氧化物。
是氮的重要氧化物。 时,在
时,在 的恒容绝热密闭容器(不发生热交换,体系温度随反应吸热或放热发生变化)中发生反应:
的恒容绝热密闭容器(不发生热交换,体系温度随反应吸热或放热发生变化)中发生反应: 反应过程中各气体浓度随时间变化的情况如图所示。
反应过程中各气体浓度随时间变化的情况如图所示。
(1)甲曲线代表___________ (填 或
或 ),当
),当 的浓度为
的浓度为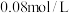 时,反应时间为
时,反应时间为 ,则
,则 时,用
时,用 气体的浓度变化量表达该反应的平均速率为
气体的浓度变化量表达该反应的平均速率为________  。
。
(2)A、B两点对应时刻,反应速率大小: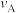
________ 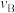 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)不能说明该反应达到平衡状态的是___________(填序号)。
(4)平衡转化率( )是指某一可逆化学反应达到化学平衡状态时,转化为目的产物的某种原料的量占该种原料起始量的百分数,如
)是指某一可逆化学反应达到化学平衡状态时,转化为目的产物的某种原料的量占该种原料起始量的百分数,如 的可逆反应,
的可逆反应, (A的初始浓度-A的平衡浓度)/A的初始浓度
(A的初始浓度-A的平衡浓度)/A的初始浓度 。求该反应的平衡转化率
。求该反应的平衡转化率
___________ 。
(5)在一定条件下,用 与
与 反应生成
反应生成 和
和 可消除
可消除 污染物。在恒温恒压下模拟该反应:
污染物。在恒温恒压下模拟该反应: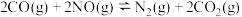 ,为提高此反应的速率,下列措施可行的是________(填字母)。
,为提高此反应的速率,下列措施可行的是________(填字母)。
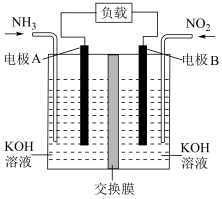
(6)某学习小组设计如下装置,有效降低含氮化合物的排放,同时充分利用化学能。___________ 。
 、
、 和
和 是氮的重要氧化物。
是氮的重要氧化物。 时,在
时,在 的恒容绝热密闭容器(不发生热交换,体系温度随反应吸热或放热发生变化)中发生反应:
的恒容绝热密闭容器(不发生热交换,体系温度随反应吸热或放热发生变化)中发生反应: 反应过程中各气体浓度随时间变化的情况如图所示。
反应过程中各气体浓度随时间变化的情况如图所示。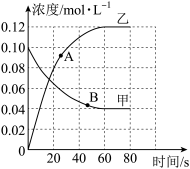
(1)甲曲线代表
 或
或 ),当
),当 的浓度为
的浓度为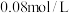 时,反应时间为
时,反应时间为 ,则
,则 时,用
时,用 气体的浓度变化量表达该反应的平均速率为
气体的浓度变化量表达该反应的平均速率为 。
。(2)A、B两点对应时刻,反应速率大小:
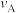
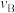 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)不能说明该反应达到平衡状态的是___________(填序号)。
| A.混合气体的温度不再改变 | B.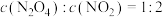 |
| C.容器内气体颜色不再改变 | D.容器内气体的密度不再改变 |
(4)平衡转化率(
 )是指某一可逆化学反应达到化学平衡状态时,转化为目的产物的某种原料的量占该种原料起始量的百分数,如
)是指某一可逆化学反应达到化学平衡状态时,转化为目的产物的某种原料的量占该种原料起始量的百分数,如 的可逆反应,
的可逆反应, (A的初始浓度-A的平衡浓度)/A的初始浓度
(A的初始浓度-A的平衡浓度)/A的初始浓度 。求该反应的平衡转化率
。求该反应的平衡转化率
(5)在一定条件下,用
 与
与 反应生成
反应生成 和
和 可消除
可消除 污染物。在恒温恒压下模拟该反应:
污染物。在恒温恒压下模拟该反应: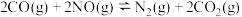 ,为提高此反应的速率,下列措施可行的是________(填字母)。
,为提高此反应的速率,下列措施可行的是________(填字母)。| A.充入氦气以增大压强 | B.降低温度 |
| C.使用适合催化剂 | D.移出 |
(6)某学习小组设计如下装置,有效降低含氮化合物的排放,同时充分利用化学能。
您最近一年使用:0次
名校
4 . 如图是课外活动小组设计用化学电源使LED灯发光的装置。下列说法正确的是
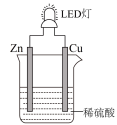
| A.溶液中阳离子移向锌片 |
| B.装置中存在“化学能→电能→光能”的转换 |
| C.电子流动方向为“Zn→稀硫酸→Cu” |
| D.如果将铜片换成碳棒,电路中的电流方向改变 |
您最近一年使用:0次
5 . 某同学依据锌与稀硫酸的反应设计成如图Ⅰ的装置;该反应的能量变化如图Ⅱ。下列说法正确的是

| A.运用该反应设计电池,负极材料可用铜或石墨 |
| B.化学反应中能量变化的主要原因是化学键的断裂 |
| C.图Ⅰ装置可以将化学能转变为电能 |
| D.该反应为放热反应 |
您最近一年使用:0次
解题方法
6 . 已知:氧化还原反应可看成由两个半反应组成,每个半反应具有一定的电极电势(用“E”表示),E越大则该电对中氧化型物质的氧化性越强,E越低则该电对中还原型物质的还原性越强。下表为部分电极的电极电势。根据表格数据分析,下列说法中错误的是
下列说法错误的是
| 氧化还原电对(氧化型/还原型) | 电极电势(E/V) | 氧化还原电对(氧化型/还原型) | 电极电势(E/V) |
 | 0.77 | 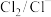 | 1.36 |
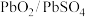 (或 (或 ) ) | 1.69 | 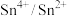 | 0.151 |
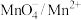 | 1.51 |  | 0.54 |
| A.向含0.2molFeCl2的溶液中加0.1molPbO2,滴加KSCN溶液,可观察到溶液变红 |
| B.往淀粉-KI溶液中滴加SnCl4溶液,溶液不变蓝 |
C.还原性: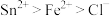 |
| D.酸化高锰酸钾溶液时,可使用盐酸 |
您最近一年使用:0次
7 . 一种利用金属磷化物作为催化剂,将CH3OH转化成甲酸钠的电化学示意图如下,阴极生成 和一种气体。下列说法错误的是
和一种气体。下列说法错误的是
 和一种气体。下列说法错误的是
和一种气体。下列说法错误的是
| A.b为电源正极 |
| B.Na+由右侧室向左侧室移动 |
C.阴极的电极反应式为2CO2+2H2O+2e-=2HCO +H2↑ +H2↑ |
D.理论上,当电路中转移 时,阴极室质量增加134g 时,阴极室质量增加134g |
您最近一年使用:0次
名校
8 . 回答下列问题
(1)把煤作为燃料可通过下列两种途径:
途径I:C(s)+O2(g)=CO2(g) ΔH1<0 ①
途径II:先制成水煤气:C(s)+H2O(g)=CO(g)+H2(g) ΔH2>0 ②
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g) ΔH3<0 ③
2H2(g)+O2(g)=2H2O(g) ΔH4<0 ④
则途径I放出的热量_______ (填“大于”“等于”或“小于”)途径II放出的热量;ΔH1、ΔH2、ΔH3、ΔH4的数学关系式是_______ 。
(2)火箭发射时可用肼(N2H4)为燃料。已知:N2(g)+2O2(g)=2NO2(g) H=+67.7kJ•mol-1;
H=+67.7kJ•mol-1;
N2H4(g)+O2(g)=N2(g)+2H2O(g) H=-534kJ•mol-1;
H=-534kJ•mol-1;
H2O(l)=H2O(g) H=+44.0kJ•mol-1;
H=+44.0kJ•mol-1;
请写出N2H4燃烧热的热化学方程式:_______ 。
(3)如表所示是部分化学键的键能参数:
一定条件下1mol气态白磷完全燃烧生成气态产物的结构如图所示,放出热量为为dkJ,表中x=_______ kJ/mol(用含a、b、c、d的代表数式表示)。 设计如图所示电池(离子交换膜对溶液里的离子具有选择透过能力)。
设计如图所示电池(离子交换膜对溶液里的离子具有选择透过能力)。_______ (阴或阳)离子交换膜,电流_______ (填“可以”或“不可以”)通过交换膜。
②电池工作一段时间后,左侧电极室溶液的碱性_______ (填“增强”、“减弱”或“几乎无变化”)。(不考虑消耗或生成的水对浓度的影响)
③电极B反应式为_______ 。
④同温同压时,左右两侧电极室中产生的气体体积比为_______ ,转移8mol电子,右侧溶液质量_______ (增加或减少)_______ g。
(1)把煤作为燃料可通过下列两种途径:
途径I:C(s)+O2(g)=CO2(g) ΔH1<0 ①
途径II:先制成水煤气:C(s)+H2O(g)=CO(g)+H2(g) ΔH2>0 ②
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g) ΔH3<0 ③
2H2(g)+O2(g)=2H2O(g) ΔH4<0 ④
则途径I放出的热量
(2)火箭发射时可用肼(N2H4)为燃料。已知:N2(g)+2O2(g)=2NO2(g)
 H=+67.7kJ•mol-1;
H=+67.7kJ•mol-1;N2H4(g)+O2(g)=N2(g)+2H2O(g)
 H=-534kJ•mol-1;
H=-534kJ•mol-1;H2O(l)=H2O(g)
 H=+44.0kJ•mol-1;
H=+44.0kJ•mol-1;请写出N2H4燃烧热的热化学方程式:
(3)如表所示是部分化学键的键能参数:
| 化学键 | P-P | P-O | O=O | P=O |
| 键能/kJ/mol | a | b | c | x |

 设计如图所示电池(离子交换膜对溶液里的离子具有选择透过能力)。
设计如图所示电池(离子交换膜对溶液里的离子具有选择透过能力)。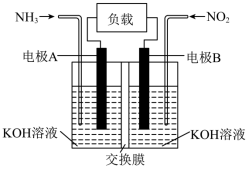
②电池工作一段时间后,左侧电极室溶液的碱性
③电极B反应式为
④同温同压时,左右两侧电极室中产生的气体体积比为
您最近一年使用:0次
名校
解题方法
9 . 锂海水电池常用在海上浮标等助航设备中,其原理如图所示。电池反应为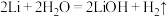 。电池工作时,下列说法错误的是
。电池工作时,下列说法错误的是
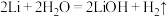 。电池工作时,下列说法错误的是
。电池工作时,下列说法错误的是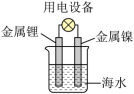
| A.如果将海水换成乙醇,该装置不可以构成原电池装置 |
| B.电子从锂电极经导线流向镍电极 |
| C.金属锂作负极,发生氧化反应 |
| D.理论上每转移2mol电子可以生成22.4LH2 |
您最近一年使用:0次
名校
解题方法
10 . 法国化学家PaulSabatier研究得出CO2在催化剂作用下能够转化为甲烷,以实现CO2的资源化利用。CO2甲烷化反应为CO2(g)+4H2(g)=CH4(g)+2H2O(g)。
请回答:
(1)某温度下,往容积为2L、装有催化剂的恒容密闭容器中充入n(CO2):n(H2)=1:5的混合气体,发生上述反应,n(CO2)与n(CH4)随时间的变化如图所示。图中表示CO2变化的曲线是___________ (用a、b表示)。___________ mol/(L·min),反应达到平衡状态时,c(H2O)=___________ mol/L。
②x、y两点用CO2表示的化学反应速率:v(x)正___________ v(y)逆(填“>”“<”或“=”)。
③下列说法正确的是___________ (填标号)。
A.交点处反应达到平衡
B.及时分离出H2O能加快反应速率
C.容器中混合气体的平均相对分子质量不再发生改变时,该反应达到平衡
D.若改变催化剂,则反应达到平衡状态所需的时间一定小于5min
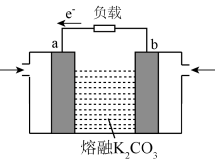
(3)新型高效甲烷空气燃料电池采用石墨烯作电极,分别往两电极通入甲烷和空气,工作原理如图所示。a电极通入的气体是___________ ;b电极的电极反应式为___________ 。
请回答:
(1)某温度下,往容积为2L、装有催化剂的恒容密闭容器中充入n(CO2):n(H2)=1:5的混合气体,发生上述反应,n(CO2)与n(CH4)随时间的变化如图所示。图中表示CO2变化的曲线是
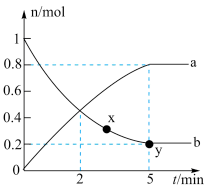
②x、y两点用CO2表示的化学反应速率:v(x)正
③下列说法正确的是
A.交点处反应达到平衡
B.及时分离出H2O能加快反应速率
C.容器中混合气体的平均相对分子质量不再发生改变时,该反应达到平衡
D.若改变催化剂,则反应达到平衡状态所需的时间一定小于5min
(3)新型高效甲烷空气燃料电池采用石墨烯作电极,分别往两电极通入甲烷和空气,工作原理如图所示。a电极通入的气体是
您最近一年使用:0次



