名校
1 . 下列装置或操作一定能达到实验目的的是
| A | B | C | D |
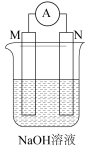 | 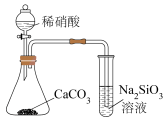 | 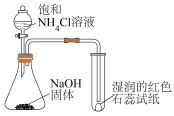 |  |
| 比较金属M和N的活动性 | 验证酸性: | 验证碱性:NaOH> | 验证氧化性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-12更新
|
196次组卷
|
2卷引用:湖北省2023届高三5月联考化学试题
2 . 下列实验装置能达到实验目的的是
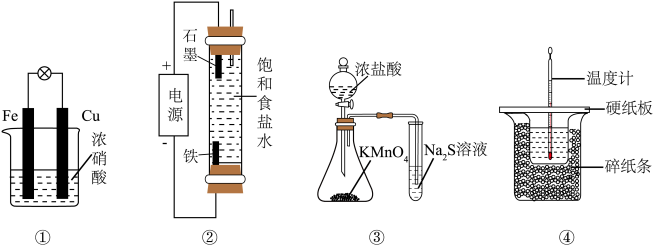
| A.装置①验证Fe和Cu的还原性强弱 | B.装置②制备少量NaClO |
C.装置③比较 、 、 和S的氧化性 和S的氧化性 | D.装置④测定中和反应的反应热 |
您最近一年使用:0次
名校
3 . 用下列装置进行相应实验,能达到实验目的的是
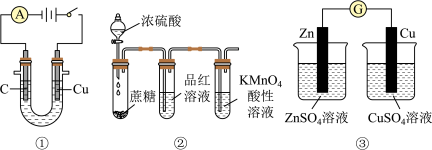



| A.图①所示装置可电解食盐水制氯气和氢气 |
B.图②所示装置可说明浓 具有脱水性、强氧化性, 具有脱水性、强氧化性, 具有氧化性、还原性 具有氧化性、还原性 |
| C.图③装置可以用来验证化学能转化为电能 |
D.用图4所示装置比较 、 、 、 、 的氧化性强弱 的氧化性强弱 |
您最近一年使用:0次
名校
解题方法
4 . 实验室探究 溶液与
溶液与 的反应。
的反应。
I.如图所示制备(经检验装置气密性良好)。

(1)仪器a的名称是_______ 。
(2)写出C中制备 的离子方程式
的离子方程式_______ 。
II.探究 溶液与
溶液与 的反应,过程如图所示:
的反应,过程如图所示:

已知:硫酸亚铜易溶于水。
回答下列问题:
(3)加入 固体后产生的无色气体和白色沉淀经检验分别是
固体后产生的无色气体和白色沉淀经检验分别是 和
和 ,说明发生了氧化还原反应。加入
,说明发生了氧化还原反应。加入 固体发生反应的原因。
固体发生反应的原因。
a. 改变了
改变了 的还原性 b.
的还原性 b. 改变了
改变了 的氧化性
的氧化性
用原电池原理进行试验,探究上述现象可能的原因。
①由实验1、2可知原因a不合理,依据是_______ 。
②实验3:用如图所示装置实验,B中有白色沉淀生成,证明原因b合理。

i.补全电化学装置示意图_______ 。
ii.写出B中的电极反应方程式中_______ 。
iii.请从反应原理的角度解释原因: 与
与 的还原产物
的还原产物 形成沉淀,
形成沉淀,_______ ,使 与
与 的反应能够反应完全。
的反应能够反应完全。
 溶液与
溶液与 的反应。
的反应。I.如图所示制备(经检验装置气密性良好)。

(1)仪器a的名称是
(2)写出C中制备
 的离子方程式
的离子方程式II.探究
 溶液与
溶液与 的反应,过程如图所示:
的反应,过程如图所示:
已知:硫酸亚铜易溶于水。
回答下列问题:
(3)加入
 固体后产生的无色气体和白色沉淀经检验分别是
固体后产生的无色气体和白色沉淀经检验分别是 和
和 ,说明发生了氧化还原反应。加入
,说明发生了氧化还原反应。加入 固体发生反应的原因。
固体发生反应的原因。a.
 改变了
改变了 的还原性 b.
的还原性 b. 改变了
改变了 的氧化性
的氧化性用原电池原理进行试验,探究上述现象可能的原因。
| 编号 | 实验1 | 实验2 |
| 实验 |  |  |
| 现象 | 闭合开关K,电流计指针发生微小偏转,烧杯中未见明显现象 | 闭合开关K,电流计指针发生微小偏转,烧杯中未见明显现象 |
②实验3:用如图所示装置实验,B中有白色沉淀生成,证明原因b合理。

i.补全电化学装置示意图
ii.写出B中的电极反应方程式中
iii.请从反应原理的角度解释原因:
 与
与 的还原产物
的还原产物 形成沉淀,
形成沉淀, 与
与 的反应能够反应完全。
的反应能够反应完全。
您最近一年使用:0次
解题方法
5 . 浓差电池有多种:一种是利用物质氧化性或还原性强弱与浓度的关系设计的原电池(如图1):一种是根据电池中存在浓度差会产生电动势而设计的原电池(如图2)。图1所示原电池能在一段时间内形成稳定电流;图2所示原电池既能从浓缩海水中提取LiCl,又能获得电能。下列说法错误的是


| A.图1电流计指针不再偏转时,左右两侧溶液浓度恰好相等 |
| B.图1电流计指针不再偏转时向左侧加入NaCl或AgNO3或Fe粉,指针又会偏转且方向相同 |
| C.图2中Y极每生成1 mol Cl2,a极区得到2 mol LiCl |
| D.两个原电池外电路中电子流动方向均为从右到左 |
您最近一年使用:0次
解题方法
6 . 能量转化是化学变化的主要特征之一,按要求回答下列问题。
(1)页岩气是从页岩层中开采出来的天然气,成分以甲烷为主,页岩气的资源潜力可能大于常规天然气。下列有关页岩气的叙述错误的是_______(填序号)。
(2)有关的电池装置如下:
①上述四种电池中,属于二次电池的是_______ (填序号,下同),属于干电池的是_______ 。
②a装置中,外电路中电子的流向是_______ (填“从Zn流向Cu”或“从Cu流向Zn”)。
③c装置中,若电解质改为碱性介质,则负极的电极反应式为_______ 。
(3)氧化还原反应一般可以设计成原电池。若将反应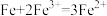 设计成原电池,则:
设计成原电池,则:
①该电池的电解质溶液可以是_______ 。
②当外电路中转移1mol e-时,电解质溶液增加的质量是_______ g。
(1)页岩气是从页岩层中开采出来的天然气,成分以甲烷为主,页岩气的资源潜力可能大于常规天然气。下列有关页岩气的叙述错误的是_______(填序号)。
| A.页岩气属于新能源 |
| B.页岩气和氧气的反应是放热反应 |
| C.甲烷中每个原子的最外层电子排布都达到8电子稳定结构 |
| D.页岩气可以作燃料电池的负极燃料 |
| 电池装置 | 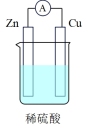 | 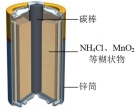 | 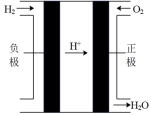 | 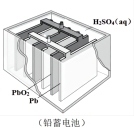 |
| 编号 | a | b | c | d |
①上述四种电池中,属于二次电池的是
②a装置中,外电路中电子的流向是
③c装置中,若电解质改为碱性介质,则负极的电极反应式为
(3)氧化还原反应一般可以设计成原电池。若将反应
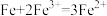 设计成原电池,则:
设计成原电池,则:①该电池的电解质溶液可以是
②当外电路中转移1mol e-时,电解质溶液增加的质量是
您最近一年使用:0次
11-12高二下·内蒙古包头·期中
名校
7 . 有关X、Y、Z、W四种金属进行如下实验:
根据以上事实,下列判断或推测错误的是
| ① | 将X和Y用导线连接,浸入电解质溶液中,Y不易腐蚀 |
| ② | 将片状的X、W分别投入等浓度盐酸中都有气体产生,W比X反应剧烈 |
| ③ | 用惰性电极电解等物质的量浓度的Y和Z的硝酸盐混合溶液,在阴极上首先析出单质Z |
| A.Z的阳离子氧化性最强 |
| B.W的还原性强于Y的还原性 |
| C.Z放入CuSO4溶液中一定有Cu析出 |
| D.用X、Z和稀硫酸可构成原电池,且X做负极 |
您最近一年使用:0次
2013-01-15更新
|
482次组卷
|
7卷引用:2011-2012学年内蒙古包头三十三中高二下学期期中考试化学试卷
(已下线)2011-2012学年内蒙古包头三十三中高二下学期期中考试化学试卷(已下线)2012-2013学年内蒙古巴市中学高二12月月考化学试卷(已下线)2014届浙江省杭州十四中高二上学期期末化学试卷 2015-2016学年浙江省海宁市三校高二下学期期中化学试卷模拟卷05(必考+选考)——2020年秋高三化学开学摸底考试卷(全国通用)河北省保定市唐县第一中学2020-2021学年高二9月月考化学试题甘肃省张掖市第二中学2021届高三上学期10月月考化学试题
名校
8 . 下列实验操作与现象及相关结论都正确的是
选项 | 实验操作及现象 | 结论 |
A | 常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者产生红棕色气体 | 浓硝酸的氧化性比稀硝酸强 |
B | 向溶有 的 的 溶液中通入气体X,出现白色沉淀 溶液中通入气体X,出现白色沉淀 | X一定具有强氧化性 |
C | 向溴水中加入苯,振荡后静置,水层颜色变浅 | 溴与苯发生了加成反应 |
D | 将银和 溶液与铜和 溶液与铜和 溶液组成原电池,连通后银表面有银白色金属沉积,铜电极附近溶液逐渐变蓝 溶液组成原电池,连通后银表面有银白色金属沉积,铜电极附近溶液逐渐变蓝 | Cu的金属性比Ag强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . X、Y、Z、M代表四种金属元素,金属X和Z用导线连接放入稀硫酸中时,Z极上有 放出;单质Z可以从Y的盐溶液中置换出单质Y;又知
放出;单质Z可以从Y的盐溶液中置换出单质Y;又知 的氧化性强于
的氧化性强于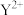 。则这四种金属的活动性由强到弱的顺序为
。则这四种金属的活动性由强到弱的顺序为
 放出;单质Z可以从Y的盐溶液中置换出单质Y;又知
放出;单质Z可以从Y的盐溶液中置换出单质Y;又知 的氧化性强于
的氧化性强于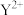 。则这四种金属的活动性由强到弱的顺序为
。则这四种金属的活动性由强到弱的顺序为A. | B. |
C. | D. |
您最近一年使用:0次
2023-05-07更新
|
914次组卷
|
5卷引用:甘肃省武威市天祝一中、民勤一中、古浪一中2022-2023学年高一下学期5月期中考试化学试题
甘肃省武威市天祝一中、民勤一中、古浪一中2022-2023学年高一下学期5月期中考试化学试题(已下线)【知识图鉴】单元讲练测必修第一册第四单元03巩固练(已下线)专题突破卷07 化学反应与能量?-2024年高考化学一轮复习考点通关卷(新教材新高考)(已下线)专题05 化学反应与能量变化(考点清单)(讲+练)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)(已下线)6.1.2 化学反应与电能
名校
解题方法
10 . 下列各项实验操作得出的现象及结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向2支均盛有2 mL相同浓度的AgNO3溶液的试管中,分别滴入2滴相同浓度的KCl、KI溶液 | 前者无明显现象,后者有黄色沉淀 | Ksp(AgI) <Ksp(AgCl) |
| B | 将铁粉加入过量浓硝酸中,加热充分反应,冷却后滴加KSCN溶液 | 有气体生成, 溶液最终呈无色 | 浓硝酸具有氧化性,将铁氧化成Fe2+ |
| C | 向蔗糖溶液中加入适量稀硫酸,水浴加热,冷却后向溶液中滴加新制Cu(OH)2悬浊液,加热 | 未出现砖红色沉淀 | 蔗糖未发生水解 |
| D | 向锌和稀硫酸反应的试管中滴加几滴CuSO4溶液 | 气泡生成速率加快 | CuSO4是该反应的催化剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



