1 . 一种清洁、低成本的三步法氯碱工艺工作原理的示意图如下,下列说法正确的是
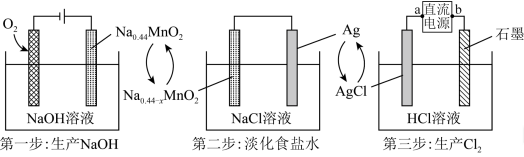
| A.第三步中a为直流电源的正极 |
B.第一步生产 的总反应为 的总反应为 |
| C.第二步为原电池,正极质量增加,负极质量减少 |
| D.第三步外电路上每转移4mol电子,电解池中就有4molHCl被电解 |
您最近一年使用:0次
2024-04-15更新
|
158次组卷
|
2卷引用:河北省金科大联考2023-2024学年高三上学期1月期末质量检测题化学试题
名校
2 . 利用如图装置处理碱性含CN-的废水,同时淡化海水(用NaCl溶液模拟海水),a电极和b电极均为惰性电极。下列说法错误的是
已知:阳极区溶液中离子放电顺序为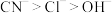 ,(未配平)。
,(未配平)。
已知:阳极区溶液中离子放电顺序为
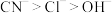 ,(未配平)。
,(未配平)。
A.CN-在阳极发生的电极反应为 |
| B.通电过程中阴极区溶液pH不断增大 |
| C.隔膜1为阴离子交换膜,隔膜2为阳离子交换膜 |
| D.将1molCN-完全转化成无污染物质时,外电路中至少需要转移4mol电子 |
您最近一年使用:0次
名校
3 . 利用钒电池电解含NH4NO3的废水制备硝酸和氨水的原理如下图所示,a、b、c、d均为惰性电极。下列说法中正确的是
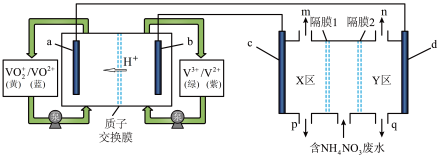

| A.用钒电池处理废水时,b电极区溶液由绿色变成紫色 |
| B.c为阴极,d为阳极 |
| C.隔膜1为阴离子交换膜 |
| D.当钒电池有2molH+通过质子交换膜时,共处理含80gNH4NO3的废水 |
您最近一年使用:0次
名校
4 . 某低成本储能电池原理如下图所示。下列说法正确的是
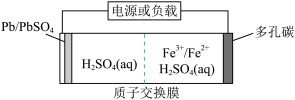

| A.放电时负极质量减小 | B.储能过程中电能转变为化学能 |
C.放电时右侧 通过质子交换膜移向左侧 通过质子交换膜移向左侧 | D.充电时阳极反应: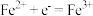 |
您最近一年使用:0次
2024-02-29更新
|
59次组卷
|
2卷引用:河北正定中学本部2023-2024学年高二上学期期末考试化学试题
名校
解题方法
5 . 2023年杭州亚运会的“数字火炬手”与最后一棒火炬手齐心协力点燃了象征亚洲大团结的亚运主火炬,也点燃了中国能源多样化战略的新灯塔绿色零增碳甲醇,整个过程只消耗太阳能,回答下列问题:
在某CO2催化加氢制CH3OH的反应体系中,发生的主要反应如下:
反应I.CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 
反应Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)  =+412kJ/mol
=+412kJ/mol
(1)表中数据是该反应中的相关物质的标准摩尔生成焓( )数据(标准摩尔生成烩是指在298.15K、100kPa由稳定态单质生成1mol化合物时的焓变)。
)数据(标准摩尔生成烩是指在298.15K、100kPa由稳定态单质生成1mol化合物时的焓变)。
则 =
=___________ ,反应I的热力学趋势较小,原因是___________ 。
(2)将CO2和H2按物质的量比1:2混合充入一恒容密闭容器中发生反应I、Ⅱ,已知反应Ⅱ的反应速率v正=k正x(CO2)·x(H2),v逆=k逆x(CO)·x(H2O), k正,k逆为速率常数,x为物质的量分数。当CO2转化率达到60%时,反应达到平衡状态,这时CO2和H2的体积分数相同,若反应Ⅱ的k正=20mol·L-1·s-1,平衡时反应Ⅱ的v逆=___________ mol·L-1·s-1。
(3)保持压强、CO2和H2的初始投料比不变进行反应,经相同时间测得如下实验数据(反应未达到平衡状态):
表中实验数据表明,温度高,CO2的实际转化率提高而甲醇的选择性降低,其原因是___________ 。
(4)CO和H2在ZnxO催化剂的作用下反应也可生成甲醇,其可能反应机理如下图所示。(资料显示:催化剂活化点位减少,吸附反应物能力会减弱)

在合成甲醇过程中,需要不断分离出甲醇的原因为___________ (填选项字母)。
a.有利于平衡正向移动 b.防止催化剂中毒 c.提高正反应速率
(5)此外,可用光电化学法将CO2还原为有机物实现碳资源的再生利用,其装置如左下图所示,其他条件一定时,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图所示:

FE%= ×100%其中,Q=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
×100%其中,Q=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
①当电解电压为u1V时,阴极生成HCHO的电极反应式为___________ 。
②当电解电压为u2V时,电解生成的HCOOH和HCHO的物质的量之比为3:2,则生成HCHO的法拉第效率为___________ 。
在某CO2催化加氢制CH3OH的反应体系中,发生的主要反应如下:
反应I.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 
反应Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)  =+412kJ/mol
=+412kJ/mol(1)表中数据是该反应中的相关物质的标准摩尔生成焓(
 )数据(标准摩尔生成烩是指在298.15K、100kPa由稳定态单质生成1mol化合物时的焓变)。
)数据(标准摩尔生成烩是指在298.15K、100kPa由稳定态单质生成1mol化合物时的焓变)。| 物质 | H2(g) | CO2(g) | H2O(g) | CH3OH(g) |
 /(kJ/mol) /(kJ/mol) | 0 | -394 | -242 | -201 |
 =
=(2)将CO2和H2按物质的量比1:2混合充入一恒容密闭容器中发生反应I、Ⅱ,已知反应Ⅱ的反应速率v正=k正x(CO2)·x(H2),v逆=k逆x(CO)·x(H2O), k正,k逆为速率常数,x为物质的量分数。当CO2转化率达到60%时,反应达到平衡状态,这时CO2和H2的体积分数相同,若反应Ⅱ的k正=20mol·L-1·s-1,平衡时反应Ⅱ的v逆=
(3)保持压强、CO2和H2的初始投料比不变进行反应,经相同时间测得如下实验数据(反应未达到平衡状态):
| T(K) | CO2实际转化率(%) | 甲醇选择性(%)(即转化的CO2中生成甲醇的百分比) |
| 543 | 12.3 | 42.3 |
| 553 | 15.3 | 39.1 |
(4)CO和H2在ZnxO催化剂的作用下反应也可生成甲醇,其可能反应机理如下图所示。(资料显示:催化剂活化点位减少,吸附反应物能力会减弱)

在合成甲醇过程中,需要不断分离出甲醇的原因为
a.有利于平衡正向移动 b.防止催化剂中毒 c.提高正反应速率
(5)此外,可用光电化学法将CO2还原为有机物实现碳资源的再生利用,其装置如左下图所示,其他条件一定时,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图所示:

FE%=
 ×100%其中,Q=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
×100%其中,Q=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。①当电解电压为u1V时,阴极生成HCHO的电极反应式为
②当电解电压为u2V时,电解生成的HCOOH和HCHO的物质的量之比为3:2,则生成HCHO的法拉第效率为
您最近一年使用:0次
名校
6 . 用一种具有“卯榫”结构的双极膜组装电解池(下图),可实现大电流催化电解KNO3溶液制氨。工作时H2O在双极膜界面处被催化解离成H+和OH-,有利于电解反应顺利进行。下列说法错误的是
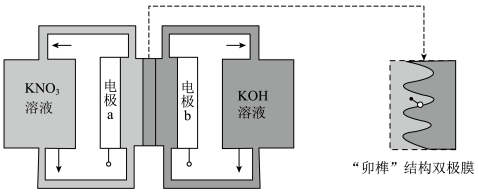

| A.相比于平面结构双极膜,“卯榫”结构可提高氮生成速率 |
B.阴极反应式为 +7H2O+8e-=NH3·H2O+9OH- +7H2O+8e-=NH3·H2O+9OH- |
| C.每生成1molNH3·H2O,双极膜界面处产生9mol的H+移向电极a |
| D.电解过程中,阳极室中KOH的物质的量不因反应而改变 |
您最近一年使用:0次
名校
解题方法
7 . 下列有关电极方程式或离子方程式正确的是
A.以铜电极电解饱和食盐水的电解方程式:2Cl-+2H2O 2OH-+Cl2↑+H2↑ 2OH-+Cl2↑+H2↑ |
| B.铅蓄电池充电时的阳极反应:Pb2++2H2O-2e-=PbO2+4H+ |
C.少量SO2通入NaClO溶液:3ClO-+SO2+H2O= +2HClO+Cl- +2HClO+Cl- |
D.Al2(SO4)3溶液中加入过量氨水:Al3++4NH3·H2O=[Al(OH)4]-+4 |
您最近一年使用:0次
名校
解题方法
8 . 氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。
I.空间站是以水为介质将不同形式的能量相互转化。原理如图所示。装置x为电解水,装置y为燃料电池。

(1)太阳能电池的能量转化形式为_______ (填字母)。
A.化学能转化为电能 B.电能转化为化学能 C.太阳能转化为电能
(2)装置x工作时,产生O2的电极为_____ 极(填“阳”或“阴”)。
(3)装置y工作时,若电解质溶液为稀硫酸,则正极反应式为______ 。
II.氢能的利用包括氢的制备、储存和应用三个环节。
(4)氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:_______ 。
(5)化工生产的副产物也是氢气的来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH- FeO
FeO +3H2↑,工作原理如图所示,装置通电后,铁电极附近生成紫红色的FeO
+3H2↑,工作原理如图所示,装置通电后,铁电极附近生成紫红色的FeO ,镍电极有气泡产生,若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质,已知:Na2FeO4只在强碱性条件下稳定,且易被H2还原。
,镍电极有气泡产生,若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质,已知:Na2FeO4只在强碱性条件下稳定,且易被H2还原。
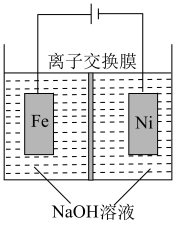
①电解一段时间后,c(OH—)降低的区域在______ (填“阴极室”或“阳极室”)。
②电解过程中,需将阴极产生的气体及时排出,其原因是______ 。
I.空间站是以水为介质将不同形式的能量相互转化。原理如图所示。装置x为电解水,装置y为燃料电池。

(1)太阳能电池的能量转化形式为
A.化学能转化为电能 B.电能转化为化学能 C.太阳能转化为电能
(2)装置x工作时,产生O2的电极为
(3)装置y工作时,若电解质溶液为稀硫酸,则正极反应式为
II.氢能的利用包括氢的制备、储存和应用三个环节。
(4)氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:
(5)化工生产的副产物也是氢气的来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH-
 FeO
FeO +3H2↑,工作原理如图所示,装置通电后,铁电极附近生成紫红色的FeO
+3H2↑,工作原理如图所示,装置通电后,铁电极附近生成紫红色的FeO ,镍电极有气泡产生,若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质,已知:Na2FeO4只在强碱性条件下稳定,且易被H2还原。
,镍电极有气泡产生,若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质,已知:Na2FeO4只在强碱性条件下稳定,且易被H2还原。
①电解一段时间后,c(OH—)降低的区域在
②电解过程中,需将阴极产生的气体及时排出,其原因是
您最近一年使用:0次
名校
解题方法
9 . 硒是典型的半导体材料,在光照下导电性可提高近千倍。如图是从某工厂的硒化银半导体废料(含Ag2Se、Cu单质)中提取硒、银的工艺流程图:
(1)已知反应③生成一种可参与大气循环的气体单质,写出该反应的离子程式_______ 。
(2)已知:常温下Ag2SO4、AgCl的饱和溶液中阳离子和阴离子浓度关系如图所示,反应②为_______ (写离子方程式);该反应的化学平衡常数的数量级为_______ 。 、SeO
、SeO 摩尔分数随pH的变化如图所示,则室温下SeO
摩尔分数随pH的变化如图所示,则室温下SeO 的Kh=
的Kh=________ 。_______ (写电极反应式)。

(1)已知反应③生成一种可参与大气循环的气体单质,写出该反应的离子程式
(2)已知:常温下Ag2SO4、AgCl的饱和溶液中阳离子和阴离子浓度关系如图所示,反应②为

 、SeO
、SeO 摩尔分数随pH的变化如图所示,则室温下SeO
摩尔分数随pH的变化如图所示,则室温下SeO 的Kh=
的Kh=
您最近一年使用:0次
10 . 一种清洁、低成本的三步法氯碱工艺工作原理的示意图如下,下列说法正确的是
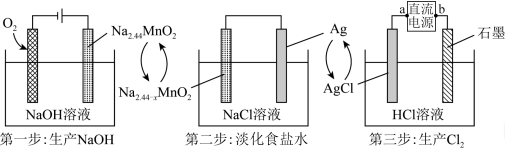
| A.第三步中a为直流电源的正极 |
B.第一步生产 的总反应为 的总反应为 |
| C.第二步为原电池,正极质量增加,负极质量减少 |
D.第三步外电路上每转移 电子,电解池中就有 电子,电解池中就有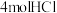 被电解 被电解 |
您最近一年使用:0次
2024-02-24更新
|
321次组卷
|
3卷引用:河北省石家庄市辛集中学、衡水中学2023-2024高三上学期期末联考化学试题



