1 . 乙烯的产量被用作衡量一个国家石油化工产业发展水平的标志,截至2022年底,我国乙烯产能首次超过美国,成为世界乙烯产能第一大国。已知乙烯能发生以下转化(部分条件和产物已略去):

(1)A中官能团的名称为___________ ,A转化为乙醛的化学方程式为___________ 。
(2)B能去除少量水垢(主要成分 ),是利用了B的
),是利用了B的___________ 性。
(3)上图中生成氯乙烷的反应类型为___________ 。
(4)某研究小组利用A与B反应制备乙酸乙酯的装置如下图。
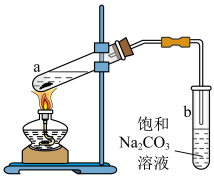
①试管a中反应的化学方程式为___________ 。
②试管b中导气管下端管口不浸入液面的目的是___________ 。
(5)C是高分子化合物,可用于制作食品塑料袋,C的结构简式为___________ 。

(1)A中官能团的名称为
(2)B能去除少量水垢(主要成分
 ),是利用了B的
),是利用了B的(3)上图中生成氯乙烷的反应类型为
(4)某研究小组利用A与B反应制备乙酸乙酯的装置如下图。

①试管a中反应的化学方程式为
②试管b中导气管下端管口不浸入液面的目的是
(5)C是高分子化合物,可用于制作食品塑料袋,C的结构简式为
您最近一年使用:0次
名校
解题方法
2 . 下列探究方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 室温下,测定浓度均为 的 的 、 、 溶液的pH 溶液的pH | 比较室温下 和 和 的电离能力 的电离能力 |
| B | 将浓硫酸和灼热木炭反应产生的气体依次通过品红溶液、饱和 溶液、澄清石灰水,观察现象 溶液、澄清石灰水,观察现象 | 浓硫酸和木炭反应产生 和 和 气体 气体 |
| C | 将少量 溶于过量热浓盐酸中,再滴加几滴 溶于过量热浓盐酸中,再滴加几滴 溶液,观察溶液颜色变化 溶液,观察溶液颜色变化 |  中含 中含 |
| D | 向含有少量乙酸的乙酸乙酯中加入过量NaOH溶液,振荡后静置分液 | 提纯含有少量乙酸的乙酸乙酯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-11更新
|
702次组卷
|
3卷引用:T11-化学实验方案的设计与评价
解题方法
3 . 实验室中可利用如图装置制取乙酸乙酯。下列说法正确的是


| A.乙酸乙酯的羧酸类同分异构体有3种 |
| B.长颈漏斗除起到导气冷凝的作用外还起到防止倒吸的作用 |
| C.若实验中用的乙醇为CH3CH218OH,则所得乙酸乙酯的相对分子质量为88 |
| D.试管b中溶液可选用NaOH溶液,用于除去乙酸乙酯中的乙酸 |
您最近一年使用:0次
4 . 实验室常用如图装置制备乙酸乙酯。下列有关说法错误的是
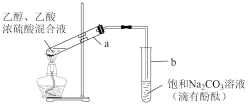

| A.a中试剂加入的顺序是:先加冰醋酸,再加浓硫酸,最后加无水乙醇 |
| B.b中导管不能插入液面下,否则会产生倒吸现象 |
| C.实验中使用浓硫酸和过量的乙醇,都可以提高乙酸的转化率 |
| D.b中的现象是液体分层,上层无色油状液体,下层溶液颜色变浅 |
您最近一年使用:0次
5 . 下列实验不能用下图实验装置进行的是
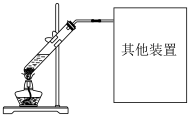

| A.乙醇与乙酸反应制备乙酸乙酯 |
| B.浓硫酸与Cu反应制备二氧化硫 |
| C.蓝矾分解制备少量无水硫酸铜 |
| D.浓硫酸与甲酸共热反应制备少量一氧化碳 |
您最近一年使用:0次
解题方法
6 . 某同学用如图1所示的装置制备乙酸乙酯,并设计了如图2所示的步骤进一步分离,得到较为纯净的乙酸乙酯,并回收乙醇和乙酸。下列说法错误的是
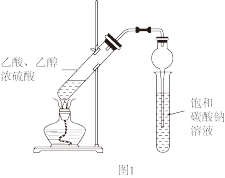
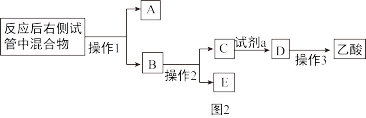


| A.球形干燥管具有防倒吸的作用 |
| B.操作1是分液,操作2和操作3是蒸馏 |
| C.A是乙酸乙酯,E是乙醇,试剂a可以是硫酸 |
| D.该实验应迅速升温到170℃ |
您最近一年使用:0次
解题方法
7 . 某小组利用如图装置(部分夹持和加热装置略去)

(1)实验前,向试管Ⅰ中加入3mL___ ,然后边振试管边慢慢加入2mL___ 和2mL乙酸。
(2)试管Ⅰ中生成乙酸乙酯的化学反应方程式是___ 。
(3)与教材实验装置不同,甲装置中采用了球形干燥管,作用是冷凝乙酸乙酯和___ 。
(4)若反应前向试管Ⅱ中加入几滴酚酞,溶液呈红色。实验完毕后,将试管Ⅱ中的溶液充分振荡、静置,现象为___ 。
(5)将试管Ⅱ中的溶液转移到乙装置中,进行___ (填操作名称),分离出的上层液体为___ (填物质名称)。
(6)下层液体利用丙装置进一步分离。实验时应在蒸馏烧瓶中放少量碎瓷片,目的是___ ;实验过程中,冷却水应从___ (填“a”或“b”)口进入。
(7)该实验用30g乙酸与46g乙醇反应,如果实际得到的乙酸乙酯的质量是26.4g,则该实验中乙酸乙酯的产率是__ 。(产率指某种生成物的实际产量与理论产量的比值)

(1)实验前,向试管Ⅰ中加入3mL
(2)试管Ⅰ中生成乙酸乙酯的化学反应方程式是
(3)与教材实验装置不同,甲装置中采用了球形干燥管,作用是冷凝乙酸乙酯和
(4)若反应前向试管Ⅱ中加入几滴酚酞,溶液呈红色。实验完毕后,将试管Ⅱ中的溶液充分振荡、静置,现象为
(5)将试管Ⅱ中的溶液转移到乙装置中,进行
(6)下层液体利用丙装置进一步分离。实验时应在蒸馏烧瓶中放少量碎瓷片,目的是
(7)该实验用30g乙酸与46g乙醇反应,如果实际得到的乙酸乙酯的质量是26.4g,则该实验中乙酸乙酯的产率是
您最近一年使用:0次
8 . 二苄叉丙酮是一种催化剂配体,可用于制备钯催化剂,实验室可用苯甲醛和丙酮在碱性条件下制得二苄叉丙酮(反应大量放热),反应原理如图:
 →2H2O+
→2H2O+
实验步骤:
I.称取2.0g氢氧化钠溶于20mL水和16mL乙醇组成的混合溶液中,冷却后装入100mL的三颈瓶,置于水浴中,放入搅拌磁子(如图1)。称取2.1g苯甲醛(沸点179℃)与0.8g丙酮(沸点56℃)并混合好,将混合物的一半加入碱溶液,控制混合物温度在20-25℃,快速搅拌2-3分钟后,产生黄色絮状沉淀。15分钟后,用胶头滴管加入剩余混合物,继续搅拌半个小时,得到大量黄色絮状沉淀。
II.将三颈瓶中的混合物转入抽滤装置(如图2),抽滤后用大量水洗至滤液接近中性后,将沉淀室温干燥,得粗晶体。

III.取粗晶体于茄形瓶中,组装好重结晶装置(如图3),通冷凝水后向茄形瓶中加入适量95%乙醇并用油浴加热,待粗产品完全溶解后,先缓慢冷却到室温,再用冰水浴冷却,抽滤,冰水洗涤、干燥、称量得到1.8g纯二苄叉丙酮晶体。

请回答下列问题。
(1)球形冷凝管的作用是冷凝回流,其冷凝效果_______ (填“强于”或“弱于”)直形冷凝管,原因是_______ 。
(2)步骤一中苯甲醛和丙酮的混合物分两次加入并用水浴控制温度的目的是_______ 。搅拌的目的是_______ 。
(3)抽滤又叫减压过滤,过滤速度明显高于普通过滤,原因是_______ 。步骤二中抽滤后水洗至滤液接近中性是为了确保除去粗晶体表面吸附的_______ 。
(4)步骤三中粗产品完全溶解后不直接用冰水浴冷却的原因是_______ 。
(5)该实验中二苄叉丙酮的产率是_______ 。(保留两位有效数字)
 →2H2O+
→2H2O+
实验步骤:
I.称取2.0g氢氧化钠溶于20mL水和16mL乙醇组成的混合溶液中,冷却后装入100mL的三颈瓶,置于水浴中,放入搅拌磁子(如图1)。称取2.1g苯甲醛(沸点179℃)与0.8g丙酮(沸点56℃)并混合好,将混合物的一半加入碱溶液,控制混合物温度在20-25℃,快速搅拌2-3分钟后,产生黄色絮状沉淀。15分钟后,用胶头滴管加入剩余混合物,继续搅拌半个小时,得到大量黄色絮状沉淀。

II.将三颈瓶中的混合物转入抽滤装置(如图2),抽滤后用大量水洗至滤液接近中性后,将沉淀室温干燥,得粗晶体。

III.取粗晶体于茄形瓶中,组装好重结晶装置(如图3),通冷凝水后向茄形瓶中加入适量95%乙醇并用油浴加热,待粗产品完全溶解后,先缓慢冷却到室温,再用冰水浴冷却,抽滤,冰水洗涤、干燥、称量得到1.8g纯二苄叉丙酮晶体。

请回答下列问题。
(1)球形冷凝管的作用是冷凝回流,其冷凝效果
(2)步骤一中苯甲醛和丙酮的混合物分两次加入并用水浴控制温度的目的是
(3)抽滤又叫减压过滤,过滤速度明显高于普通过滤,原因是
(4)步骤三中粗产品完全溶解后不直接用冰水浴冷却的原因是
(5)该实验中二苄叉丙酮的产率是
您最近一年使用:0次



