1 . 下列元素相关基态粒子的电子排布式中,前者一定是金属元素,后者一定是非金属元素的是
A. 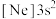 | B.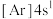 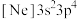 |
C. 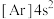 | D. 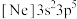 |
您最近一年使用:0次
2024-02-25更新
|
138次组卷
|
14卷引用:河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1
河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1宁夏吴忠市2017-2018学年高二人教版选修3化学同步练习:第1章 原子结构与性质综合练习1【全国百强校】河北省武邑中学2017-2018学年高二下学期期末考试化学试题云南省盐津县第一中学2018-2019学年高二上学期12月份考试化学试题山西省平遥中学校2018-2019学年高二下学期第二次月考化学试题吉林省松原市扶余市第一中学2019-2020学年高二下学期期中考试化学试题广西壮族自治区北海市2019-2020学年高二下学期期末教学质量检测化学试题山西省运城市2019-2020学年高二下学期期末测试化学试题(已下线)模块同步卷02 原子结构与元素的性质-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)河南省辉县市一中2020-2021学年高二(培优班)下学期第二次阶段性考试化学试题海南省儋州川绵中学2021-2022学年高二下学期第一次月考化学试题广东省惠州市惠东县惠东荣超中学2021-2022学年高二下学期期中考试 化学试题(已下线)1.1.2 构造原理与电子排布式、电子云与原子轨道课堂例题广东梅州五华县中英文实验学校2023-2024学年高二下学期3月考试化学试题
名校
解题方法
2 . 已知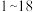 号元素的离子
号元素的离子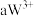 、
、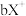 、
、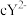 、
、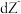 都具有相同电子层结构,下列关系正确的是
都具有相同电子层结构,下列关系正确的是
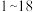 号元素的离子
号元素的离子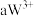 、
、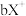 、
、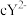 、
、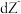 都具有相同电子层结构,下列关系正确的是
都具有相同电子层结构,下列关系正确的是A.质子数: ,离子的还原性: ,离子的还原性: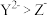 |
B.电负性: |
C.氢化物的稳定性: |
D.原子半径: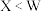 ,第一电离能: ,第一电离能: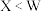 |
您最近一年使用:0次
2022-12-02更新
|
1061次组卷
|
33卷引用:河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1
河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测12016-2017学年河北省衡水中学高二上学期五调考试化学试卷人教版2017-2018学年高二化学选修三同步训练:第一章 原子结构与性质1河北省石家庄市启明中学2019-2020学年高二四月月考化学试题鲁科版(新)必修第二册第一章检测题(已下线)模块同步卷03 第一章综合检测-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)2015-2016学年贵州省思南中学高二下第一次月考化学试卷2015-2016学年山西大学附属中学高二下3月月考化学试卷2015-2016学年吉林省汪清六中高二3月月考化学试卷2015-2016学年山西大学附中高二下3月月考化学试卷2016-2017学年河南省洛阳市第一高级中学高二(平行班)3月月考化学试卷2016-2017学年山西省大同市第一中学高二3月月考化学试卷福建省三明市第一中学2016-2017学年高二下学期半期考试化学试题贵州省思南中学2016-2017学年高二下学期期中考试化学试题吉林省辽源五中2017-2018学年高二下学期第一次月考化学试题【全国百强校】甘肃省嘉峪关市酒钢三中2017-2018学年高二下学期期中考试化学试题【全国百强校】宁夏吴忠中学2017-2018学年高二6月月考化学试题2020届高三化学二轮物质结构题型专攻——元素性质的递变规律【选择提升专练】福建省厦门市思明区厦门外国语学校2019-2020学年高二上学期周末练习10——化学试题河南省林州市林虑中学2019-2020学年高二3月线上考试化学试题吉林省白山市第七中学2019-2020学年高二下学期3月份月考化学试题辽宁省六校协作体2019-2020学年高二下学期期中考试化学试卷(鲁科版2019)选择性必修2 第1章 原子结构与元素性质 第3节 元素性质及其变化规律(人教版2019)选择性必修2 第一章 原子结构与性质 第二节 原子结构与元素的性质(人教版2019)选择性必修2第一章 原子结构与性质 第二节 原子结构与元素的性质 第3课时 元素的电负性及其变化规律鲁科版2019选择性必修2第1章 原子结构与元素性质 第3节 元素性质及其变化规律 第2课时 元素的电负性及其变化规律专题强化练2 电离能和电负性的应用吉林省辉南县第六中学2022-2023学年高二上学期期中考试化学试题湖南省长沙市周南中学2022-2023学年高二上学期期末考试化学试题安徽省池州市第一中学2022-2023学年高二下学期第一次月考化学试题北京市第三十五中学2021-2022学年高三上学期期中考试化学试题四川省内江市资中县第二中学2023-2024学年高二下学期3月月考化学试题黑龙江省黑河市第一中学2023-2024学年高二下学期4月月考化学试题
名校
3 . 下列基态原子的电子排布式、价电子排布式或排布图不正确的是
| A.Al 3s23p1 | B.As [Ar]4s24p3 |
| C.Ar 3s23p6 | D.Ni 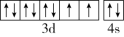 |
您最近一年使用:0次
2021-05-24更新
|
253次组卷
|
14卷引用:河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1
河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测12016-2017学年河北省衡水中学高二上学期五调考试化学试卷【全国百强校】四川省绵阳市南山中学2018-2019学年高二9月月考化学试题辽宁省凤城市第一中学2018-2019学年高二6月月考化学试题新疆石河子第二中学2018-2019学年高二下学期第一次月考化学试题(已下线)专题11.1 原子结构与性质(练)-《2020年高考一轮复习讲练测》辽宁省阜新市第二高级中学2019-2020学年高二下学期第一次月考化学试题四川省阿坝州九寨沟2019-2020学年高二上学期期末考试化学试题陕西省周至县第二中学2020-2021学年高二上学期期末考试化学试题吉林省乾安县第七中学2020-2021学年高二下学期第六次质量检测化学试题黑龙江省哈尔滨市第六中学2021-2022学年高二下学期期中考试化学试题四川省宜宾市叙州区第二中学校2022-2023学年高二下学期开学考试化学试题湖北省十堰市普通高中协作体2022-2023学年高二下学期3月月考化学试题宁夏银川市唐徕中学2022-2023学年高二下学期期中考试化学试题
名校
解题方法
4 . 如图为周期表中部分元素某种性质(X值)随原子序数变化的关系。

(1)短周期中原子核外p能级上电子数与s能级上电子总数相等的元素是___ (填元素符号)。
(2)同主族内不同元素的X值变化的特点是___ ;同周期内,随着原子序数的增大,X值的变化总趋势是___ 。周期表中X值的这种变化特点体现了元素性质的___ 变化规律。
(3)X值较小的元素集中在元素周期表的___ (填序号,下同)。
a.左下角 b.右上角 c.分界线附近
(4)下列说法正确的是___ 。
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱

(1)短周期中原子核外p能级上电子数与s能级上电子总数相等的元素是
(2)同主族内不同元素的X值变化的特点是
(3)X值较小的元素集中在元素周期表的
a.左下角 b.右上角 c.分界线附近
(4)下列说法正确的是
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱
您最近一年使用:0次
2020-04-09更新
|
485次组卷
|
6卷引用:河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1
河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1第1章 原子结构 易错疑难集训(二)——A学习区 夯实基础(鲁科版选修3)(已下线)第一单元 原子结构(能力提升)-2020-2021学年高二化学单元测试定心卷(鲁科版选修3)(已下线)易错25 电离能和电负性-备战2021年高考化学一轮复习易错题安徽省 淮北师范大学附属实验中学2022-2023学年高二下学期第一次月考化学试题山东省平邑县第一中学2022-2023学年高二下学期第一次月考化学试题
5 . “胃舒平的主要成分是氢氧化铝,同时含有三硅酸镁(Mg2Si3O8·H2O)等化合物。下列叙述中错误的是
| A.镁元素基态原子的核外电子排布式是1s22s22p63s2 |
| B.铝元素原子核外共有5种不同运动状态的电子。 |
| C.钠元素离子半径比铝离子半径大 |
| D.金属铝与钠的最高价氧化物对应的水化物溶液发生反应的离子方程式为2A1+2OH-+2H2O=2A1O2⁻+3H2↑ |
您最近一年使用:0次
2020-03-23更新
|
544次组卷
|
10卷引用:河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1
河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1人教版2017-2018学年高二化学选修三同步训练:第一章 原子结构与性质1(已下线)第1章 章末综合测评B-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修1)2015-2016学年贵州省思南中学高二下第一次月考化学试卷2020届高三化学二轮物质结构题型专攻——原子结构与性质【基础专练】河南省林州市林虑中学2019-2020学年高二3月线上考试化学试题(已下线)模块同步卷01 原子结构和元素周期律-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)广东省东莞市新世纪英才学校2021-2022学年高二上学期第一次教学质量检测化学试题广东省东莞市第四高级中学2022-2023学年高二上学期期中考试化学试题(已下线)BBWYhjhx1112.pdf
名校
解题方法
6 . 有A、B、C、D、E、F六种主族元素,有关信息如下:
①短周期元素C原子的价电子排布式为:ns2np2,E的单质可在空气中燃烧;
②下表是元素周期表中主族元素的一部分:
③A、B同周期,其电离能数据如下(单位:kJ·mol-1):
试回答下列问题:
(1)F原子的核外电子排布式为__________________ 。
(2)C、D、E元素的电负性相对大小为____________________ (用元素符号表示)。
(3)C的最高价氧化物与烧碱溶液反应的离子方程式为_______________________ 。
(4)化合价是元素的一种性质,由A、B的电离能数据判断下列说法正确的是________ (填序号)。
a.A通常显+1价,B通常显+4价
b.B元素的第一电离能较小,其活泼性比A强
c.A、B的单质分别与盐酸反应放出等量氢气时,消耗单质的物质的量之比为3:2
①短周期元素C原子的价电子排布式为:ns2np2,E的单质可在空气中燃烧;
②下表是元素周期表中主族元素的一部分:
| C | D | E |
| F |
| I1 | I2 | I3 | I4 | |
| A | 738 | 1451 | 7733 | 10540 |
| B | 578 | 1817 | 2745 | 11575 |
(1)F原子的核外电子排布式为
(2)C、D、E元素的电负性相对大小为
(3)C的最高价氧化物与烧碱溶液反应的离子方程式为
(4)化合价是元素的一种性质,由A、B的电离能数据判断下列说法正确的是
a.A通常显+1价,B通常显+4价
b.B元素的第一电离能较小,其活泼性比A强
c.A、B的单质分别与盐酸反应放出等量氢气时,消耗单质的物质的量之比为3:2
您最近一年使用:0次
2018-02-12更新
|
978次组卷
|
2卷引用:河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1
7 . 第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的最低能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图。
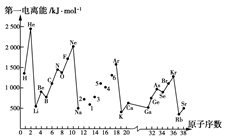
请回答以下问题:
(1)认真分析上图中同周期元素第一电离能的变化规律,将Na~Ar之间的元素用短线连接起来,构成完整的图象________ 。
(2)从上图分析可知,同一主族元素原子的第一电离能I1的变化规律是_________ 。
(3)上图中5号元素在周期表中的位置是_________________________________ 。
(4)上图中4、5、6号三种元素的气态氢化物的化学式分别为__________________ 。
(5)上图中1~6号元素中,最高价氧化物对应水化物中酸性最强的是_______ ,两性化合物有______ 。

请回答以下问题:
(1)认真分析上图中同周期元素第一电离能的变化规律,将Na~Ar之间的元素用短线连接起来,构成完整的图象
(2)从上图分析可知,同一主族元素原子的第一电离能I1的变化规律是
(3)上图中5号元素在周期表中的位置是
(4)上图中4、5、6号三种元素的气态氢化物的化学式分别为
(5)上图中1~6号元素中,最高价氧化物对应水化物中酸性最强的是
您最近一年使用:0次
名校
8 . 回答下列问题:
(1)已知铁是26号元素,写出Fe的价层电子排布式________ ;在元素周期表中,该元素在________ (填“s”“p”“d”“f”或“ds”)区。
(2)写出与N同主族的As的基态原子的核外电子排布式:__________________ 。从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为________ 。
(3)写出Fe2+的核外电子排布式:________ 。
(4)Zn2+的核外电子排布式为________ 。
(1)已知铁是26号元素,写出Fe的价层电子排布式
(2)写出与N同主族的As的基态原子的核外电子排布式:
(3)写出Fe2+的核外电子排布式:
(4)Zn2+的核外电子排布式为
您最近一年使用:0次
名校
9 . 甲、乙两元素原子的L层电子数都是其他层电子总数的2倍。下列推断正确的是( )
| A.甲与乙位于同一周期 |
| B.甲与乙位于同一主族 |
| C.甲与乙都位于元素周期表的p区 |
| D.甲与乙的原子序数之和为偶数 |
您最近一年使用:0次
2018-02-12更新
|
500次组卷
|
10卷引用:河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1
河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1云南省曲靖市沾益二中2017-2018学年高二下学期期末考试化学试题吉林省白山市第七中学2018-2019学年高二下学期期中考试化学试题云南省永平县第二中学2019-2020学年高二上学期期末考试化学试题江苏省如东高级中学2019-2020学年高一下学期第二次阶段测试化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题(已下线)模块同步卷02 原子结构与元素的性质-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)四川省达州市第一中学校2022-2023学年高二上学期10月月考化学试题湖北省十堰市普通高中协作体2022-2023学年高二下学期3月月考化学试题湖北省武汉西藏中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
10 . 下列有关原子核外电子排布规律,说法正确的是( )
| A.原子核外电子都是先排内层后排外层 |
| B.Fe2+的价层电子排布式为3d54s1 |
C.15P原子的电子排布式是1s22s22p63s23p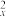 3p 3p |
| D.同一原子中,1s、2s、3s能级最多容纳的电子数相同 |
您最近一年使用:0次



