解题方法
1 . 卢瑟福发现质子的核反应为 ;卢瑟福的学生查德威克发现中子的核反应为
;卢瑟福的学生查德威克发现中子的核反应为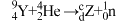 。下列说法错误的是
。下列说法错误的是
 ;卢瑟福的学生查德威克发现中子的核反应为
;卢瑟福的学生查德威克发现中子的核反应为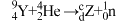 。下列说法错误的是
。下列说法错误的是| A.Y元素的第一电离能高于同周期相邻元素的 |
B.元素的电负性: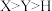 |
C. 和 和 的简单氢化物中中心原子的价层电子对数目相同 的简单氢化物中中心原子的价层电子对数目相同 |
D. 的空间结构为直线形 的空间结构为直线形 |
您最近一年使用:0次
名校
解题方法
2 . 科学家研发出一种新型储氢材料,晶胞结构如下图所示,晶胞参数为apm,下列说法正确的是
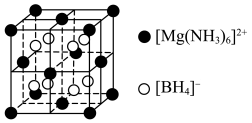
| A.所含非金属元素的电负性N>B>H |
B.该晶体的化学式为 |
C.阴、阳离子的最小距离为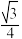 apm apm |
| D.若晶胞以[BH4]-为顶点,所得晶胞结构与NaCl晶胞相同 |
您最近一年使用:0次
3 . 离子液体被广泛应用于化工生产的分离过程,也是许多反应的优良溶剂。某离子液体结构如图所示。W、X、Y、Z为原子序数依次增大的主族元素,W、X和Y的原子序数之和为14,Z是第四周期元素。下列说法错误的是
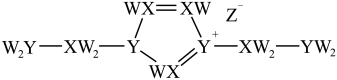
| A.X、Z的简单氢化物均可溶于水 |
| B.最高价氧化物的水化物酸性:Y>X |
| C.第一电离能:Y>X |
| D.X、Y、Z都位于元素周期表p区 |
您最近一年使用:0次
4 . 下列说法错误的是
| A.已知电负性:Si<H<Cl,则SiHCl3水解时发生氧化还原反应 |
| B.已知Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O,则氧化剂与还原剂物质的量之比为1:2 |
C.已知Na+KCl(熔融) K+NaCl,则可推知钠的还原性和金属性都强于钾 K+NaCl,则可推知钠的还原性和金属性都强于钾 |
| D.已知4KO2+2H2O=4KOH+3O2,则O2为氧化产物 |
您最近一年使用:0次
2024-05-11更新
|
137次组卷
|
2卷引用:河北省石家庄市第十七中学2023-2024学年高三下学期第一次月考化学试题
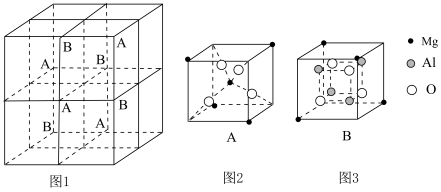
5 . 某晶体由镁、铝、氧三种元素组成,若将其晶胞按图1方式切成8个体积相同的小立方体,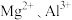 和
和 在小立方体中的分布如图2、图3所示.已知
在小立方体中的分布如图2、图3所示.已知 之间的最小间距为
之间的最小间距为 .下列说法错误的是
.下列说法错误的是
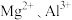 和
和 在小立方体中的分布如图2、图3所示.已知
在小立方体中的分布如图2、图3所示.已知 之间的最小间距为
之间的最小间距为 .下列说法错误的是
.下列说法错误的是
A.晶体的化学式为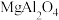 | B.晶体中三种元素的第一电离能: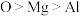 |
C.晶胞的体积为 | D.晶体中 的配位数为4 的配位数为4 |
您最近一年使用:0次
6 . 下列说法正确的是
A. 的空间结构与其VSEPR模型相同 的空间结构与其VSEPR模型相同 |
B.氢键 中的三原子均在一条直线上 中的三原子均在一条直线上 |
| C.基态O原子核外电子的运动状态有8种 |
| D.第一电离能和电负性的大小可分别作为判断元素金属性和非金属性强弱的依据 |
您最近一年使用:0次
解题方法
7 . 不锈钢是由铁、铬、镍、碳及多种不同元素所组成的合金,铁是主要成分元素,铬是第一主要的合金元素。其中铬的含量不能低于11%,不然就不能生成致密氧化膜 。回答下列问题:
。回答下列问题: 的电子排布式:
的电子排布式:___________ 。基态镍原子的未成对电子数为___________ 。
(2)铁和镍位于元素周期表的同一周期同一族,它们均位于第___________ 周期第___________ 族。
(3)金属铜及镍都是由金属键形成的晶体,元素铜与镍的第二电离能分别为: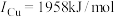 、
、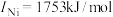 ,
,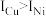 的原因是
的原因是___________ 。
(4)某镍镧合金是优质储氢材料,其晶胞如图所示,则它的化学式为___________ 。 的一种晶体如图甲、乙所示。
的一种晶体如图甲、乙所示。___________ 。
②若按甲中虚线(面对角线)方向切乙,得到的图像正确的是___________ (填字母)。 ,则晶体中铬原子的半径为
,则晶体中铬原子的半径为___________  (阿伏加德罗常数的值为
(阿伏加德罗常数的值为 ,列出表达式)。
,列出表达式)。
 。回答下列问题:
。回答下列问题:
 的电子排布式:
的电子排布式:(2)铁和镍位于元素周期表的同一周期同一族,它们均位于第
(3)金属铜及镍都是由金属键形成的晶体,元素铜与镍的第二电离能分别为:
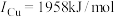 、
、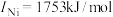 ,
,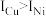 的原因是
的原因是(4)某镍镧合金是优质储氢材料,其晶胞如图所示,则它的化学式为
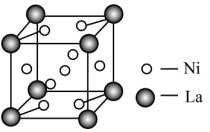
 的一种晶体如图甲、乙所示。
的一种晶体如图甲、乙所示。
②若按甲中虚线(面对角线)方向切乙,得到的图像正确的是
A. B.
B. C.
C. D.
D.
 ,则晶体中铬原子的半径为
,则晶体中铬原子的半径为 (阿伏加德罗常数的值为
(阿伏加德罗常数的值为 ,列出表达式)。
,列出表达式)。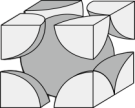
您最近一年使用:0次
解题方法
8 . 下列说法正确的是
A. 的电子排布式 的电子排布式 ,违反了泡利不相容原理 ,违反了泡利不相容原理 |
B.因硫元素核电荷数比磷元素大,故硫元素 比磷元素 比磷元素 大 大 |
C.电子排布式 违反了洪特规则 违反了洪特规则 |
D.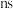 电子的能量一般低于 电子的能量一般低于 电子的能量 电子的能量 |
您最近一年使用:0次
9 . 过渡金属元素在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)原子序数为21~30的元素基态原子中,未成对电子数最多的和成对电子数最多的元素在周期表中的位置分别是______ 和______ 。
(2)基态钒原子核外电子的运动状态有_____ 种。
(3)A元素M层电子数是N电子数7倍,其价层电子轨道表示式________ 。
(4)C元素基态原子的轨道表示式是下图中的_____ (填“①”或“②”),另一轨道表示式不能作为基态原子的轨道表示式是因为它不符合_____ (填“A”“B”或“C”)。
(5)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能(设为I1)。如图所示:_____ 。
②根据图中提供的信息,可推断出I1(N)_____ I1(O)(填“>”“<”或“=”);原因是_____ 。
(1)原子序数为21~30的元素基态原子中,未成对电子数最多的和成对电子数最多的元素在周期表中的位置分别是
(2)基态钒原子核外电子的运动状态有
(3)A元素M层电子数是N电子数7倍,其价层电子轨道表示式
(4)C元素基态原子的轨道表示式是下图中的
①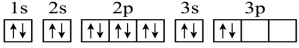
②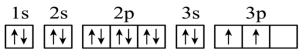
(5)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能(设为I1)。如图所示:
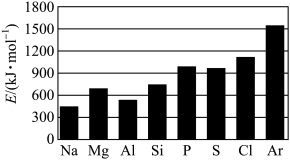
②根据图中提供的信息,可推断出I1(N)
您最近一年使用:0次
10 . 回答下列问题
(1)基态碘原子的价层电子的运动状态有_____ 种,基态Pb原子的价层电子排布式为_____ 。
(2) 价电子轨道表示式为
价电子轨道表示式为_____ ;
(3)一种磷酸硅铝分子筛常用于催化甲醇制烯烃的反应。由硅原子核形成的三种微粒: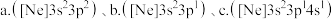 ,半径由大到小的顺序为
,半径由大到小的顺序为_____ (填标号);第三周期元素中,第一电离能介于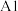 和P之间的元素有
和P之间的元素有_____ 种。
(4)下列状态的铁中,电离最外层一个电子所需能量最大的是_____ (填标号)。
 原子的价电子中,两种自旋状态的电子数之比为
原子的价电子中,两种自旋状态的电子数之比为_____ 。
(6)原子发射光谱法是通过处于激发态的待测元素微粒回到基态时发射的特征谱线对其进行鉴别的方法。下列状态的铁粒子处于激发态的是_____(填标号)。
(1)基态碘原子的价层电子的运动状态有
(2)
 价电子轨道表示式为
价电子轨道表示式为(3)一种磷酸硅铝分子筛常用于催化甲醇制烯烃的反应。由硅原子核形成的三种微粒:
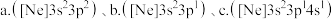 ,半径由大到小的顺序为
,半径由大到小的顺序为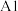 和P之间的元素有
和P之间的元素有(4)下列状态的铁中,电离最外层一个电子所需能量最大的是
a.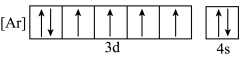
b.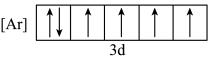
c.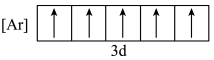
d.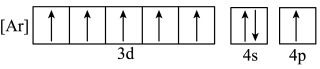
 原子的价电子中,两种自旋状态的电子数之比为
原子的价电子中,两种自旋状态的电子数之比为(6)原子发射光谱法是通过处于激发态的待测元素微粒回到基态时发射的特征谱线对其进行鉴别的方法。下列状态的铁粒子处于激发态的是_____(填标号)。
A.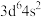 | B.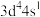 | C.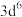 | D.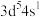 |
您最近一年使用:0次



