名校
1 . 某晶体立方晶胞如图所示。已知图中微粒1的分数坐标是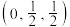 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
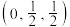 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
A. 周围距离最近且相等的 周围距离最近且相等的 个数是6 个数是6 |
B.微粒2的分数坐标是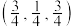 |
| C.已知银与铜位于同一族,银元素位于元素周期表的d区 |
D.若晶胞边长为a pm,则晶体密度为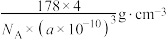 |
您最近一年使用:0次
2024-02-25更新
|
1285次组卷
|
6卷引用:湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题
湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题广西柳州高中、南宁三中名校联盟2023-2024学年高三一轮复习诊断联考化学试题(已下线)专题04 物质结构与性质 元素推断-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)选择题11-14安徽省蚌埠第二中学2023-2024学年高二下学期3月月考化学试题江西省南昌市2024届高三下学期第三次模拟测试化学试题
名校
解题方法
2 . 过渡金属配合物的一些特有性质的研究正受到许多研究人员的关注,因为这方面的研究无论是理论上还是工业应用上都有重要意义。
(1)氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示:

此配离子中含有的作用力有____ (填字母)。
A.离子键 B.金属键 C.极性键 D.非极性键 E.配位键 F.氢键 G.σ键 H.π键
(2)此配合物中碳原子的杂化轨道类型有____ 。
(3)与H2O分子互为等电子体的阴离子为____ 。
(4)下列微粒中键角按由大到小的顺序排列为____ (用序号填写)。
①CO2②SiF4③SCl2④CO ⑤H3O+
⑤H3O+
(5)氨硼烷(NH3BH3)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
①H、B、N中,原子半径最大的是____ 。根据对角线规则,B的一些化学性质与元素____ 的相似。
②氨硼烷在催化剂作用下水解释放氢气:3NH3BH3+6H2O=3NH +B3O
+B3O +9H2,B3O
+9H2,B3O 的结构如图所示;在该反应中,B原子的杂化轨道类型由
的结构如图所示;在该反应中,B原子的杂化轨道类型由____ 变为____ 。

(1)氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示:

此配离子中含有的作用力有
A.离子键 B.金属键 C.极性键 D.非极性键 E.配位键 F.氢键 G.σ键 H.π键
(2)此配合物中碳原子的杂化轨道类型有
(3)与H2O分子互为等电子体的阴离子为
(4)下列微粒中键角按由大到小的顺序排列为
①CO2②SiF4③SCl2④CO
 ⑤H3O+
⑤H3O+(5)氨硼烷(NH3BH3)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
①H、B、N中,原子半径最大的是
②氨硼烷在催化剂作用下水解释放氢气:3NH3BH3+6H2O=3NH
 +B3O
+B3O +9H2,B3O
+9H2,B3O 的结构如图所示;在该反应中,B原子的杂化轨道类型由
的结构如图所示;在该反应中,B原子的杂化轨道类型由
您最近一年使用:0次
2022-04-21更新
|
225次组卷
|
2卷引用:湖南省株洲市第二中学2021届高三下学期第三次模拟考试化学试卷
3 . 太阳能电池的发展已经进入了第三代。第一代为单晶硅太阳能电池,第二代为多晶硅、非晶硅等太阳能电池,第三代就是铜钢镓硒 (
( 中掺入
中掺入 )等化合物薄膜太阳能电池以及薄膜
)等化合物薄膜太阳能电池以及薄膜 系太阳能电池。
系太阳能电池。
(1)亚铜离子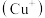 基态时的价电子排布式表示为
基态时的价电子排布式表示为___________ 。
(2)硒为第四周期元素,相邻的元素有砷和溴,则3种元素的第一电离能从大到小顺序为___________ (用元素符号表示)。
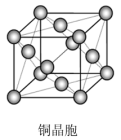
(3) 晶体的堆积方式是
晶体的堆积方式是___________ (填堆积名称),其配位数为___________ ;往 的硫酸盐溶液中加入过量氨水,可生成
的硫酸盐溶液中加入过量氨水,可生成 ,下列说法正确的是
,下列说法正确的是___________ 。
A. 中所含的化学键有离子键、极性键和配位键
中所含的化学键有离子键、极性键和配位键
B.在 中
中 给出孤电子对,
给出孤电子对, 提供空轨道
提供空轨道
C. 组成元素中第一电离能最大的是氧元素
组成元素中第一电离能最大的是氧元素
D. 与
与 互为等电子体,空间构型均为正四面体形
互为等电子体,空间构型均为正四面体形
(4)与镓元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸( )溶于水显弱酸性,但它却只是一元酸,可以用硼酸在水溶液中的电离平衡解释它只是一元弱酸的原因。
)溶于水显弱酸性,但它却只是一元酸,可以用硼酸在水溶液中的电离平衡解释它只是一元弱酸的原因。
① 中B的原子杂化类型为
中B的原子杂化类型为___________ 杂化;
②写出硼酸在水溶液中的电离方程式___________ 。
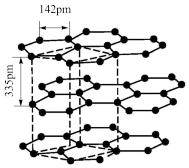
(5)硅与碳是同一主族元素,其中石墨为混合型晶体,已知石墨的层间距为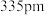 ,
, 键长为
键长为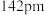 ,计算石墨晶体密度=
,计算石墨晶体密度=___________  (结果保留两位有效数字,
(结果保留两位有效数字, 为
为 )。
)。
 (
(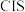 中掺入
中掺入 )等化合物薄膜太阳能电池以及薄膜
)等化合物薄膜太阳能电池以及薄膜 系太阳能电池。
系太阳能电池。(1)亚铜离子
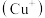 基态时的价电子排布式表示为
基态时的价电子排布式表示为(2)硒为第四周期元素,相邻的元素有砷和溴,则3种元素的第一电离能从大到小顺序为
(3)
 晶体的堆积方式是
晶体的堆积方式是 的硫酸盐溶液中加入过量氨水,可生成
的硫酸盐溶液中加入过量氨水,可生成 ,下列说法正确的是
,下列说法正确的是
A.
 中所含的化学键有离子键、极性键和配位键
中所含的化学键有离子键、极性键和配位键B.在
 中
中 给出孤电子对,
给出孤电子对, 提供空轨道
提供空轨道C.
 组成元素中第一电离能最大的是氧元素
组成元素中第一电离能最大的是氧元素D.
 与
与 互为等电子体,空间构型均为正四面体形
互为等电子体,空间构型均为正四面体形(4)与镓元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(
 )溶于水显弱酸性,但它却只是一元酸,可以用硼酸在水溶液中的电离平衡解释它只是一元弱酸的原因。
)溶于水显弱酸性,但它却只是一元酸,可以用硼酸在水溶液中的电离平衡解释它只是一元弱酸的原因。①
 中B的原子杂化类型为
中B的原子杂化类型为②写出硼酸在水溶液中的电离方程式
(5)硅与碳是同一主族元素,其中石墨为混合型晶体,已知石墨的层间距为
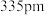 ,
, 键长为
键长为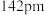 ,计算石墨晶体密度=
,计算石墨晶体密度= (结果保留两位有效数字,
(结果保留两位有效数字, 为
为 )。
)。
您最近一年使用:0次
2022-01-23更新
|
703次组卷
|
5卷引用:湖南省岳阳市2021-2022学年高三上学期质量监测化学试题
湖南省岳阳市2021-2022学年高三上学期质量监测化学试题(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-测试江西省鹰潭市2022届高三下学期第一次模拟考试理科综合化学试题四川省成都艺术高级中学2021-2022学年高三下学期模拟考试理科综合化学部分试题(三)安徽省滁州市定远县育才学校2021-2022学年高三下学期开学考试理科综合化学试题
名校
解题方法
4 . 尖晶石的主要成分是镁铝氧化物,常含有锰、铁、镍等元素,形成种类繁多的尖晶石型化合物,可研制成优质半导体光催化材料。回答下列问题:
(1)基态锰原子的价层电子排布图(轨道表示式)为___________ 。
(2)羰基锰[ ]的结构如图所示,配体为CO,则配体的电子式为
]的结构如图所示,配体为CO,则配体的电子式为___________ ,该结构中 键与
键与 键个数比为
键个数比为___________ 。

(3) 容易形成六配位的配合物,
容易形成六配位的配合物,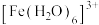 通常会水解生成棕色的
通常会水解生成棕色的 ,通过氢氧根形成双聚体
,通过氢氧根形成双聚体 ,请写出该双聚体的结构(水分子中O—H键省略,其他化学键用短横线“—”表示)
,请写出该双聚体的结构(水分子中O—H键省略,其他化学键用短横线“—”表示)___________ 。
(4)鉴定 的特征反应如下所示:
的特征反应如下所示:
Ni2++2 →
→ +2H+
+2H+
将丁二酮肟加入 溶液中,生成一种鲜红色的二丁二酮肟合镍(Ⅱ)螯合物,在该螯合物中,碳原子的杂化方式是
溶液中,生成一种鲜红色的二丁二酮肟合镍(Ⅱ)螯合物,在该螯合物中,碳原子的杂化方式是___________ ,组成该螯合物的第二周期元素第一电离能从大到小的顺序为___________ 。
(5)某镁铝尖晶石的晶胞由M区和N区组成,其结构如图所示,该化合物的化学式为___________ ,已知该晶胞参数为a pm,NA为阿伏加德罗常数的值,则该晶体的密度
___________ g/cm3 (列出计算表达式)。

(1)基态锰原子的价层电子排布图(轨道表示式)为
(2)羰基锰[
 ]的结构如图所示,配体为CO,则配体的电子式为
]的结构如图所示,配体为CO,则配体的电子式为 键与
键与 键个数比为
键个数比为
(3)
 容易形成六配位的配合物,
容易形成六配位的配合物,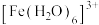 通常会水解生成棕色的
通常会水解生成棕色的 ,通过氢氧根形成双聚体
,通过氢氧根形成双聚体 ,请写出该双聚体的结构(水分子中O—H键省略,其他化学键用短横线“—”表示)
,请写出该双聚体的结构(水分子中O—H键省略,其他化学键用短横线“—”表示)(4)鉴定
 的特征反应如下所示:
的特征反应如下所示:Ni2++2
 →
→ +2H+
+2H+将丁二酮肟加入
 溶液中,生成一种鲜红色的二丁二酮肟合镍(Ⅱ)螯合物,在该螯合物中,碳原子的杂化方式是
溶液中,生成一种鲜红色的二丁二酮肟合镍(Ⅱ)螯合物,在该螯合物中,碳原子的杂化方式是(5)某镁铝尖晶石的晶胞由M区和N区组成,其结构如图所示,该化合物的化学式为


您最近一年使用:0次
2021-12-30更新
|
806次组卷
|
3卷引用:八省八校(T8联考)2021-2022学年高三上学期第一次联考化学试题(湖南师大附中)
八省八校(T8联考)2021-2022学年高三上学期第一次联考化学试题(湖南师大附中)(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-练习陕西省西安市长安区第一中学2022届高三第三次模拟考试理综化学试题
名校
解题方法
5 . 单晶硅、砷化镓、碳化硅、、等是制作半导体芯片的关键材料,也是我国优先发展的新材料.请解答如下问题:
(1)基态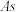 原子核外电子占据最高能级的电子云轮廓图为
原子核外电子占据最高能级的电子云轮廓图为____________ 形.
(2) 中
中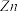 、
、 、
、 的电负性从大到小的顺序为
的电负性从大到小的顺序为____________ .
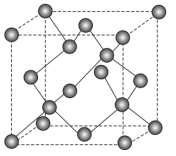
(3)硅的晶体结构是金刚石结构,如图所示.材料密度是制作芯片的重要参数之一,已知 的共价半径是
的共价半径是 ,求每立方厘米体积的单晶硅中硅的原子数目
,求每立方厘米体积的单晶硅中硅的原子数目______________ .
(4)亚砷酸 是一种三元弱酸,分子中含有羟基数目为
是一种三元弱酸,分子中含有羟基数目为_________ 个;根据价层电子对互斥理论推测的空间构型为___________ ;与 互为等电子体的两种分子分别为
互为等电子体的两种分子分别为___________ (写化学式).
(5)GaAs的熔点为1238℃,晶胞结构如图所示:
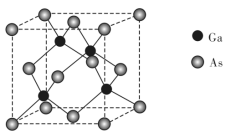
①在 晶体中,镓原子的配位数是
晶体中,镓原子的配位数是_____________ ,与同一个镓原子相连的砷原子构成的空间构型为_____________ .
②若砷化镓晶胞边长为 ,则该晶体密度为
,则该晶体密度为___________ (用含的代数式表示).
(1)基态
 原子核外电子占据最高能级的电子云轮廓图为
原子核外电子占据最高能级的电子云轮廓图为(2)
 中
中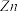 、
、 、
、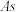 的电负性从大到小的顺序为
的电负性从大到小的顺序为(3)硅的晶体结构是金刚石结构,如图所示.材料密度是制作芯片的重要参数之一,已知
 的共价半径是
的共价半径是 ,求每立方厘米体积的单晶硅中硅的原子数目
,求每立方厘米体积的单晶硅中硅的原子数目
(4)亚砷酸
 是一种三元弱酸,分子中含有羟基数目为
是一种三元弱酸,分子中含有羟基数目为 互为等电子体的两种分子分别为
互为等电子体的两种分子分别为(5)GaAs的熔点为1238℃,晶胞结构如图所示:

①在
 晶体中,镓原子的配位数是
晶体中,镓原子的配位数是②若砷化镓晶胞边长为
 ,则该晶体密度为
,则该晶体密度为
您最近一年使用:0次
解题方法
6 . 过渡金属元素锰(Mn)是钢的一种重要添加剂,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)下列叙述正确的是_______(填标号)。
(2) 能形成配离子为八面体的配合物
能形成配离子为八面体的配合物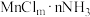 ,
, 位于八面体的中心。已知含1mol该配合物的溶液与足量
位于八面体的中心。已知含1mol该配合物的溶液与足量 ,溶液作用可生成1mol AgCl沉淀,该配离子中提供电子对形成配位键的原子是
,溶液作用可生成1mol AgCl沉淀,该配离子中提供电子对形成配位键的原子是_______ ,中心离子的配位数为_______
(3)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与 形成黄色的配合物,其结构如图所示。
形成黄色的配合物,其结构如图所示。

在锰试剂分子中,电负性最大的原子是_______ ,采取 杂化的原子是
杂化的原子是_______ ,1 mol分子中π键数目是_______ 。
(4)已知金属锰有多种晶型,a锰(体心立方)晶胞俯视图符合下列_______ (选填编号),每个Mn原子周围紧邻的原子数为_______ 。
A. B.
B. 
C.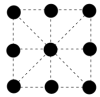 D.
D. 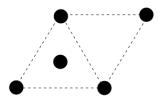
(5)硫化锰是一种重要的半导体材料,其中 具有稳定的岩盐矿结构,晶胞结构如图所示。若晶胞参数为a pm,
具有稳定的岩盐矿结构,晶胞结构如图所示。若晶胞参数为a pm, 为阿伏加德罗常数的值,晶胞的密度是
为阿伏加德罗常数的值,晶胞的密度是_______  。
。

(1)下列叙述正确的是_______(填标号)。
A.基态Mn原子电子排布式为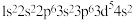 |
| B.Mn元素位于元素周期表的ds区 |
C.基态 价层电子的自旋状态相反 价层电子的自旋状态相反 |
D.第三电离能: |
 能形成配离子为八面体的配合物
能形成配离子为八面体的配合物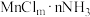 ,
, 位于八面体的中心。已知含1mol该配合物的溶液与足量
位于八面体的中心。已知含1mol该配合物的溶液与足量 ,溶液作用可生成1mol AgCl沉淀,该配离子中提供电子对形成配位键的原子是
,溶液作用可生成1mol AgCl沉淀,该配离子中提供电子对形成配位键的原子是(3)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与
 形成黄色的配合物,其结构如图所示。
形成黄色的配合物,其结构如图所示。
在锰试剂分子中,电负性最大的原子是
 杂化的原子是
杂化的原子是(4)已知金属锰有多种晶型,a锰(体心立方)晶胞俯视图符合下列
A.
 B.
B. 
C.
 D.
D. 
(5)硫化锰是一种重要的半导体材料,其中
 具有稳定的岩盐矿结构,晶胞结构如图所示。若晶胞参数为a pm,
具有稳定的岩盐矿结构,晶胞结构如图所示。若晶胞参数为a pm, 为阿伏加德罗常数的值,晶胞的密度是
为阿伏加德罗常数的值,晶胞的密度是 。
。
您最近一年使用:0次
解题方法
7 . 回答下列问题:
(1)我国自主研发的DF—31A洲际战略导弹是我国大国地位、国防实力的显著标志,其材料中包含了Fe、Cr、Ni、C等多种元素。
①基态镍原子的价电子排布式为__ 。
②Cr与K位于同一周期且最外层电子数相同,两种元素原子第一电离能的大小关系为K___ (填“>”或“<”)Cr;
③SCN-常用于检验Fe3+,其对应酸有硫氰酸(H—S—C≡N)和异硫氰酸(H—N=C=S)两种。硫氰酸分子中σ键与π键的数目比为___ ,异硫氰酸沸点较高的原因是__ 。
(2)大连理工大学彭孝军院士课题组报道了基于硼氟荧类荧光染料(BODIPY)的铜荧光探针的设计与应用,利用Cu2+诱导胺的氧化脱氢反应形成的Cu+配合物,进行Hela细胞中的Cu2+荧光成像和检测。其反应如图所示:
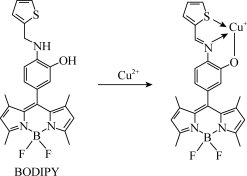
在水溶液里,Cu2+比Cu+稳定,是由于水分子配体的作用。在气态时,Cu2+比Cu+活泼的原因是____ ;BODIPY荧光探针分子中,1molBODIPY分子中含有__ mol配位键。
(3)六方石墨和三方石墨都是由石墨层形分子平行堆积而形成的晶体。已知六方石墨晶体由层状石墨“分子”按ABAB…方式堆积而成,如图甲所示,一个石墨的六方晶胞如图乙所示。而三方石墨层形分子堆积的次序为ABCABC
 ,一个三方石墨晶胞如图丙所示。
,一个三方石墨晶胞如图丙所示。
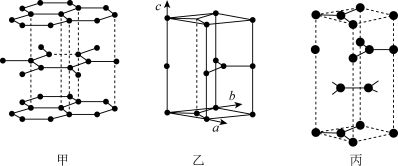
画出六方石墨晶胞沿c轴的投影:__ (用“·”标出碳原子位置即可),已知一个三方石墨晶胞的体积为Vpm3,则该晶胞的密度为__ g/cm3。(用含NA和V的代数式表示)
(1)我国自主研发的DF—31A洲际战略导弹是我国大国地位、国防实力的显著标志,其材料中包含了Fe、Cr、Ni、C等多种元素。
①基态镍原子的价电子排布式为
②Cr与K位于同一周期且最外层电子数相同,两种元素原子第一电离能的大小关系为K
③SCN-常用于检验Fe3+,其对应酸有硫氰酸(H—S—C≡N)和异硫氰酸(H—N=C=S)两种。硫氰酸分子中σ键与π键的数目比为
(2)大连理工大学彭孝军院士课题组报道了基于硼氟荧类荧光染料(BODIPY)的铜荧光探针的设计与应用,利用Cu2+诱导胺的氧化脱氢反应形成的Cu+配合物,进行Hela细胞中的Cu2+荧光成像和检测。其反应如图所示:

在水溶液里,Cu2+比Cu+稳定,是由于水分子配体的作用。在气态时,Cu2+比Cu+活泼的原因是
(3)六方石墨和三方石墨都是由石墨层形分子平行堆积而形成的晶体。已知六方石墨晶体由层状石墨“分子”按ABAB…方式堆积而成,如图甲所示,一个石墨的六方晶胞如图乙所示。而三方石墨层形分子堆积的次序为ABCABC

 ,一个三方石墨晶胞如图丙所示。
,一个三方石墨晶胞如图丙所示。
画出六方石墨晶胞沿c轴的投影:
您最近一年使用:0次
名校
解题方法
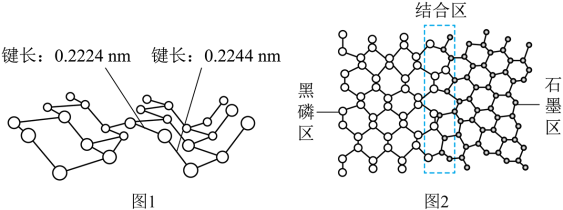
8 . 磷及其化合物在电池、催化等领域有重要应用。黑磷与石墨类似,也具有层状结构(图1)。 为大幅度提高锂电池的充电速率,科学家最近研发了黑磷-石墨复合负极材料,其单层结构俯视图如图2所示。
回答下列问题:
(1)Li、C、P三种元素中,电负性最小的是_________________ (用元素符号作答)。
(2)基态磷原子价电子排布式为________________ 。
(3)图2黑磷区中P原子的杂化方式为_________________ ,石墨区中C原子的杂化方式为____________ 。
(4)氢化物PH3、CH4、NH3的沸点由高到低顺序为________________ 。
(5)根据图1和图2的信息,下列说法正确的有________ (填字母)。
A. 黑磷区中P-P键的键能不完全相同
B. 黑磷与石墨都属于混合型晶体
C. 由石墨与黑磷制备该复合材料的过程,发生了化学反应
D. 石墨与黑磷的交界结合区域中,P原子与C原子共平面
E. 复合材料单层中,P原子与C原子之间的作用力属范德华力
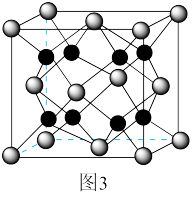
(6)贵金属磷化物Rh2P (化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图3所示。已知晶胞参数为anm,晶体中与P距离最近的Rh的数目为___________________ , 晶体的密度为__________ g·cm-3(列出计算式)。

回答下列问题:
(1)Li、C、P三种元素中,电负性最小的是
(2)基态磷原子价电子排布式为
(3)图2黑磷区中P原子的杂化方式为
(4)氢化物PH3、CH4、NH3的沸点由高到低顺序为
(5)根据图1和图2的信息,下列说法正确的有
A. 黑磷区中P-P键的键能不完全相同
B. 黑磷与石墨都属于混合型晶体
C. 由石墨与黑磷制备该复合材料的过程,发生了化学反应
D. 石墨与黑磷的交界结合区域中,P原子与C原子共平面
E. 复合材料单层中,P原子与C原子之间的作用力属范德华力
(6)贵金属磷化物Rh2P (化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图3所示。已知晶胞参数为anm,晶体中与P距离最近的Rh的数目为

您最近一年使用:0次
2021-05-28更新
|
735次组卷
|
9卷引用:湖南省长沙市第一中学2021-2022学年高三上学期月考化学试题
湖南省长沙市第一中学2021-2022学年高三上学期月考化学试题广东省2021年普通高中学业水平选择考适应性测试化学试题(已下线)难点10 物质结构与性质综合题-2021年高考化学【热点·重点·难点】专练(新高考)河北省石家庄市第二十四中学2020-2021学年高二第二学期期中考试化学试题湖南省株洲市攸县第一中学2022届高三下学期四月月考化学试题(已下线)3.3.2 过渡晶体和混合型晶体-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)广东省深圳外国语学校2021-2022学年下学期高三第二次检测考试化学试题(已下线)专题19 物质结构与性质-2022年高考化学二轮复习重点专题常考点突破练广东省惠州市惠州中学2022-2023学年高二下学期化学考试题
9 . 二氧化碳化学资源化利用已经显示出越来越重要的科技与经济价值,如用铜锌氧化物催化二氧化碳加氢生成 ,合成碳酸乙烯酯(EC)等。回答下列问题:
,合成碳酸乙烯酯(EC)等。回答下列问题:
(1)基态铜原子价电子排布式为___________ ;第一电离能 的原因是
的原因是___________ 。
(2) 的空间构型为
的空间构型为___________ 。
(3)EC的结构简式为 ,其碳原子杂化方式为
,其碳原子杂化方式为___________ ,每个分子中含___________ 个 键。
键。
(4) 加氢得到
加氢得到 ,
, 的沸点比
的沸点比 的高,原因是
的高,原因是___________ 。
(5)高温时,太阳能反应器中的 失去部分氧,温度稍低时,从
失去部分氧,温度稍低时,从 中重新夺取氧。一种铈(Ce)的氧化物的晶胞结构如图所示:
中重新夺取氧。一种铈(Ce)的氧化物的晶胞结构如图所示:

①Ce的配位数为___________ 。
②若高温下该晶胞中1个氧原子变为空位,___________ 个面心上的铈由+4价变为+3价(不考虑顶点)。
③已知 的密度为7.13g/cm3,设NA为阿伏加德罗常数的值,则晶胞边长a=
的密度为7.13g/cm3,设NA为阿伏加德罗常数的值,则晶胞边长a=___________ pm。
 ,合成碳酸乙烯酯(EC)等。回答下列问题:
,合成碳酸乙烯酯(EC)等。回答下列问题:(1)基态铜原子价电子排布式为
 的原因是
的原因是(2)
 的空间构型为
的空间构型为(3)EC的结构简式为
 ,其碳原子杂化方式为
,其碳原子杂化方式为 键。
键。(4)
 加氢得到
加氢得到 ,
, 的沸点比
的沸点比 的高,原因是
的高,原因是(5)高温时,太阳能反应器中的
 失去部分氧,温度稍低时,从
失去部分氧,温度稍低时,从 中重新夺取氧。一种铈(Ce)的氧化物的晶胞结构如图所示:
中重新夺取氧。一种铈(Ce)的氧化物的晶胞结构如图所示:
①Ce的配位数为
②若高温下该晶胞中1个氧原子变为空位,
③已知
 的密度为7.13g/cm3,设NA为阿伏加德罗常数的值,则晶胞边长a=
的密度为7.13g/cm3,设NA为阿伏加德罗常数的值,则晶胞边长a=
您最近一年使用:0次
2021-05-20更新
|
360次组卷
|
3卷引用:湖南省永州市省重点中学2021届高三5月联考化学试题
解题方法
10 . 在庆祝中华人民共和国成立70周年的阅兵仪式上,最后亮相的 洲际战略导弹是我国大国地位、国防实力的显著标志。其制作材料中包含了
洲际战略导弹是我国大国地位、国防实力的显著标志。其制作材料中包含了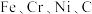 等多种元素。请回答:
等多种元素。请回答:
(1)基态铁原子的价电子排布式为____ , 的熔点为
的熔点为 ,沸点为
,沸点为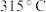 ,
, 的晶体类型是
的晶体类型是__ 。
(2)氧化亚铁晶体的晶胞如图所示。已知:氧化亚铁晶体的密度为 代表阿伏加德罗常数的值。在该晶胞中,与
代表阿伏加德罗常数的值。在该晶胞中,与 紧邻且等距离的
紧邻且等距离的 数目为
数目为____ ; 与
与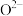 最短核间距为
最短核间距为___  。
。

(3)硫酸镍溶于氨水形成 蓝色溶液。
蓝色溶液。
① 中阴离子的立体构型是
中阴离子的立体构型是___ ;
②在 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为_ ,提供孤电子对的成键原子是_ 。
(4)无水 和氨分子作用能形成某种配合物,该配合物的组成相当于
和氨分子作用能形成某种配合物,该配合物的组成相当于 。已知:若加入
。已知:若加入 溶液,能从该配合物的水溶液中将所有的氯沉淀为AgCl;若加入
溶液,能从该配合物的水溶液中将所有的氯沉淀为AgCl;若加入 溶液并加热,无刺激性气体产生。请从配合物的形式推算出它的内界和外界,写出该配合物的结构式
溶液并加热,无刺激性气体产生。请从配合物的形式推算出它的内界和外界,写出该配合物的结构式___ , 该配合物中含有σ键的数目为
该配合物中含有σ键的数目为____ 。
 洲际战略导弹是我国大国地位、国防实力的显著标志。其制作材料中包含了
洲际战略导弹是我国大国地位、国防实力的显著标志。其制作材料中包含了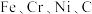 等多种元素。请回答:
等多种元素。请回答:(1)基态铁原子的价电子排布式为
 的熔点为
的熔点为 ,沸点为
,沸点为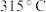 ,
, 的晶体类型是
的晶体类型是(2)氧化亚铁晶体的晶胞如图所示。已知:氧化亚铁晶体的密度为
 代表阿伏加德罗常数的值。在该晶胞中,与
代表阿伏加德罗常数的值。在该晶胞中,与 紧邻且等距离的
紧邻且等距离的 数目为
数目为 与
与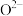 最短核间距为
最短核间距为 。
。
(3)硫酸镍溶于氨水形成
 蓝色溶液。
蓝色溶液。①
 中阴离子的立体构型是
中阴离子的立体构型是②在
 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为(4)无水
 和氨分子作用能形成某种配合物,该配合物的组成相当于
和氨分子作用能形成某种配合物,该配合物的组成相当于 。已知:若加入
。已知:若加入 溶液,能从该配合物的水溶液中将所有的氯沉淀为AgCl;若加入
溶液,能从该配合物的水溶液中将所有的氯沉淀为AgCl;若加入 溶液并加热,无刺激性气体产生。请从配合物的形式推算出它的内界和外界,写出该配合物的结构式
溶液并加热,无刺激性气体产生。请从配合物的形式推算出它的内界和外界,写出该配合物的结构式 该配合物中含有σ键的数目为
该配合物中含有σ键的数目为
您最近一年使用:0次
2021-03-28更新
|
375次组卷
|
3卷引用:湖南省郴州市2021届高三3月第三次教学质量监测化学试题
湖南省郴州市2021届高三3月第三次教学质量监测化学试题湖南省邵阳市2021届高三第一次模拟测试化学试题(已下线)2021年高考化学押题预测卷(山东卷)(01)(含考试版、答题卡、参考答案、全解全析)



