名校
1 . A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是
| A.A B C D E | B.E C D B A | C.E C D B A | D.C D A B E |
您最近一年使用:0次
2 . 下表是元素周期表的一部分:
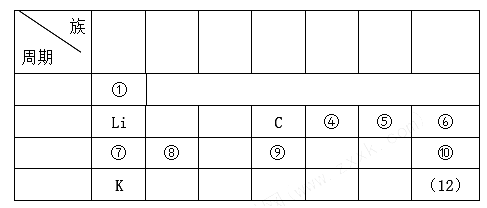
(1)表中元素______ 的非金属性最强(填写元素符号,下同);元素______ 的单质室温下呈液态,它的原子序数是_________ 。
(2)表中元素⑤和⑦、①和⑤均可以组成原子比例为1:1的物质,这两种物质内所含有相同的化学键是__________ (填写“离子键”、“极性共价键”或“非极性共价键”)。
(3)表中元素⑥⑩(12)氢化物的稳定性由大到小的顺序为:_________ (填写化学式,下同)。
(4)表中有一种元素的单质可作为半导体材料,它在元素周期表中的位置是_____ 。
(5)用电子式表示表中⑧⑩两元素形成化合物的过程__________________ 。

(1)表中元素
(2)表中元素⑤和⑦、①和⑤均可以组成原子比例为1:1的物质,这两种物质内所含有相同的化学键是
(3)表中元素⑥⑩(12)氢化物的稳定性由大到小的顺序为:
(4)表中有一种元素的单质可作为半导体材料,它在元素周期表中的位置是
(5)用电子式表示表中⑧⑩两元素形成化合物的过程
您最近一年使用:0次
3 . 下图是部分短周期元素的常见化合价与原子序数的关系:
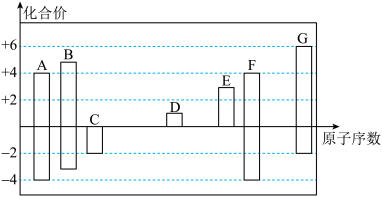
(1)元素A在周期表中的位置____________ 。C2﹣、D+、G2﹣离子半径大小顺序是____________ (填离子符号)。
(2)用电子式表示D2G的形成过程________________________ 。
(3)C、G的氢化物中沸点较低的是____________ (填化学式)。
(4)C与D形成的具有强氧化性的化合物的电子式为____________ 。

(1)元素A在周期表中的位置
(2)用电子式表示D2G的形成过程
(3)C、G的氢化物中沸点较低的是
(4)C与D形成的具有强氧化性的化合物的电子式为
您最近一年使用:0次
名校
4 .
铁和钴是重要的过渡元素。
(l)钴位于元素周期表中第_____ 族,其基态原子中未成对电子的个数为______ .
(2)[Fe(H2NCONH2)6](NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中中心离子Fe3+的核外价电子排布式为___________ ;尿素分子中N原子的杂化方式是_____ ,所含非金属元素的电负性由大到小的顺序是___________ 。
(3)Co(NH3)5BrSO4可形成两种结构的钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:
在第一种配合物溶液中加硝酸银溶液产生白色沉淀.
在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀,则第二种配合物的配体为_______ 。
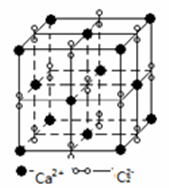
(4)离子化合物CaC2的一种晶体结构如图。从钙离子看,属于_____ 堆积,其配位数是_____ ;一个晶胞含有的σ键平均有______ 个。
(5)科学研究结果表明.碳的氧化物CO2能够与H2O借助于太阳能制备HCOOH。其反应原理如下:2CO2+2H2O=2HCOOH+O2,则生成的HCOOH分子中σ键和π键的个数比是______ .
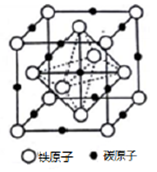
(6)奥氏体是碳溶解在γ—Fe中形成的一种间隙固溶体,无磁性,其晶胞如右图所示,则该物质的化学式为________ ,若晶体密度为dg/cm3,则晶胞中最近的两个碳原子的距离为____ pm。(阿伏伽德罗常数的值用NA表示,写出简化后的计算式即可)。
铁和钴是重要的过渡元素。
(l)钴位于元素周期表中第
(2)[Fe(H2NCONH2)6](NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中中心离子Fe3+的核外价电子排布式为
(3)Co(NH3)5BrSO4可形成两种结构的钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:
在第一种配合物溶液中加硝酸银溶液产生白色沉淀.
在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀,则第二种配合物的配体为
(4)离子化合物CaC2的一种晶体结构如图。从钙离子看,属于
(5)科学研究结果表明.碳的氧化物CO2能够与H2O借助于太阳能制备HCOOH。其反应原理如下:2CO2+2H2O=2HCOOH+O2,则生成的HCOOH分子中σ键和π键的个数比是
(6)奥氏体是碳溶解在γ—Fe中形成的一种间隙固溶体,无磁性,其晶胞如右图所示,则该物质的化学式为
您最近一年使用:0次
名校
解题方法
5 . 短周期元素Q、R、T、W在周期表中的位置如图所示,其中,T所处周期序数与主族序数相等,则下列说法正确的是

| A.元素R的最高价氧化物对应的水化物是高沸点酸 |
| B.元素T和W各自形成的简单离子都能促进水的电离 |
| C.简单离子半径:W>T>R |
| D.常温下,T的单质能完全溶于R的最高价氧化物的水化物的浓溶液中 |
您最近一年使用:0次
2017-05-27更新
|
538次组卷
|
2卷引用:宁夏石嘴山市第三中学2017届高三下学期第四次模拟考试理综化学试题
6 . W、X、Y、Z为原子序数依次增大的短周期主族元素,W的原子核外只有6个电子,X+和Y3+的电子层结构相同,Z-的电子数比Y3+多8个,下列叙述正确的是
| A.W在自然界只有一种核素 | B.半径大小:X+>Y3+>Z- |
| C.Y与Z形成的化合物的水溶液呈弱酸性 | D.X的最高价氧化物对应的水化物为弱碱 |
您最近一年使用:0次
2017-05-25更新
|
1002次组卷
|
4卷引用:福建省宁德市2017届高三毕业班第三次质量检查化学试题
名校
7 . X、Y、Z、M、W、N六种元素的原子序数依次增大,其中X、Y、Z、M、W为五种短周期元素。X元素的某种核素无中子,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示,N是用量最多的金属元素。下列说法不正确 的是
| Y | Z | M | ||
| W |
| A.原子半径:W>Y>Z>M>X |
| B.N的一种氧化物可用作油漆和涂料 |
| C.氢化物的沸点:Z小于M |
| D.工业上制备W单质的方法为电解熔融的W的氧化物 |
您最近一年使用:0次
2017-05-25更新
|
1560次组卷
|
4卷引用:辽宁省鞍山市第一中学2017届高三下学期最后一次模拟考试理科综合化学试题
辽宁省鞍山市第一中学2017届高三下学期最后一次模拟考试理科综合化学试题【全国百强校】云南省曲靖市第一中学2018-2019学年高一下学期期中考试化学试题辽宁省实验中学东戴河分校2019-2020学年高二12月月考化学试题(已下线)专题16 元素周期律和元素周期表(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练
名校
8 . 中学常见的短周期主族元素R、X、Y、Z、M的原子序数依次增大,它们占据三个周期。Y和M位于同主族,Y原子最外层电子数是电子层数的3倍。这五种元素组成一种离子化合物Q。取一定量Q溶于蒸馏水得到溶液,向溶液中滴加稀氢氧化钠溶液,产生沉淀与氢氧化钠溶液体积如图所示。下列说法不正确的是
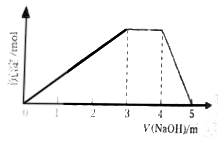
| A.简单的离子半径:M>Y>Z |
| B.气态氢化物的热稳定性:Y>X |
| C.由R、X、Y、M四种元素只组成一种盐 |
| D.最高价氧化物对应水化物的酸性:M>Z |
您最近一年使用:0次
2017-05-25更新
|
607次组卷
|
3卷引用:广东省汕头市2017届高三第三次模拟考试理科综合化学试题
名校
9 . 2017年1月26日,美国《科学》杂志刊发论文称发现了一种新材料——金属氢,证实了一百多年前提出的存在金属氢的假说。下列事实不能说明氢可能具有金属性的是
| A.可以把H写入金属活动性顺序表 | B.H与Na、K等碱金属元素同属于第IA族 |
| C.H存在H- | D.H与非金属反应,产物中H通常显正价 |
您最近一年使用:0次
2017-05-24更新
|
626次组卷
|
2卷引用:河北省石家庄市第二中学2017届高三5月联考理科综合化学试题
名校
10 . 下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素的元素符号:① ______ ,⑥______ ,⑦ _______ ,⑨______ 。
(2)画出下列微粒的结构示意图:④的原子:____________ ,⑧的离子:___________ 。
(3)表中的12种元素中,金属性最强的元素是________ ,非金属性最强的元素是_________ ,最不活泼的元素是_______ 。(均填元素符号)
(4)③④⑤⑦⑧五种元素中,离子半径最大的元素是______ (填元素符号)。元素③和⑦可以形成 _____________ (填“离子”或“共价”)化合物。
(5)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子方程式____________ 。
族 周期 | IA | IIA | IIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)画出下列微粒的结构示意图:④的原子:
(3)表中的12种元素中,金属性最强的元素是
(4)③④⑤⑦⑧五种元素中,离子半径最大的元素是
(5)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子方程式
您最近一年使用:0次



