名校
1 . 航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料。
(1)写出高氯酸铵组成元素中,原子核外有三层电子的原子的结构示意图___________ 。
(2)高氯酸铵对应酸高氯酸HClO4的酸酐是___________ 。
(3)150℃时高氯酸铵发生分解反应:2NH4ClO4=N2↑+Cl2↑+2O2↑+4H2O↑,其气态生成物组成的混合气的平均相对分子质量为___________ 。
(1)写出高氯酸铵组成元素中,原子核外有三层电子的原子的结构示意图
(2)高氯酸铵对应酸高氯酸HClO4的酸酐是
(3)150℃时高氯酸铵发生分解反应:2NH4ClO4=N2↑+Cl2↑+2O2↑+4H2O↑,其气态生成物组成的混合气的平均相对分子质量为
您最近一年使用:0次
名校
2 . 肼(N2H4)是重要的化工原料,能与水、乙醇等混溶;它是一种二元弱碱,在水中的电离方式与氨相似,室温下电离常数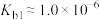 ;在碱性溶液中,N2H4是强还原剂。
;在碱性溶液中,N2H4是强还原剂。
(1)写出N元素在元素周期表中的位置___________ 。
(2)写出N2H4与过量硫酸反应形成的酸式盐的化学式___________ 。
(3)N2H4可通过NH3和NaClO反应制得,总反应主要分为两步,
已知第一步: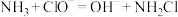
①写出第二步反应的离子方程式___________ 。
②请设计实验,检验总反应中产物的主要阴离子(假设反应物完全反应)___________ 。
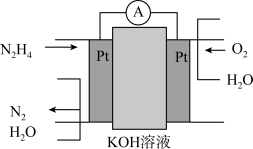
(4)N2H4是一种高能燃料,可用于燃料电池,原理如图,电池的负极反应式为___________ 。
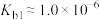 ;在碱性溶液中,N2H4是强还原剂。
;在碱性溶液中,N2H4是强还原剂。(1)写出N元素在元素周期表中的位置
(2)写出N2H4与过量硫酸反应形成的酸式盐的化学式
(3)N2H4可通过NH3和NaClO反应制得,总反应主要分为两步,
已知第一步:
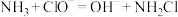
①写出第二步反应的离子方程式
②请设计实验,检验总反应中产物的主要阴离子(假设反应物完全反应)
(4)N2H4是一种高能燃料,可用于燃料电池,原理如图,电池的负极反应式为

您最近一年使用:0次
解题方法
3 . 如表为元素周期表中的一部分,请回答下列问题:
(1)写出⑤元素的名称_______ 。
(2)写出③元素的离子结构示意图_______ 。
(3)④单质与水发生反应的离子方程式_______ 。
(4)写出⑥元素在周期表中的位置_______ 。
(5)比较单质氧化性的强弱⑤_______ ⑦(填”>”、”<”或”=”)。
| 项目 | I A | II A | III A | IV A | V A | VI A | VII A |
| 二 | ① | ② | ③ | ||||
| 三 | ④ | ⑤ | |||||
| 四 | ⑥ | ⑦ |
(1)写出⑤元素的名称
(2)写出③元素的离子结构示意图
(3)④单质与水发生反应的离子方程式
(4)写出⑥元素在周期表中的位置
(5)比较单质氧化性的强弱⑤
您最近一年使用:0次
名校
解题方法
4 . 金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)基态Na原子的原子结构示意图表示式为___________ ,在周期表中的位置是___________ 。
(2)Na2O2的电子式为___________ 。Na2O2可作供氧剂,写出Na2O2与CO2反应的化学方程式___________ 。若有1molNa2O2参加反应则转移电子的物质的量为___________ mol。
(3)采用空气和Na为原料可直接制备Na2O2。空气与熔融金属Na反应前需依次通过___________ 、___________ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(4)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应: ___________MnO +___________H++___________Na2O2=___________Mn2++___________O2↑+___________H2O+___________Na+,配平该离子方程式
+___________H++___________Na2O2=___________Mn2++___________O2↑+___________H2O+___________Na+,配平该离子方程式_________ ;该反应说明Na2O2具有___________ 性(选填“氧化”,“还原”或“漂白”)。
(5)天然碱的主要成分为Na2CO3·NaHCO3·2H2O,1molNa2CO3·NaHCO3·2H2O经充分加热得到Na2CO3的质量为___________ g。
(1)基态Na原子的原子结构示意图表示式为
(2)Na2O2的电子式为
(3)采用空气和Na为原料可直接制备Na2O2。空气与熔融金属Na反应前需依次通过
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(4)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应: ___________MnO
 +___________H++___________Na2O2=___________Mn2++___________O2↑+___________H2O+___________Na+,配平该离子方程式
+___________H++___________Na2O2=___________Mn2++___________O2↑+___________H2O+___________Na+,配平该离子方程式(5)天然碱的主要成分为Na2CO3·NaHCO3·2H2O,1molNa2CO3·NaHCO3·2H2O经充分加热得到Na2CO3的质量为
您最近一年使用:0次
2023-12-02更新
|
199次组卷
|
2卷引用:黑龙江省哈尔滨市第三十二中学校2023-2024学年高三上学期11月期中考试化学试题
5 . 下面是元素周期表的一部分,表中的每个字母表示一种短周期元素,请回答下列问题:
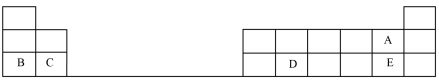
(1)D在元素周期表中的位置是第三周期___________ 族。
(2)A、E两种元素所形成的气态氢化物较稳定的是___________ (填化学式)。
(3)B、C两元素的原子半径较小的是___________ (填元素符号)。
(4)在盛有水的小烧杯中加入元素B的单质,发生反应的化学方程式为:___________ 。
(5)非金属性最强的元素是___________ (元素符号)。

(1)D在元素周期表中的位置是第三周期
(2)A、E两种元素所形成的气态氢化物较稳定的是
(3)B、C两元素的原子半径较小的是
(4)在盛有水的小烧杯中加入元素B的单质,发生反应的化学方程式为:
(5)非金属性最强的元素是
您最近一年使用:0次
6 . 按要求填空。
(1)已知A原子,其核外电子数为17,则A是_______ (填元素符号)。
(2)已知B原子,L层上的电子数为K层的3倍,则其原子结构示意图是_______ 。
(3)已知C原子,其最外层电子数等于次外层电子数的2倍,则C的元素名称是_______ 。
(4)某元素D的原子得到2个电子后,电子层排布与氖原子相同的,写出该元素的离子结构示意图_______ 。
(1)已知A原子,其核外电子数为17,则A是
(2)已知B原子,L层上的电子数为K层的3倍,则其原子结构示意图是
(3)已知C原子,其最外层电子数等于次外层电子数的2倍,则C的元素名称是
(4)某元素D的原子得到2个电子后,电子层排布与氖原子相同的,写出该元素的离子结构示意图
您最近一年使用:0次
名校
解题方法
7 . 硫元素在周期表中的位置是___________ ;基态硫原子价电子轨道表示式:___________ 。
您最近一年使用:0次
名校
解题方法
8 . 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
(1)②的最高价氧化物的分子式为_______ ;⑦的最高价氧化物对应水化物的分子式为_______ 。
(2)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:_______ 。
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是_______(填字母)。
(4)已知Cs元素位于元素周期表中第六周期第IA族,请回答下列问题:
①铯的原子序数为_______ 。
②铯单质与 反应的化学反应方程式为
反应的化学反应方程式为_______ 。
③预测铯单质的还原性比钠单质的还原性_______ (填“弱”或“强”)。
④下列推断正确的是_______ (填字母)。
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为_______ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是_______(填字母)。
| A.在化合物中最高正化合价为+6 | B.单质可以与 气体反应并置换出单质S 气体反应并置换出单质S |
| C.最高价氧化物对应水化物的酸性比硫酸弱 | D.单质在常温下可与氢气化合 |
①铯的原子序数为
②铯单质与
 反应的化学反应方程式为
反应的化学反应方程式为③预测铯单质的还原性比钠单质的还原性
④下列推断正确的是
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
2023-11-10更新
|
895次组卷
|
2卷引用:广西柳州铁一中学2022-2023学年高一上学期期末考试化学试题
名校
9 . 如图是氟元素在元素周期表中的信息及原子结构示意图,回答下列问题:
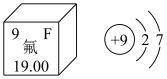
(1)图中“19.00”代表___________ ,请写出氟原子最外层的轨道表示式:___________ 。其最外层有___________ 种运动状态不同的电子,能量最高的能级的原子轨道的形状___________ 。
(2)氟气非常活泼,易与金属和某些非金属反应生成不同的化合物,如 、
、 ,请写出
,请写出 的电子式
的电子式___________ , 中的化学键类型为
中的化学键类型为___________ ; 是
是___________ 化合物, 是10电子微粒,请再写出两个10电子微粒
是10电子微粒,请再写出两个10电子微粒___________ 。

(1)图中“19.00”代表
(2)氟气非常活泼,易与金属和某些非金属反应生成不同的化合物,如
 、
、 ,请写出
,请写出 的电子式
的电子式 中的化学键类型为
中的化学键类型为 是
是 是10电子微粒,请再写出两个10电子微粒
是10电子微粒,请再写出两个10电子微粒
您最近一年使用:0次
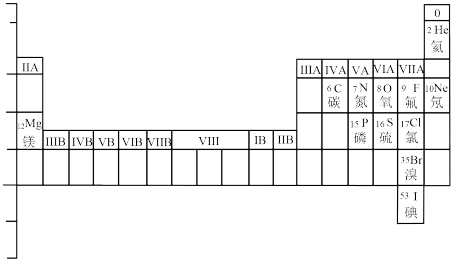
10 . 请仿照表中已有元素的呈现方式补全下表_____ 。

您最近一年使用:0次



