名校
1 . 一些元素在周期表中的分布情况如图:___________ 。
(2)Na、Cl、K元素对应的简单离子半径由小到大的顺序___________ (用离子符号表示)。
(3)Sn的价电子数为___________ 。
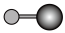
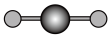
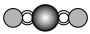
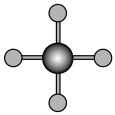
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是___________(填字母)。
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________。
(6)用电子式表示 的形成过程
的形成过程___________ 。
(7)在下列物质中:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦Ar⑧
⑦Ar⑧ (用物质前序号填空)。其中既存在极性键又存在非极性键的是
(用物质前序号填空)。其中既存在极性键又存在非极性键的是___________ ;既存在离子键又存在极性键的是___________ 。
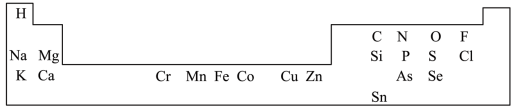
(2)Na、Cl、K元素对应的简单离子半径由小到大的顺序
(3)Sn的价电子数为
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是___________(填字母)。
| A | B | C | D |
 |  |  |  |
|
|
|
|
| 直线形 | 直线形 | 直线形 | 平面正方形 |
| A.A | B.B | C.C | D.D |
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________。
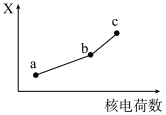
| A.若a、b、c表示ⅠA族金属元素,则X表示对应单质的密度 |
| B.若a、b、c表示ⅦA族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示ⅥA族元素,则X表示对应氢化物的稳定性 |
| D.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
(6)用电子式表示
 的形成过程
的形成过程(7)在下列物质中:①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦Ar⑧
⑦Ar⑧ (用物质前序号填空)。其中既存在极性键又存在非极性键的是
(用物质前序号填空)。其中既存在极性键又存在非极性键的是
您最近一年使用:0次
2 . 下表为元素周期表的一部分。
(1)表中元素________ 的非金属性最强;元素________ 的金属性最强;元素________ 的单质在室温下呈液态;(写元素符号)。
(2)表中半径最大的元素是_______ ;(写元素符号)
(3)表中元素⑤、⑥、⑦对应的单质氧化性最强的是_______ ;(写化学式,下同)
(4)表中元素⑥、⑦氢化物的稳定性顺序为________ >________ ;
(5)表中元素最高价氧化物对应水化物酸性最强的酸是_________________ 。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | ||||||
| 二 | ② | ⑤ | |||||
| 三 | ③ | ⑥ | |||||
| 四 | ④ | ⑦ | |||||
(1)表中元素
(2)表中半径最大的元素是
(3)表中元素⑤、⑥、⑦对应的单质氧化性最强的是
(4)表中元素⑥、⑦氢化物的稳定性顺序为
(5)表中元素最高价氧化物对应水化物酸性最强的酸是
您最近一年使用:0次
3 . 在元素周期表中,氧、硫、硒、碲4种元素属于第ⅥA族元素(又称氧族元素),请回答下列问题。
(1)查阅资料,填写下表中的空白_______ 。
(2)根据上表中的数据,找出氧、硫、硒、碲的熔点、沸点和密度的变化规律_____ 。
(3)若要研究氧、硫、硒、碲4种元素非金属性强弱的变化规律,你认为可从哪些方面入手_____ ?
(1)查阅资料,填写下表中的空白
| 元素名称 | 元素符号 | 核电荷数 | 原子结构示意图 | 单质 | 氢化物 | 氧化物的化学式 | 氧化物的水化物的化学式 | ||||
| 熔点 ℃ | 沸点 ℃ | 密度 (g·cm-3) | 化学式 | 化和条件 | 稳定性变化规律 | ||||||
| 氧 | O | 8 |  | 点燃 | — | — | |||||
| 硫 | S | 16 | 加热 |   | |||||||
| 硒 | Se | 34 | 217 | 684.9 | 4.81 | 加热 | |||||
| 碲 | Te | 52 | 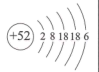 | 452 | 1390 | 6.25 | 不直接化合 | ||||
(3)若要研究氧、硫、硒、碲4种元素非金属性强弱的变化规律,你认为可从哪些方面入手
您最近一年使用:0次
4 . 下表是元素周期表的一部分。表中所列字母分别代表一种元素。
回答下列问题:
(1)j在元素周期表中的位置是______ 。
(2)e、h、m形成的简单离子其半径由大到小的顺序为________ 。(填写离子符号)
(3)n与g形成的化合物为______ (填写化学式,下同),将该化合物进行焰色反应,火焰呈______ 色。
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为______ 。
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为______ 。
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg_____ Al(选填“>”或“<”);
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律对上述实验结论进行解释______ 。
| a | b | |||||||
| c | d | e | f | |||||
| g | h | i | j | k | l | m | ||
| n |
(1)j在元素周期表中的位置是
(2)e、h、m形成的简单离子其半径由大到小的顺序为
(3)n与g形成的化合物为
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律对上述实验结论进行解释
您最近一年使用:0次
2022-01-14更新
|
785次组卷
|
4卷引用:湖南省怀化市2021-2022学年高一上学期期末考试化学试题
湖南省怀化市2021-2022学年高一上学期期末考试化学试题(已下线)第四章 物质结构 元素周期律(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)湖北省孝感市新高考联考协作体2022-2023学年高二上学期9月联考化学试题(已下线)【2023】【高一下】【其他】【杭高卷四-期中复习卷】【高中化学】【刘尼尼收集】
解题方法
5 . 下表是元素周期表的一部分,表中的每个编号代表一种短周期元素,回答下列问题:
(1)①和③两种元素形成化合物的电子式为___________ 。
(2)④、⑤、⑥三种元素的最高价氧化物对应水化物的碱性由强到弱的顺序为___________ (用化学式表示)。
(3)①和⑧两种元素按原子个数比2∶1组成的化合物中含有的化学键为___________ 。
(4)元素⑥的单质与①、③、④三种元素组成化合物的溶液反应的离子方程式为___________ 。
(5)元素②的一种氧化物具有还原性,可以冶炼生铁,写出其反应的化学方程式___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)①和③两种元素形成化合物的电子式为
(2)④、⑤、⑥三种元素的最高价氧化物对应水化物的碱性由强到弱的顺序为
(3)①和⑧两种元素按原子个数比2∶1组成的化合物中含有的化学键为
(4)元素⑥的单质与①、③、④三种元素组成化合物的溶液反应的离子方程式为
(5)元素②的一种氧化物具有还原性,可以冶炼生铁,写出其反应的化学方程式
您最近一年使用:0次
6 . I.如图为元素周期表的一部分,请回答下列问题。

(1)图中阴影部分所示区域的元素称为_______ 元素,下列元素属于该区域的是_______ 。
A.Ba B.Mn C.I D.Rb
(2)下列说法不正确的是_______;
II.已知A、B、C、D、E、F六种短周期元素的原子半径和主要化合价如表:
(3)写出C元素在元素周期表中的位置_______ ;
(4)E和F的最高价氧化物的水化物相互反应的离子方程式为_______ ;
(5)以上元素的单质中还原性最强的是_______ (填化学式);
(6)上述某种元素其最高价氧化物的水化物与其气态氢化物相互反应的化学方程式_______ 。

(1)图中阴影部分所示区域的元素称为
A.Ba B.Mn C.I D.Rb
(2)下列说法不正确的是_______;
| A.最高正价与最低负价绝对值相等的元素一定处于IVA族 |
| B.图中①形成的最高价氧化物的水化物比③形成的最高价氧化物的水化物碱性强 |
| C.图中②的单质可与冷水剧烈反应 |
| D.同周期相邻主族元素的原子序数可能相差1、11或25 |
II.已知A、B、C、D、E、F六种短周期元素的原子半径和主要化合价如表:
| 元素代号 | A | B | C | D | E | F |
| 原子半径/nm | 0.074 | 0.075 | 0.077 | 0.160 | 0.186 | 0.143 |
| 主要化合价 |  |  、 、 |  、 、 |  |  |  |
(4)E和F的最高价氧化物的水化物相互反应的离子方程式为
(5)以上元素的单质中还原性最强的是
(6)上述某种元素其最高价氧化物的水化物与其气态氢化物相互反应的化学方程式
您最近一年使用:0次
名校
7 . 下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为_______ 。
(2)地壳中含量最多的金属元素是____ ,写出元素⑥的简单气态氢化物的化学式______ 。
(3)这些元素中的最高价氧化物对应的水化物中,碱性最强的是______ ,呈两性的氢氧化物是_______ 。
(4)写出②、③、⑤对应离子的离子半径由大到小的顺序是______ ,
(5)写出②、⑦、⑩对应阴离子还原性由强到弱的顺序是______ 。
(6)元素⑦与元素⑩相比,非金属性较强的是____ ,能证明这一事实的依据是_____ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ⑥ | ① | ② | |||||
| 三 | ③ | ④ | ⑤ | ⑪ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(2)地壳中含量最多的金属元素是
(3)这些元素中的最高价氧化物对应的水化物中,碱性最强的是
(4)写出②、③、⑤对应离子的离子半径由大到小的顺序是
(5)写出②、⑦、⑩对应阴离子还原性由强到弱的顺序是
(6)元素⑦与元素⑩相比,非金属性较强的是
您最近一年使用:0次
名校
8 . 下表是元素周期表的一部分,请依据该表回答问题。
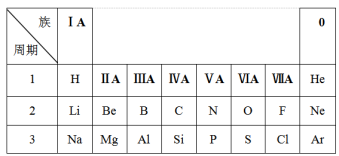
(1)第2周期VIIA族元素的原子结构示意图是___________ ,该元素与同周期IA族元素组成的化合物类型是___________ (填“离子化合物”或“共价化合物”)。
(2)第3周期元素的最高价氧化物对应水化物中,碱性最强的是___________ (填化学式,下同);具有两性的是___________ 。加热时,碳单质能与S的最高价氧化物对应的水化物的浓溶液反应,写出该反应的化学方程式___________ 。
(3)下列判断正确的是___________(填标号)。

(1)第2周期VIIA族元素的原子结构示意图是
(2)第3周期元素的最高价氧化物对应水化物中,碱性最强的是
(3)下列判断正确的是___________(填标号)。
| A.最低负化合价的绝对值:P>S |
| B.非金属性:P>N |
| C.离子半径:Mg2+>O2− |
| D.还原性:S2−>Cl− |
您最近一年使用:0次
9 . 如图是氨元素的几种价态与物质类别的对应关系:

回答下列问题:
(1)写出氮元素在元素周期表的位置_______ 。
(2)从氢元素化合价分析, 具有氧化性和还原性。写出
具有氧化性和还原性。写出 生成A的化学反应方程式:
生成A的化学反应方程式:_______ ,这个反应 体现了
体现了_______ 性。
(3) 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为_______ 。写出用C检验 的存在的离子方程式
的存在的离子方程式_______ 。
(4)物质B为氮元素的气态氢化物,B的化学式为_______ ;实验室制取B的化学方程式为_______ 。
(5)浓硝酸与木炭在加热条件下反应的化学方程式为_______ 。

回答下列问题:
(1)写出氮元素在元素周期表的位置
(2)从氢元素化合价分析,
 具有氧化性和还原性。写出
具有氧化性和还原性。写出 生成A的化学反应方程式:
生成A的化学反应方程式: 体现了
体现了(3)
 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为 的存在的离子方程式
的存在的离子方程式(4)物质B为氮元素的气态氢化物,B的化学式为
(5)浓硝酸与木炭在加热条件下反应的化学方程式为
您最近一年使用:0次
10 . 下表是元素周期表的一部分,请回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为________ 。
(2)写出③的单质的电子式________ 。
(3)①、⑥、⑦、⑧四种元素的最高价氧化物的水化物中碱性最强的是________ (填化学式)。写出⑥、⑧元素的最高价氧化物的水化物发生反应的离子方程式_________ 。
(4)②、③、④的简单氢化物中最稳定的是________ (填化学式),沸点最高的是________ (填结构式)。
(5)⑨的一种氧化物常用于漂白纸浆,该氧化物具有还原性,一定条件下能与常见氧化剂发生反应,写出其中一个反应的化学方程式_________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ③ | ④ | ⑤ | |||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为
(2)写出③的单质的电子式
(3)①、⑥、⑦、⑧四种元素的最高价氧化物的水化物中碱性最强的是
(4)②、③、④的简单氢化物中最稳定的是
(5)⑨的一种氧化物常用于漂白纸浆,该氧化物具有还原性,一定条件下能与常见氧化剂发生反应,写出其中一个反应的化学方程式
您最近一年使用:0次