解题方法
1 . 下表是元素周期表的一部分。
(1)写出表中 元素的元素符号:
元素的元素符号:
__________ 、
__________ 、
__________ 、
__________ 、
__________ 、
__________ 、
__________ 、
__________ 。
(2) 的简单离子的结构示意图为
的简单离子的结构示意图为________ 。
(3) 元素形成的单质中氧化性最强的是
元素形成的单质中氧化性最强的是_______ ,还原性最强的是_____ 。
(4) 元素最高价氧化物对应的水化物中酸性最强的是
元素最高价氧化物对应的水化物中酸性最强的是_____ ,最稳定的气态氢化物是______ 。
(5)按碱性逐渐减弱、酸性逐渐增强的顺序,将 、
、 、
、 、
、 4种元素的最高价氧化物对应的水化物的化学式进行排序
4种元素的最高价氧化物对应的水化物的化学式进行排序_______ 。
(6) 单质与
单质与 的最高价氧化物对应的水化物反应的离子方程式为
的最高价氧化物对应的水化物反应的离子方程式为________ 。
| 族 周期 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 |
| 1 |  | |||||||
| 2 |  |  |  | |||||
| 3 |  |  |  |  |
(1)写出表中
 元素的元素符号:
元素的元素符号:







(2)
 的简单离子的结构示意图为
的简单离子的结构示意图为(3)
 元素形成的单质中氧化性最强的是
元素形成的单质中氧化性最强的是(4)
 元素最高价氧化物对应的水化物中酸性最强的是
元素最高价氧化物对应的水化物中酸性最强的是(5)按碱性逐渐减弱、酸性逐渐增强的顺序,将
 、
、 、
、 、
、 4种元素的最高价氧化物对应的水化物的化学式进行排序
4种元素的最高价氧化物对应的水化物的化学式进行排序(6)
 单质与
单质与 的最高价氧化物对应的水化物反应的离子方程式为
的最高价氧化物对应的水化物反应的离子方程式为
您最近一年使用:0次
解题方法
2 . (1) 某元素价层电子排布式为3d64s2,该元素在周期表中位于_____ 区_____ 族。
(2)某元素N能层只有1个电子,其余能层均已填满电子,该元素价层电子排布图为_____ 。
(3) SO2分子中,S原子采用_____ 杂化轨道成键,该分子的价层电子对互斥模型_____ 。
(2)某元素N能层只有1个电子,其余能层均已填满电子,该元素价层电子排布图为
(3) SO2分子中,S原子采用
您最近一年使用:0次
3 . 画出下列各微粒的结构示意图:
(1)与氖原子电子层结构相同的-2价阴离子:_____________ 。
(2)最外层电子数为次外层电子数2倍的原子:________________ 。
(3)第2层电子数为第1层、第3层电子数之和的原子:________ 。
(4)观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:

①属于离子结构示意图的是_____ (填编号)。
②属于金属元素的是___ (填编号)
③性质最稳定的原子是(填写编号,下同)______ ,最容易失去电子的原子是____ ,最容易得到电子的原子是________ 。
④A在周期表中的位置_____ 周期______ 族。
(1)与氖原子电子层结构相同的-2价阴离子:
(2)最外层电子数为次外层电子数2倍的原子:
(3)第2层电子数为第1层、第3层电子数之和的原子:
(4)观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:

①属于离子结构示意图的是
②属于金属元素的是
③性质最稳定的原子是(填写编号,下同)
④A在周期表中的位置
您最近一年使用:0次
4 . 如图是元素周期表的一部分,其中每个数字序号代表一种 短周期元素。根据表中所列①~⑩元素,请按要求回答下列问题:

(1)元素⑤形成的氧化物的电子式为_______ ;①、⑦两种元素的最高价氧化物的熔点较高的是________ (填化学式)。
(2)①~⑨元素的最高价氧化物的水化物中酸性最强的是_______ (填化学式)。
(3)由③④⑩三种元素组成的离子化合物中所含有的化学键有______ 。
(4)①的单质与②的最高价氧化物的水化物的浓溶液反应的化学方程式为_________ 。
(5)下列事实能说明③非金属性比⑧强的有___________ (填字母)。
a.通常状况下,③的单质是无色气体,⑧的单质是固体
b.③的单质与⑧的氢化物溶液反应,溶液变浑浊
c.③与⑧两元素的简单氢化物受热分解,前者的分解温度高
d.常温常压下,③与⑧两元素的简单氢化物的沸点,前者高

(1)元素⑤形成的氧化物的电子式为
(2)①~⑨元素的最高价氧化物的水化物中酸性最强的是
(3)由③④⑩三种元素组成的离子化合物中所含有的化学键有
(4)①的单质与②的最高价氧化物的水化物的浓溶液反应的化学方程式为
(5)下列事实能说明③非金属性比⑧强的有
a.通常状况下,③的单质是无色气体,⑧的单质是固体
b.③的单质与⑧的氢化物溶液反应,溶液变浑浊
c.③与⑧两元素的简单氢化物受热分解,前者的分解温度高
d.常温常压下,③与⑧两元素的简单氢化物的沸点,前者高
您最近一年使用:0次
5 . 下表为元素周期表中的一部分,回答下列问题。
(1)这10种元素中,非金属性最强的是___ (填元素符号)。
(2)这10种元素中,最高价氧化物对应的水化物中碱性最强的是___ (填化学式)。.
(3)①、③两种元素按原子个数比1:4形成的化合物的结构式为___ 。
(4)元素④的最高价氧化物对应的水化物与元素⑩的简单氢化物反应的离子方程式为___ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 四 | ⑧ | ⑨ | ⑩ |
(1)这10种元素中,非金属性最强的是
(2)这10种元素中,最高价氧化物对应的水化物中碱性最强的是
(3)①、③两种元素按原子个数比1:4形成的化合物的结构式为
(4)元素④的最高价氧化物对应的水化物与元素⑩的简单氢化物反应的离子方程式为
您最近一年使用:0次
6 . (1)从能量的角度看,形成生成物中的化学键要__ (填“吸收”或"放出”,下同)能量;已知石墨比金刚石稳定,所以石墨转化为金刚石的反应要__ 热量。
(2)现有甲、乙、丙三种金属片:①把甲、乙用导线连接后同时浸入稀硫酸中;乙上有气泡产生,则__ (填“甲”或“乙”)发生氧化反应;②将乙、丙用导线连接后局时浸入稀硫酸中,电子的流动方向为乙→导线→丙。则三种金属的活动性由强到弱的顺序是__ 。
(3)短周期元素X的最高价氧化物的水化物化学式为HXO4,则其气态氢化物的化学式为__ ;在周期表中第__ 周期第_ 族。
(2)现有甲、乙、丙三种金属片:①把甲、乙用导线连接后同时浸入稀硫酸中;乙上有气泡产生,则
(3)短周期元素X的最高价氧化物的水化物化学式为HXO4,则其气态氢化物的化学式为
您最近一年使用:0次
名校
解题方法
7 . 下表是元素周期表的一部分,按要求填空(填元素符号或化学式):
(1)在这些元素中,最活泼的非金属元素是________ ,最不活泼的元素是_______ 。
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是_________ (此空可填化学式或填物质名称),碱性最强的是________ 。
(3)写出⑥和⑨的单质反应产物的电子式________ ,其晶体属于__________ 晶体。
(4) 在周期表中的位置:
在周期表中的位置:_______ ,它的最简单气态氢化物的电子式_________ ;
(5)判断⑥与⑦的单质金属性强弱的实验依据是___________ ;
(6)②与③可形成A2B2型分子,该分子中各原子均达到最外层8电子稳定结构,则该分子的电子式为___________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在这些元素中,最活泼的非金属元素是
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是
(3)写出⑥和⑨的单质反应产物的电子式
(4)
 在周期表中的位置:
在周期表中的位置:(5)判断⑥与⑦的单质金属性强弱的实验依据是
(6)②与③可形成A2B2型分子,该分子中各原子均达到最外层8电子稳定结构,则该分子的电子式为
您最近一年使用:0次
8 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系,下图是元素周期表的一部分, 回答下列问题:
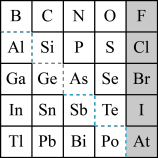
(1)元素Ga在元素周期表中的位置为:________ ;
(2)Sn的最高正价为_______ ,Cl的最高价氧化物对应水化物的化学式为______ ;
(3)根据元素周期律,推断:
①阴影部分元素形成的氢化物中热稳定性最高的是_____ ;(写化学式)
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4_______ H2SeO4 (填“>”、“<”、“=”或“无法比较”);
③氢化物的还原性:H2O_______ H2S (填“>”、“<”、“=”或“无法比较”);
④原子半径比较: N______ Si (填“>”、“<”、“=”或“无法比较”);
(4)可在图中分界线(虚线部分)附近寻找_______ (填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料 D.农药

(1)元素Ga在元素周期表中的位置为:
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素形成的氢化物中热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4
③氢化物的还原性:H2O
④原子半径比较: N
(4)可在图中分界线(虚线部分)附近寻找
A.优良的催化剂 B.半导体材料 C.合金材料 D.农药
您最近一年使用:0次
9 .  、
、 既是燃料又是化工原料。工业上,可用煤炭在高温下与水蒸气反应制备水煤气(主要成分为
既是燃料又是化工原料。工业上,可用煤炭在高温下与水蒸气反应制备水煤气(主要成分为 和
和 ),发生的反应为
),发生的反应为 。
。
(1)碳位于周期表中第__________ 周期第__________ 族。
(2)在体积可变的密闭容器中发生上述反应,改变下列条件,不会改变反应速率的是________ (填字母)。
a.增大压强 b.增大炭的质量 c.增大水蒸气浓度 d.升高温度
(3) 和
和 在一定条件下可以合成下列有机物,其中原子利用率小于100%的是
在一定条件下可以合成下列有机物,其中原子利用率小于100%的是_______ (填字母)。
a. b.
b. c.
c. d.
d.
(4) 和
和 在
在 溶液中可以组成燃料电池,装置如图所示。在石墨1极上发生的电极反应为
溶液中可以组成燃料电池,装置如图所示。在石墨1极上发生的电极反应为 ;在石墨2极上发生的电极反应为
;在石墨2极上发生的电极反应为 。
。
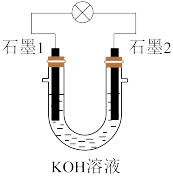
①石墨1极为____________ (填“负”或“正”)极。在石墨2极上发生________ 反应(填“氧化”或“还原”)。
②放电时,电子流向是_________ (填字母)。
a.由石墨1极流出,经外电路流向石墨2极 b.由石墨2极流出,经外电路流向石墨1极
c.由石墨1极流出,经电解质溶液流向石墨2极 d.由石墨1极流出,经电解质溶液流向石墨2极
 、
、 既是燃料又是化工原料。工业上,可用煤炭在高温下与水蒸气反应制备水煤气(主要成分为
既是燃料又是化工原料。工业上,可用煤炭在高温下与水蒸气反应制备水煤气(主要成分为 和
和 ),发生的反应为
),发生的反应为 。
。(1)碳位于周期表中第
(2)在体积可变的密闭容器中发生上述反应,改变下列条件,不会改变反应速率的是
a.增大压强 b.增大炭的质量 c.增大水蒸气浓度 d.升高温度
(3)
 和
和 在一定条件下可以合成下列有机物,其中原子利用率小于100%的是
在一定条件下可以合成下列有机物,其中原子利用率小于100%的是a.
 b.
b. c.
c. d.
d.
(4)
 和
和 在
在 溶液中可以组成燃料电池,装置如图所示。在石墨1极上发生的电极反应为
溶液中可以组成燃料电池,装置如图所示。在石墨1极上发生的电极反应为 ;在石墨2极上发生的电极反应为
;在石墨2极上发生的电极反应为 。
。
①石墨1极为
②放电时,电子流向是
a.由石墨1极流出,经外电路流向石墨2极 b.由石墨2极流出,经外电路流向石墨1极
c.由石墨1极流出,经电解质溶液流向石墨2极 d.由石墨1极流出,经电解质溶液流向石墨2极
您最近一年使用:0次
解题方法
10 . 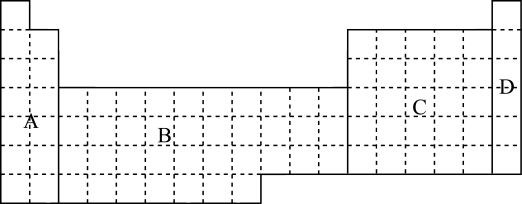
(1)在上面元素周期表中全部是金属元素的区域为____ 。
A B C D
(2)有人认为形成化合物最多的元素不是IVA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是____ (写出元素符号)。
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①画出甲原子的基态外围电子轨道表示式:_____ 。
② 甲、乙两元素相比较,金属性较强的是____ (填名称),可以验证该结论的实验是__ 。
A 将在空气中放置已久的这两种元素的块状单质分别放入热水中
B 将这两种元素的单质粉末分别和同浓度的盐酸反应
C 将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
D 比较这两种元素的气态氢化物的稳定性
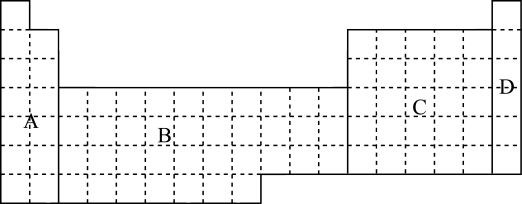
(1)在上面元素周期表中全部是金属元素的区域为
A B C D
(2)有人认为形成化合物最多的元素不是IVA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①画出甲原子的基态外围电子轨道表示式:
② 甲、乙两元素相比较,金属性较强的是
A 将在空气中放置已久的这两种元素的块状单质分别放入热水中
B 将这两种元素的单质粉末分别和同浓度的盐酸反应
C 将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
D 比较这两种元素的气态氢化物的稳定性
您最近一年使用:0次



