1 . 现行的元素周期表共18个纵行,18个族,七个周期( )
您最近一年使用:0次
解题方法
2 . 处于金属和非金属分界线附近的元素常作催化剂( )
您最近一年使用:0次
解题方法
3 . 联合国大会将2019年定为“化学元素周期表国际年”,显示了元素周期表的重要性。下表列出了a-j 10种元素在周期表中的位置:
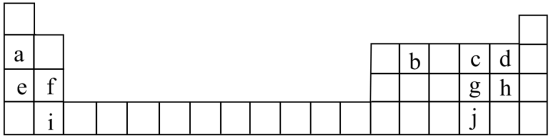
(1)元泰a的原于结构示意图为__________ 。
(2)元素b可以形成多种单质,写出其中的两种____________________ (填名称)。
(3)元素a~j中非金属性最强的是___________ (填元素符号)。
(4)若e单质着火,可用于灭火的物质是___________ (填字母)
A 自来水 B CO2. C 干沙子 D 湿抹布
(5)元素h和i形成的化合物中化学键的类型是___________ 键。h单质与NaOH溶液反应的离子方程式为____________ 。
(6)3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法正确的有___________ (填字母)。
A a的金属性比e弱 B 自然界中,e的储量比a高
B a的原子半径比e大 D 基于a的电池质量轻、易携带

(1)元泰a的原于结构示意图为
(2)元素b可以形成多种单质,写出其中的两种
(3)元素a~j中非金属性最强的是
(4)若e单质着火,可用于灭火的物质是
A 自来水 B CO2. C 干沙子 D 湿抹布
(5)元素h和i形成的化合物中化学键的类型是
(6)3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法正确的有
A a的金属性比e弱 B 自然界中,e的储量比a高
B a的原子半径比e大 D 基于a的电池质量轻、易携带
您最近一年使用:0次
2020-12-04更新
|
552次组卷
|
2卷引用:2020年7月广东省普通高中学业水平合格性考试化学试卷
名校
4 . 下表是元素周期表的一部分,回答下列有关问题(用化学符号回答):
(1)写出序号对应的元素符号:①________ ;④__________ ;⑤_________ ;
(2)在①~⑨元素中,最活泼的金属元素是________ ,最活泼的非金属元素是_______ 。
(3)在①~⑨元素的最高价氧化物对应的水化物中,碱性最强的是___________ ,呈两性的是____________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | He | ||||||
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)写出序号对应的元素符号:①
(2)在①~⑨元素中,最活泼的金属元素是
(3)在①~⑨元素的最高价氧化物对应的水化物中,碱性最强的是
您最近一年使用:0次
2020-12-02更新
|
509次组卷
|
2卷引用:广东省珠海市北京师范大学珠海分校附属外国语学校2020-2021学年高二上学期期中考试化学试题(B卷)
名校
5 . 下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)非金属性最强的元素是______ (填元素符号,下同),形成化合物种类最多的元素是________________________ 。
(2)第三周期元素除⑩外原子半径最小的是______ (填元素符号),
(3)这些元素的最高价氧化物对应水化物中碱性最强的是__________ (填化学式,下同),具有两性的是____________ 。
(4)⑤、⑧两种元素的最高价氧化物对应的水化物相互反应的离子方程式为__________ 。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)非金属性最强的元素是
(2)第三周期元素除⑩外原子半径最小的是
(3)这些元素的最高价氧化物对应水化物中碱性最强的是
(4)⑤、⑧两种元素的最高价氧化物对应的水化物相互反应的离子方程式为
您最近一年使用:0次
名校
6 . 下表是元素周期表的一部分,其中每个数字序号代表一种短周期元素。
(1)⑤、⑥两元素的最高价氧化物对应的水合物酸性更强的是_______ (写化学式)。
(2)②和④形成的化合物的化学式是________ ;
(3)在上述六种元素中,原子半径最大的是_______ (写元素符号)。
(4)写出①的气态氢化物与它的最高价氧化物对应的水化物发生反应的离子方程式为________ 。
| ① | ② | |||||||
| ③ | ④ | ⑤ | ⑥ | |||||
(1)⑤、⑥两元素的最高价氧化物对应的水合物酸性更强的是
(2)②和④形成的化合物的化学式是
(3)在上述六种元素中,原子半径最大的是
(4)写出①的气态氢化物与它的最高价氧化物对应的水化物发生反应的离子方程式为
您最近一年使用:0次
名校
解题方法
7 . 下表是元素周期表的一部分,按要求回答下列问题:
(1)③的元素符号为__________ ,⑦的原子结构示意图为___________ ,⑨的单质的电子式为___________ 。
(2)①~⑨对应元素中,非金属性最强的是___________ (填元素符号,下同),金属性最强的是__________ ,单质的化学性质最不活泼的是__________ 。
(3)②③④三种元素对应的简单氢化物中最稳定的是__________ (填化学式,下同),⑥⑦两种元素的最高价氧化物对应水化物中,碱性最强的是__________ 。
(4)⑧的最高价氧化物对应水化物的化学式为____________ ,写出实验室制备②的简单氢化物的化学方程式____________ 。
| 族 周期 | ⅠA | ⅡA | Ⅲ | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ |
(1)③的元素符号为
(2)①~⑨对应元素中,非金属性最强的是
(3)②③④三种元素对应的简单氢化物中最稳定的是
(4)⑧的最高价氧化物对应水化物的化学式为
您最近一年使用:0次
2020-11-29更新
|
716次组卷
|
6卷引用:云南省2020年9月普通高中学业水平考试化学试卷
云南省2020年9月普通高中学业水平考试化学试卷云南省玉溪市一中2020-2021学年高一下学期期中考试化学(文)试题(已下线)专题02 元素周期律【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版必修2)云南省梁河县第一中学2020-2021学年高一下学期期中考试化学试题 云南省玉溪市第二中学2021-2022学年高二上学期期中考试化学试题云南省玉溪市江川区第二中学2021-2022学年高二上学期期中考试化学试题
名校
8 . 下表为元素周期表的一部分,请参照元素①一④在表中的位置回答下列问题:
(1)③、⑤、⑥的离子半径由大到小的顺序为____________ '(用离子符号表示)。
(2)写出⑤和⑥的最高价氧化物的水化物相互反应的化学方程式_______________
(3)②的某核素可用于文物年代的测定,该核素有8个中子,该核素的符号是______
(4)比较元素②、⑦和⑧的最高价氧化物的水化物的酸性大小_____
(5)①④两种元素可组成的一种既有极性共价键也有非极性共价键的化合物,写出该物质的电子式______
(6)①和④的单质可组成燃料电池,正极反应物为_____ (用化学式表示,下同),若电解溶液为稀硫酸,写出负极的电极反应__________
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)③、⑤、⑥的离子半径由大到小的顺序为
(2)写出⑤和⑥的最高价氧化物的水化物相互反应的化学方程式
(3)②的某核素可用于文物年代的测定,该核素有8个中子,该核素的符号是
(4)比较元素②、⑦和⑧的最高价氧化物的水化物的酸性大小
(5)①④两种元素可组成的一种既有极性共价键也有非极性共价键的化合物,写出该物质的电子式
(6)①和④的单质可组成燃料电池,正极反应物为
您最近一年使用:0次
名校
9 . 下表是元素周期表短周期的一部分:
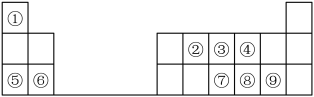
请按要求用化学用语 回答下列问题:
(1)元素④、⑥、⑨的离子半径由大到小的顺序为___ ;
(2)用电子式表示元素④与元素⑥形成的化合物的形成过程___ ;
(3)比元素⑦的原子序数多17的元素在周期表的位置为___ ;
(4)写出由①④⑤三种元素组成的一种离子化合物的电子式___ ,若将其溶于水,破坏了其中的___ (填“离子键”、“共价键”或“离子键和共价键”);
(5)元素①和元素④形成的化合物及元素①和元素⑧形成的化合物均为18电子分子,请写出这两种化合物按物质的量之比4:1反应的离子方程式___ 。

请按要求
(1)元素④、⑥、⑨的离子半径由大到小的顺序为
(2)用电子式表示元素④与元素⑥形成的化合物的形成过程
(3)比元素⑦的原子序数多17的元素在周期表的位置为
(4)写出由①④⑤三种元素组成的一种离子化合物的电子式
(5)元素①和元素④形成的化合物及元素①和元素⑧形成的化合物均为18电子分子,请写出这两种化合物按物质的量之比4:1反应的离子方程式
您最近一年使用:0次
2020-11-24更新
|
327次组卷
|
2卷引用:四川省射洪中学校2020-2021学年高二上学期第二次月考化学试题
10 . 图中反应①是制备SiH4的一种方法,其副产物MgCl2·6NH3是优质的镁资源。回答下列问题:

(1)Si在元素周期表中的位置是______ ,NH3的电子式为_______ 。
(2)A2B的化学式为______ ,上图中可以循环使用的物质有______ 。
(3)在一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料:______ (填化学式),其中含有的化学键类型是________ 。
(4)单质硼可用于生成具有优良抗冲击性能的硼钢。以硼酸(H3BO3)和金属镁为原料在加热条件下制备单质硼,用化学方程式表示其制备过程:________ 、___________ 。

(1)Si在元素周期表中的位置是
(2)A2B的化学式为
(3)在一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料:
(4)单质硼可用于生成具有优良抗冲击性能的硼钢。以硼酸(H3BO3)和金属镁为原料在加热条件下制备单质硼,用化学方程式表示其制备过程:
您最近一年使用:0次



