1 . 元素周期表是学习物质结构和性质的重要工具,如图是元素周期表的一部分,①~⑧分别代表一种元素。回答下列问题:
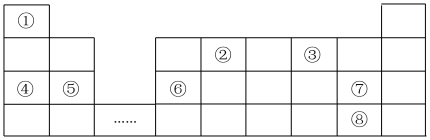
(1)元素①含2个中子的核素为_____ (填符号)。
(2)元素②、③形成的化合物_____ (填“属于”或“不属于”)电解质。
(3)元素③、⑤、⑦形成的简单离子半径由大到小的顺序为_____ (用离子符号填空)。
(4)元素④、⑤、⑥金属性由强到弱的顺序为_____ ,元素④和⑥的最高价氧化物对应的水化物反应的离子方程式为_____ 。
(5)将少量元素⑦的单质通入元素④与元素⑧形成化合物的水溶液中,溶液中的实验现象为_____ ,该反应的离子方程式为_____ 。

(1)元素①含2个中子的核素为
(2)元素②、③形成的化合物
(3)元素③、⑤、⑦形成的简单离子半径由大到小的顺序为
(4)元素④、⑤、⑥金属性由强到弱的顺序为
(5)将少量元素⑦的单质通入元素④与元素⑧形成化合物的水溶液中,溶液中的实验现象为
您最近一年使用:0次
2 . 已知元素周期表中共有18纵行,如图实线表示元素周期表的边界。按电子排布,可把周期表里的元素划分为几个区:s区、p区、d区、ds区等。除ds区外,其他区的名称来自按构造原理最后填入的电子的能级符号。
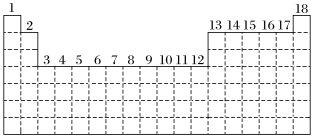
(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并分别用阴影 和
和 表示d区和ds区。
表示d区和ds区。___________
(2)有的同学受这种划分的启发,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在___________ 区。
(3)随着科学技术的发展,不断有新的元素被发现。若把第七周期排满,则元素周期表共可以排布___________ 种元素。

(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并分别用阴影
 和
和 表示d区和ds区。
表示d区和ds区。(2)有的同学受这种划分的启发,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在
(3)随着科学技术的发展,不断有新的元素被发现。若把第七周期排满,则元素周期表共可以排布
您最近一年使用:0次
2023高三·全国·专题练习
3 . 1869年,俄国化学家门捷列夫提出了元素周期律,并在此基础上发表了第一张元素周期表。为了纪念元素周期表诞生150年,联合国将2019年定为“国际化学元素周期表年”,并认为元素周期表是“科学共同的语言”。
(1)认识元素周期表的结构:
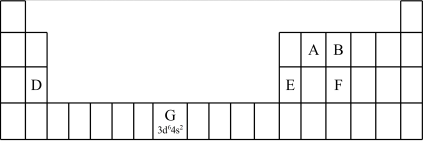
①在元素周期表中,第ⅠB、ⅡB元素属于___________ 区。
②2017年5月9日我国发布了113号Nh、115号Mc、117号Ts、118号Og四种元素,则下列说法正确的是___________ (填字母序号)。
a.113号元素在周期表中的位置是第七周期VB族
b.117号元素Ts位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:Nh>Mc
(2)认识原子结构与元素周期表的关系:见表中元素G的信息,其中“3d64s2”称为该元素原子的___________ ,该元素M能层上具有___________ 种不同运动状态的电子。
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D___________ E(填“>”“<”或“=”)。
②气态氢化物的沸点:B___________ F(填“>”“<”或“=”),理由是___________ 。
(1)认识元素周期表的结构:

①在元素周期表中,第ⅠB、ⅡB元素属于
②2017年5月9日我国发布了113号Nh、115号Mc、117号Ts、118号Og四种元素,则下列说法正确的是
a.113号元素在周期表中的位置是第七周期VB族
b.117号元素Ts位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:Nh>Mc
(2)认识原子结构与元素周期表的关系:见表中元素G的信息,其中“3d64s2”称为该元素原子的
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D
②气态氢化物的沸点:B
您最近一年使用:0次
名校
4 . 现代化学在材料、资源、能源、环境、医药、信息技术等领域均有重大应用。
I.新疆也要建造磁悬浮列车了。在磁悬浮列车制造过程中将使用大量含钇(Y)元素的超导材料。钇(Y)元素在元素周期表中的信息如图所示:
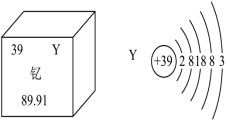
(1)钇原子核内有___________ 个质子,图中89.91表示的是___________ 。
(2)钇元素形成氧化物的化学式是___________ 。
II.电解质是维持人体生理活动的基础之一、请回答下列问题:
①CO2 ②Al ③乙醇 ④Fe(OH)3胶体 ⑤熔融BaSO4 ⑥KOH溶液 ⑦固态
(3)上述物质中属于电解质的是___________ 。(填序号)
(4)属于非电解质的是___________ 。(填序号)
(5)能导电的纯净物是___________ 。(填序号)
(6)写出⑦在水中的电离方程式___________ 。
(7)写出①和⑥的反应方程式___________ 。
(8)请写出实验室中制备Fe(OH)3胶体的化学反应方程式___________ 。
I.新疆也要建造磁悬浮列车了。在磁悬浮列车制造过程中将使用大量含钇(Y)元素的超导材料。钇(Y)元素在元素周期表中的信息如图所示:

(1)钇原子核内有
(2)钇元素形成氧化物的化学式是
II.电解质是维持人体生理活动的基础之一、请回答下列问题:
①CO2 ②Al ③乙醇 ④Fe(OH)3胶体 ⑤熔融BaSO4 ⑥KOH溶液 ⑦固态

(3)上述物质中属于电解质的是
(4)属于非电解质的是
(5)能导电的纯净物是
(6)写出⑦在水中的电离方程式
(7)写出①和⑥的反应方程式
(8)请写出实验室中制备Fe(OH)3胶体的化学反应方程式
您最近一年使用:0次
解题方法
5 . 下表列出了A~R9种元素在周期表中的位置:
请回答下列问题。
(1)这些元素分别为:A___________ ,B___________ ,C___________ ,D___________ ,E___________ ,F___________ ,G___________ ,R___________ ,其中化学性质最不活泼的是___________ (用元素符号表示)。
(2)画出G的原子结构示意图___________ 。
(3)元素周期表共有___________ 个周期___________ 个族,18纵行元素化合价通常表现为___________ 价所以称为0族元素,又叫惰性气体元素。A位于___________ 周期___________ 族
(4)H元素与A元素形成的化合物高温灼烧时,火焰呈___________ 色。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H | ||||||
(1)这些元素分别为:A
(2)画出G的原子结构示意图
(3)元素周期表共有
(4)H元素与A元素形成的化合物高温灼烧时,火焰呈
您最近一年使用:0次
2024-01-05更新
|
150次组卷
|
2卷引用:贵州省清镇市博雅实验学校2023-2024学年高一上学期第四次月考化学试卷
名校
6 . 航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料。
(1)写出高氯酸铵组成元素中,原子核外有三层电子的原子的结构示意图___________ 。
(2)高氯酸铵对应酸高氯酸HClO4的酸酐是___________ 。
(3)150℃时高氯酸铵发生分解反应:2NH4ClO4=N2↑+Cl2↑+2O2↑+4H2O↑,其气态生成物组成的混合气的平均相对分子质量为___________ 。
(1)写出高氯酸铵组成元素中,原子核外有三层电子的原子的结构示意图
(2)高氯酸铵对应酸高氯酸HClO4的酸酐是
(3)150℃时高氯酸铵发生分解反应:2NH4ClO4=N2↑+Cl2↑+2O2↑+4H2O↑,其气态生成物组成的混合气的平均相对分子质量为
您最近一年使用:0次
名校
7 . 肼(N2H4)是重要的化工原料,能与水、乙醇等混溶;它是一种二元弱碱,在水中的电离方式与氨相似,室温下电离常数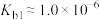 ;在碱性溶液中,N2H4是强还原剂。
;在碱性溶液中,N2H4是强还原剂。
(1)写出N元素在元素周期表中的位置___________ 。
(2)写出N2H4与过量硫酸反应形成的酸式盐的化学式___________ 。
(3)N2H4可通过NH3和NaClO反应制得,总反应主要分为两步,
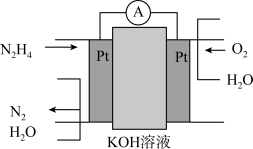
已知第一步: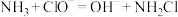
①写出第二步反应的离子方程式___________ 。
②请设计实验,检验总反应中产物的主要阴离子(假设反应物完全反应)___________ 。
(4)N2H4是一种高能燃料,可用于燃料电池,原理如图,电池的负极反应式为___________ 。
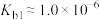 ;在碱性溶液中,N2H4是强还原剂。
;在碱性溶液中,N2H4是强还原剂。(1)写出N元素在元素周期表中的位置
(2)写出N2H4与过量硫酸反应形成的酸式盐的化学式
(3)N2H4可通过NH3和NaClO反应制得,总反应主要分为两步,
已知第一步:
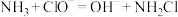
①写出第二步反应的离子方程式
②请设计实验,检验总反应中产物的主要阴离子(假设反应物完全反应)
(4)N2H4是一种高能燃料,可用于燃料电池,原理如图,电池的负极反应式为

您最近一年使用:0次
8 . 元素周期表是学习和研究化学的重要工具,下面是元素周期表的部分内容,请根据下表回答问题:
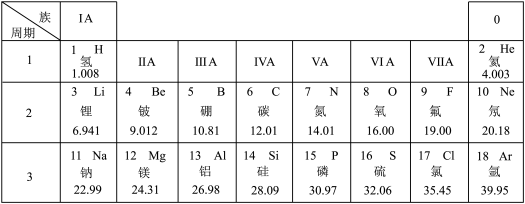
(1)发现了元素周期律并编制出元素周期表的化学家是___________(填字母)。
(2)氟元素是人体必需微量元素之一,能防治龋齿。氟元素的相对原子质量为___________ 。
(3)已知某微粒的结构示意图为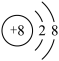 ,请写出该微粒的符号
,请写出该微粒的符号___________ 。
(4)地壳中含量最多的金属元素和最多的非金属元素组成的化合物的化学式为___________ 。

(1)发现了元素周期律并编制出元素周期表的化学家是___________(填字母)。
| A.门捷列夫 | B.拉瓦锡 | C.道尔顿 | D.阿伏加德罗 |
(3)已知某微粒的结构示意图为
 ,请写出该微粒的符号
,请写出该微粒的符号(4)地壳中含量最多的金属元素和最多的非金属元素组成的化合物的化学式为
您最近一年使用:0次
9 . 合成氨是人类科学技术发展史上的一项重大成就,是化学和技术对社会发展与进步的巨大贡献。
(1)基态氮原子中,能量最高的电子的电子云在空间有___________ 个伸展方向。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用“ ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为___________ 。
(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有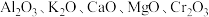 等氧化物中的几种。
等氧化物中的几种。
①Cr原子的价电子排布图为___________ ;第四周期ds区元素中,与基态Cr原子最外层电子数目相同的元素的元素符号为___________ 。
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素有___________ (填元素符号)。
(4)我国科研人员研制出了 (M为Fe、Mn等金属)等催化剂,使得合成氨工业温度,压强分别降到了350℃、
(M为Fe、Mn等金属)等催化剂,使得合成氨工业温度,压强分别降到了350℃、 ,这是近年来合成氨反应研究中的重要突破。第三电离能
,这是近年来合成氨反应研究中的重要突破。第三电离能
___________ 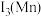 (填“>”或“<”),原因是
(填“>”或“<”),原因是___________ 。
(1)基态氮原子中,能量最高的电子的电子云在空间有
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用“
 ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
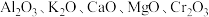 等氧化物中的几种。
等氧化物中的几种。①Cr原子的价电子排布图为
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素有
(4)我国科研人员研制出了
 (M为Fe、Mn等金属)等催化剂,使得合成氨工业温度,压强分别降到了350℃、
(M为Fe、Mn等金属)等催化剂,使得合成氨工业温度,压强分别降到了350℃、 ,这是近年来合成氨反应研究中的重要突破。第三电离能
,这是近年来合成氨反应研究中的重要突破。第三电离能
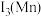 (填“>”或“<”),原因是
(填“>”或“<”),原因是
您最近一年使用:0次
名校
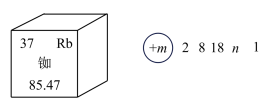
10 . 近年来,我国航空航天事业成果显著,“北斗三号”导航卫星搭载了精密计时的铷( )原子钟。如图为铷元素在元素周期表中的信息和铷的原子结构示意图(如图)。回答下列问题:
)原子钟。如图为铷元素在元素周期表中的信息和铷的原子结构示意图(如图)。回答下列问题:
(1)下列说法错误的是_____(填字母)。
(2) 原子第一电子层上电子的能量比最外层上电子的能量
原子第一电子层上电子的能量比最外层上电子的能量_____ (填“低”或“高”)。
(3)如图2中A-E所示粒子共表示种元素;铷元素原子的化学性质与如图中_____ (填字母)的化学性质相似;属于阴离子结构示意图的是_____ (填字母);写出B与D形成化合物的化学式_____ 。
(4)在核电荷数1~10的元素内,列举两个与图2中E电子层结构相同的离子,写出离子的符号_____ 。
A.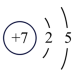 B.
B.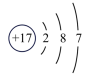 C.
C.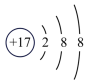 D.
D.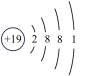 E.
E.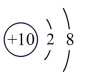
 )原子钟。如图为铷元素在元素周期表中的信息和铷的原子结构示意图(如图)。回答下列问题:
)原子钟。如图为铷元素在元素周期表中的信息和铷的原子结构示意图(如图)。回答下列问题:
(1)下列说法错误的是_____(填字母)。
A.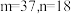 |
| B.铷是金属元素 |
| C.铷的相对原子质量是85.47 |
| D.铷原子有5个电子层,最外层有1个电子 |
(2)
 原子第一电子层上电子的能量比最外层上电子的能量
原子第一电子层上电子的能量比最外层上电子的能量(3)如图2中A-E所示粒子共表示种元素;铷元素原子的化学性质与如图中
(4)在核电荷数1~10的元素内,列举两个与图2中E电子层结构相同的离子,写出离子的符号
A.
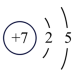 B.
B. C.
C. D.
D. E.
E.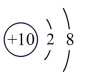
您最近一年使用:0次



