名校
解题方法
1 . 中国高铁对实现“一带一路”的战略构想有重要的作用。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是___________ 。
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是___________ ;乘务员使用的无线通话机的芯片材料所含元素在元素周期中的位置___________ 。
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式___________ 。
(4)高铁上的卫生间没有任何异味,是由于所使用的马桶、地漏和洗手盆下水口都是纳米硅胶的高科技产品,向硅酸钠溶液中加入稀盐酸可产生硅酸胶体,该反应的离子方程式___________ 。
(5)硅酸盐材料具有硬度高、难溶于水、耐高温等特点。硅酸盐中常含有Al、K等元素,如钾长石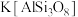 和钠长石
和钠长石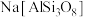 等,
等,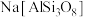 用氧化物形式表示为
用氧化物形式表示为___________ 。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式
(4)高铁上的卫生间没有任何异味,是由于所使用的马桶、地漏和洗手盆下水口都是纳米硅胶的高科技产品,向硅酸钠溶液中加入稀盐酸可产生硅酸胶体,该反应的离子方程式
(5)硅酸盐材料具有硬度高、难溶于水、耐高温等特点。硅酸盐中常含有Al、K等元素,如钾长石
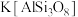 和钠长石
和钠长石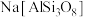 等,
等,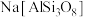 用氧化物形式表示为
用氧化物形式表示为
您最近一年使用:0次
名校
2 . 元素周期表反映元素之间的内在联系,是研究物质性质的重要工具。如表是元素周期表的一部分,请回答下列问题:
(1)元素②、③、⑥的简单离子半径由大到小的排序为___________ (填离子符号)。
(2)②和④组成的物质中含有___________ 键,可以证明该化合物含有此类型化学键的实验事实为___________ 。
(3)⑤的氧化物和⑥的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(4)已知④的单质与①的最高价氧化物A在点燃条件下能反应生成黑色单质,推测③的单质___________ (填“能”或“不能”)与A反应,说明推测的理由___________ 。
| 周期 | IA | 0 | |||||||
| 1 | IIA | … | IIIA | IVA | VA | VIA | VIIA | ||
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | |||||
(2)②和④组成的物质中含有
(3)⑤的氧化物和⑥的最高价氧化物对应的水化物反应的离子方程式为
(4)已知④的单质与①的最高价氧化物A在点燃条件下能反应生成黑色单质,推测③的单质
您最近一年使用:0次
名校
3 . 如图是元素周期表的一部分,A~J代表对应的元素,回答下列问题:
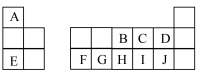
(1)F的元素符号为___________ ,元素C在周期表中的位置为___________ 。
(2)A、D和E三种元素的离子半径由大到小的顺序是___________ (用离子符号表示)。
(3)图中对应元素最高价氧化物的水化物中,碱性最强的是___________ (填化学式)。
(4)A、B和J三种元素形成常见化合物所含化学键的类型是___________ 。
(5)下列说法错误的是___________ (填标号)。
a.单质的熔点:
b.简单氢化物的沸点:
c.氧化物对应水化物的酸性:
(6)元素F的单质与元素E的最高价氧化物对应水化物反应的离子方程式为___________ 。

(1)F的元素符号为
(2)A、D和E三种元素的离子半径由大到小的顺序是
(3)图中对应元素最高价氧化物的水化物中,碱性最强的是
(4)A、B和J三种元素形成常见化合物所含化学键的类型是
(5)下列说法错误的是
a.单质的熔点:

b.简单氢化物的沸点:

c.氧化物对应水化物的酸性:

(6)元素F的单质与元素E的最高价氧化物对应水化物反应的离子方程式为
您最近一年使用:0次
2023-09-12更新
|
453次组卷
|
2卷引用:安徽省皖江名校联考2023-2024学年高二上学期开学化学试题
4 . I.我国科学家在铁基高温超导体的研究上取得重大突破,发现了该超导体是由Fe、Ba、As三种元素组成,这为进一步理解超导配对机理及其与电荷密度波的关系提供了重要实验证据。回答下列问题:
(1)As元素属于元素周期表的___________ 区元素,其价电子排布式是___________ 。
(2)基态Fe原子核外电子排布式为___________ 。
Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有___________ 种。
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的___________ 区(用符号填空),原子序数最大的在周期表的第___________ 周期、___________ 族。
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为d0或d10排布时,无颜色,为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色。据此判断,[Mn(H2O)6]2+___________ (填“无”或“有”)颜色。
(1)As元素属于元素周期表的
(2)基态Fe原子核外电子排布式为
Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为d0或d10排布时,无颜色,为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色。据此判断,[Mn(H2O)6]2+
您最近一年使用:0次
名校
5 . 生活中处处有化学。请回答下列问题:
(1)苏打水是很多人喜爱的饮品,请写出小苏打在水中的电离方程式_______ 。
(2)“84消毒液”与洁厕灵(主要成分是浓盐酸)不能混用,混合会产生黄绿色的有毒气体,请用离子方程式解释原因_______ 。
(3)Na2O2常用作呼吸面罩供氧剂,请写出Na2O2的电子式_______ 。
(4)硅是太阳能电池板的主要原材料,请写出硅元素在周期表的位置_______ 。
(5)4gCO在氧气中燃烧生成CO2,放出9.6kJ热量,写出CO燃烧的热化学方程式_______ 。
(6)已知:①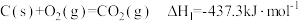
②H2(g)+1/2O2(g)=H2O(g) ∆H2=-285.8kJ·mol-1
③CO(g)+1/2O2(g)=CO2(g) ∆H3=-283.0kJ·mol-1
写出煤气化(碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式_______ 。
(1)苏打水是很多人喜爱的饮品,请写出小苏打在水中的电离方程式
(2)“84消毒液”与洁厕灵(主要成分是浓盐酸)不能混用,混合会产生黄绿色的有毒气体,请用离子方程式解释原因
(3)Na2O2常用作呼吸面罩供氧剂,请写出Na2O2的电子式
(4)硅是太阳能电池板的主要原材料,请写出硅元素在周期表的位置
(5)4gCO在氧气中燃烧生成CO2,放出9.6kJ热量,写出CO燃烧的热化学方程式
(6)已知:①
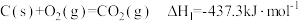
②H2(g)+1/2O2(g)=H2O(g) ∆H2=-285.8kJ·mol-1
③CO(g)+1/2O2(g)=CO2(g) ∆H3=-283.0kJ·mol-1
写出煤气化(碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式
您最近一年使用:0次
6 . 元素周期表中周期与族的划分与原子结构的哪部分有关_____ ?
您最近一年使用:0次
7 . 每一周期都是从活泼金属开始以惰性气体结束吗_____ ?
您最近一年使用:0次
8 . 填空
(1)砷原子的最外层电子排布式是4s24p3,在元素周期表中,砷元素位于第_____ 周期_____ 族;最高价氧化物的化学式为_____ ,砷酸钠的化学式是_____ 。
(2)已知下列元素在周期表中的位置,写出它们的价电子排布式和元素符号:
①第4周期ⅣB族_____ ;
②第5周期ⅦA族_____ 。
(1)砷原子的最外层电子排布式是4s24p3,在元素周期表中,砷元素位于第
(2)已知下列元素在周期表中的位置,写出它们的价电子排布式和元素符号:
①第4周期ⅣB族
②第5周期ⅦA族
您最近一年使用:0次
9 . 某元素M2+的3d轨道上有5个电子,则
(1)M原子的核外电子排布式为_____ 。
(2)M元素在元素周期表中的位置为第_____ 周期。
(1)M原子的核外电子排布式为
(2)M元素在元素周期表中的位置为第
您最近一年使用:0次



