1 . X、Y、Z、W、M为原子序数依次增大的前四周期元素,5种元素组成的化合物M(YX3)4WZ常用作杀虫剂。其中Y的基态原子2p轨道半充满,Z为地壳中含量最高的元素,Z的核外电子数等于X、Y核外电子数之和,W和Z同族,M元素基态原子的内层电子全充满、最外层只有1个电子。下列说法错误的是
| A.原子半径:W>Y>Z |
| B.简单氢化物的稳定性:Y>Z |
| C.M元素位于周期表的ds区 |
D.YX3和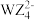 的中心原子杂化方式相同 的中心原子杂化方式相同 |
您最近一年使用:0次
名校
2 . 短周期主族元素V、W、X、Y、Z的原子序数依次增大。基态V原子核外3个能级上电子数相等,基态X原子核外s能级、p能级上电子总数相等。0.2molZ与足量的稀硫酸反应产生 (标准状况)。Y的部分电离能数据如下:
(标准状况)。Y的部分电离能数据如下:
下列叙述错误的是
 (标准状况)。Y的部分电离能数据如下:
(标准状况)。Y的部分电离能数据如下:| 电离能 |  |  |  |  |
( ) ) | 738 | 1451 | 7733 | 10540 |
| A.原子半径:Y>Z>V | B.第一电离能:V<W<X |
| C.简单氢化物的稳定性:V<W<X | D.最高价氧化物对应水化物的碱性:Z<Y |
您最近一年使用:0次
名校
解题方法
3 . 前四周期元素A、B、C、D、E、F、G、H的原子序数依次增大,在元素周期表中A的原子半径最小,B与C相邻且C的最外层电子数是次外层的3倍,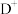 与
与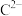 具有相同的电子层结构,E是地壳中含量最多的金属元素,F与C同主族,DGC是一种常见的漂白性物质,H原子的最外层只有1个电子,内层属于全满状态。回答下列问题:
具有相同的电子层结构,E是地壳中含量最多的金属元素,F与C同主族,DGC是一种常见的漂白性物质,H原子的最外层只有1个电子,内层属于全满状态。回答下列问题:
(1)C在元素周期表中的位置为___________ , 的离子结构示意图
的离子结构示意图___________ 。
(2)C和D也可形成一种漂白性物质,其电子式为___________ ,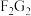 是
是___________ 键(填“极性键”或“非极性键”)构成的___________ 分子(填“极性”或“非极性”)。
(3)比较C和F简单氢化物的键角大小:___________ (用化学式表示),F和G的最高价氧化物的水化物酸性较强的是___________ (用化学式表示)。
(4)比较C、D、E三者离子半径的大小:___________ (用离子符号表示)。
(5)下列叙述正确且能用于比较元素D和E金属性强弱的是___________(填序号)。
(6)过量的 与G的单质的反应方程式:
与G的单质的反应方程式:___________ 。
(7)H的氢氧化物可溶于B的简单氢化物对应的水溶液反应,其离子方程式为___________ 。
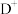 与
与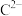 具有相同的电子层结构,E是地壳中含量最多的金属元素,F与C同主族,DGC是一种常见的漂白性物质,H原子的最外层只有1个电子,内层属于全满状态。回答下列问题:
具有相同的电子层结构,E是地壳中含量最多的金属元素,F与C同主族,DGC是一种常见的漂白性物质,H原子的最外层只有1个电子,内层属于全满状态。回答下列问题:(1)C在元素周期表中的位置为
 的离子结构示意图
的离子结构示意图(2)C和D也可形成一种漂白性物质,其电子式为
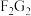 是
是(3)比较C和F简单氢化物的键角大小:
(4)比较C、D、E三者离子半径的大小:
(5)下列叙述正确且能用于比较元素D和E金属性强弱的是___________(填序号)。
| A.在化合物中E的化合价比D的高 |
| B.E的单质不能与冷水反应而D的单质能 |
| C.E的最高价氧化物对应水化物的碱性比D弱 |
| D.D的单质无法从E的盐溶液中置换出E |
 与G的单质的反应方程式:
与G的单质的反应方程式:(7)H的氢氧化物可溶于B的简单氢化物对应的水溶液反应,其离子方程式为
您最近一年使用:0次
名校
4 . A、B、C、D、E五种原子序数均小于18的元素,且原子序数依次增大,其中B与C的电子层数相同,D与E的电子层数相同,A与D的最外层电子数相同,C与E的最外层电子数相同,E元素的原子最外层电子数是电子层数的2倍,D与其他具有相同电子层数的原子相比半径最大。又知由B元素组成的单质是空气中的主要成分。
(1)B的元素名称是_______ ,该元素的原子结构示意图为_______ ,核外有___ 个未成对电子,用电子式表示B的简单氢化物的形成过程_________ 。
(2)C、D、E三种元素形成的简单离子的半径由大到小的顺序是________ (用离子符号表示)。
(3)请在以上五种元素中任意选择几种元素,画出由这几种元素组成的离子化合物的电子式(画出1种即可)_____ 。
(4)以下说法正确的是________ 。
①B的氧化物均为酸性氧化物
②A和C形成的化合物中既可能存在极性共价键,也可能存在非极性共价键
③由A、B、C形成的化合物中不可能存在离子键
④D2E的熔沸点较高,硬度较大
(1)B的元素名称是
(2)C、D、E三种元素形成的简单离子的半径由大到小的顺序是
(3)请在以上五种元素中任意选择几种元素,画出由这几种元素组成的离子化合物的电子式(画出1种即可)
(4)以下说法正确的是
①B的氧化物均为酸性氧化物
②A和C形成的化合物中既可能存在极性共价键,也可能存在非极性共价键
③由A、B、C形成的化合物中不可能存在离子键
④D2E的熔沸点较高,硬度较大
您最近一年使用:0次
2024-01-21更新
|
133次组卷
|
2卷引用:黑龙江省牡丹江市第三高级中学2023-2024学年高三上学期第三次月考化学试卷
2023高三·全国·专题练习
解题方法
5 . 已知W、X、Y、Z均为短周期元素,常温下,它们的最高价氧化物对应的水化物溶液(浓度均为0.01mol·L-1)的pH和原子半径、原子序数的关系如图所示。下列说法正确的是
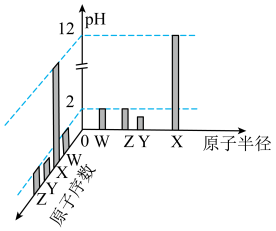

| A.化合物X2Y2中含有极性共价键和非极性共价键 |
| B.简单气态氢化物的热稳定性:Y<W |
| C.简单离子半径:Z>Y>W>X |
| D.非金属性:Y>Z |
您最近一年使用:0次
名校
解题方法
6 . 钛酸钙是最典型的钙钛矿型化合物,该类化合物具有特殊的理化性质。
(1)基态 的核外电子排布式为
的核外电子排布式为____________ 。
(2)钛酸钙的晶胞如下图所示。
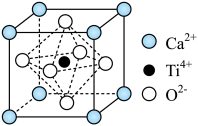
①每个 周围等距且紧邻的
周围等距且紧邻的 有
有______ 个。
②比较 和
和 的离子半径大小并说明理由
的离子半径大小并说明理由____________ 。
(3)钛酸钙的阴、阳离子均可被半径相近的其它离子替代,从而衍生出多种钙钛矿型化合物。
①已知钛酸钙晶胞中距离最近的 和
和 之间的距离为
之间的距离为 ,则钛酸钙晶体密度
,则钛酸钙晶体密度
______  (列出计算式)。
(列出计算式)。
②若忽略离子替代时的体积变化,下列钙钛矿型化合物中,密度大于钛酸钙的是______ (填字母序号)。
a. b.
b.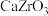 c.
c.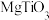
(4)通过离子替代可获得具有优异光电性能的有机钙钛矿型化合物 。其中有机阳离子
。其中有机阳离子 可由甲胺(
可由甲胺( )制得。
)制得。
① 中N的杂化方式为
中N的杂化方式为____________ 。
请从化学键的角度解释由甲胺形成 的过程:
的过程:____________ 。
(1)基态
 的核外电子排布式为
的核外电子排布式为(2)钛酸钙的晶胞如下图所示。

①每个
 周围等距且紧邻的
周围等距且紧邻的 有
有②比较
 和
和 的离子半径大小并说明理由
的离子半径大小并说明理由(3)钛酸钙的阴、阳离子均可被半径相近的其它离子替代,从而衍生出多种钙钛矿型化合物。
①已知钛酸钙晶胞中距离最近的
 和
和 之间的距离为
之间的距离为 ,则钛酸钙晶体密度
,则钛酸钙晶体密度
 (列出计算式)。
(列出计算式)。②若忽略离子替代时的体积变化,下列钙钛矿型化合物中,密度大于钛酸钙的是
a.
 b.
b.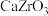 c.
c.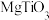
(4)通过离子替代可获得具有优异光电性能的有机钙钛矿型化合物
 。其中有机阳离子
。其中有机阳离子 可由甲胺(
可由甲胺( )制得。
)制得。①
 中N的杂化方式为
中N的杂化方式为请从化学键的角度解释由甲胺形成
 的过程:
的过程:
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
7 . 如图为分子X的结构图,其中A、B、C、D为同一族的元素,B电负性大于D,E与C的价电子数之和与Mg的质子数相同,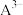 与
与 电子结构相同,工业上利用沸点差异分离出C的单质。下列说法错误的是
电子结构相同,工业上利用沸点差异分离出C的单质。下列说法错误的是

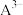 与
与 电子结构相同,工业上利用沸点差异分离出C的单质。下列说法错误的是
电子结构相同,工业上利用沸点差异分离出C的单质。下列说法错误的是
| A.X中A、C的杂化轨道类型相同 | B.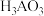 是三元酸 是三元酸 |
| C.原子半径大小:A>E | D.A、B、C、D、E均满足8电子结构 |
您最近一年使用:0次
名校
解题方法
8 . 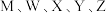 是五种原子序数依次增大的短周期主族元素,其原子序数之和为31;其中Y的最外层电子数等于X的核外电子总数;五种主族元素组成的化合物Q的结构如图所示。下列说法正确的是
是五种原子序数依次增大的短周期主族元素,其原子序数之和为31;其中Y的最外层电子数等于X的核外电子总数;五种主族元素组成的化合物Q的结构如图所示。下列说法正确的是
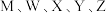 是五种原子序数依次增大的短周期主族元素,其原子序数之和为31;其中Y的最外层电子数等于X的核外电子总数;五种主族元素组成的化合物Q的结构如图所示。下列说法正确的是
是五种原子序数依次增大的短周期主族元素,其原子序数之和为31;其中Y的最外层电子数等于X的核外电子总数;五种主族元素组成的化合物Q的结构如图所示。下列说法正确的是
A.原子半径: |
| B.X的氧化物一定属于酸性氧化物 |
| C.在Q的结构中,所有原子最外层均满足8电子稳定结构 |
| D.Y元素组成的最常见单质和M的单质,在加热条件下生成的化合物中只含离子键 |
您最近一年使用:0次
2023-12-05更新
|
1970次组卷
|
11卷引用:吉林省长春市东北师大附中2023-2024学年高三上学期第三次摸底考试化学科试卷
吉林省长春市东北师大附中2023-2024学年高三上学期第三次摸底考试化学科试卷宁夏回族自治区石嘴山市第三中学2023-2024学年高三上学期第四次月考理综试题福建省泉州市培元中学2023-2024学年高三上学期12月月考化学试题宁夏石嘴山市第三中学2023-2024学年高三上学期第四次月考理科综合试卷湖南省永州市第一中学2023-2024学年高二上学期12月月考化学试题四川省成都市石室中学2023-2024学年高三上学期期末考试理综试题-高中化学(已下线)选择题11-16(已下线)专题04 物质结构与性质-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)黑龙江省大庆市大庆中学2023-2024学年高三下学期开学化学试题陕西省西安中学2023-2024学年高三下学期模拟预测(五)理综试题-高中化学江西省赣州地区2023-2024学年十大教学能手选拔赛高中化学试题
名校
解题方法
9 . 常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物溶液(浓度均为0.01 )的
)的 和原子半径、原子序数的关系如图所示。下列说法错误的是
和原子半径、原子序数的关系如图所示。下列说法错误的是

 )的
)的 和原子半径、原子序数的关系如图所示。下列说法错误的是
和原子半径、原子序数的关系如图所示。下列说法错误的是
A.电负性: |
| B.W和X形成的化合物XW3中含有离子键和共价键 |
C.简单氢化物的沸点: |
D.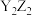 为非极性分子, 为非极性分子, 为极性分子,二者中的Y原子都是 为极性分子,二者中的Y原子都是 杂化 杂化 |
您最近一年使用:0次
10 . X,Y、Z、W、R为原子序数依次增大的前20号主族元素,且分属于四个周期。Y的最外层电子数是电子层数的3倍,Z、W为同周期相邻元素,Y、W可形成如图所示的离子,R原子核外无未成对电子。回答下列问题:
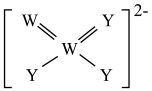
(1)第七周期与Z同族元素的原子序数为___________ 。
(2)Z、W、R简单离子半径由大到小的顺序为___________ (用化学式表示)。
(3)用电子式表示X与R组成的物质的形成过程:___________ 。
(4)Y、W的简单氢化物沸点较高的是___________ (填化学式),判断依据是___________ 。
(5)写出图中离子与稀硫酸反应的离子方程式:___________ 。

(1)第七周期与Z同族元素的原子序数为
(2)Z、W、R简单离子半径由大到小的顺序为
(3)用电子式表示X与R组成的物质的形成过程:
(4)Y、W的简单氢化物沸点较高的是
(5)写出图中离子与稀硫酸反应的离子方程式:
您最近一年使用:0次



