解题方法
1 . 由三种短周期元素组成的盐X,为测定其组成进行如下实验。已知A为金属单质、C为非金属单质,B、C中含有同种元素,F焰色反应呈紫红色。请回答下列问题:
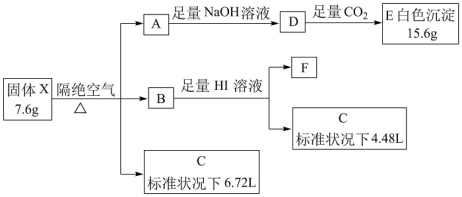
(1)组成X的三种元素是__ (填元素符号),X的化学式为__ 。
(2)固体X能与水反应生成C、E和另一种碱性物质,写出该反应的化学方程式:__ 。
(3)溶液D与过量CO2反应生成E,写出其反应的离子方程式:__ 。
(4)写出X与NH3按物质的量1∶4发生反应的化学方程式:__ 。
(5)物质F是电池工业重要原料,请设计实验方案检验F中的离子:__ 。

(1)组成X的三种元素是
(2)固体X能与水反应生成C、E和另一种碱性物质,写出该反应的化学方程式:
(3)溶液D与过量CO2反应生成E,写出其反应的离子方程式:
(4)写出X与NH3按物质的量1∶4发生反应的化学方程式:
(5)物质F是电池工业重要原料,请设计实验方案检验F中的离子:
您最近一年使用:0次
名校
解题方法
2 . X、Y、Z、M为短周期元素,原子序数依次增大。A~J均由该四种元素构成的单质或化合物,其转化关系如图所示,部分生成物省略。
已知:①A、B、C、G都是由两种元素构成的化合物,其中A、G分子所含的电子数为10e-,B、C分子所含的电子数为18e-;D为空气的主要成分之一、
②另取16.8gJ在真空条件下,控制温度350~400oC加热至完全分解,得到F和8.96L(已折算成标准状况)A两种物质。

请回答下列问题:
(1)写出C的化学式是___________ ;D的电子式是___________ 。
(2)请写出金属单质E在生产生活中的一种作用___________ 。
(3)写出次氯酸钠与过量气体A反应生成B的化学方程式是___________ ;B在制备过程中,气体A需要过量的理由是___________ 。
(4)写出F和G反应生成H和A的化学方程式是___________ 。
(5)B在加热条件下与CuO反应可生成气体D和金属单质,请设计实验方案,验证B与CuO反应后固体的成分(不考虑其他反应)___________ 。
(6)写出J在已知②条件下受热分解的化学方程式是___________ 。
已知:①A、B、C、G都是由两种元素构成的化合物,其中A、G分子所含的电子数为10e-,B、C分子所含的电子数为18e-;D为空气的主要成分之一、
②另取16.8gJ在真空条件下,控制温度350~400oC加热至完全分解,得到F和8.96L(已折算成标准状况)A两种物质。

请回答下列问题:
(1)写出C的化学式是
(2)请写出金属单质E在生产生活中的一种作用
(3)写出次氯酸钠与过量气体A反应生成B的化学方程式是
(4)写出F和G反应生成H和A的化学方程式是
(5)B在加热条件下与CuO反应可生成气体D和金属单质,请设计实验方案,验证B与CuO反应后固体的成分(不考虑其他反应)
(6)写出J在已知②条件下受热分解的化学方程式是
您最近一年使用:0次
2021-11-05更新
|
1081次组卷
|
2卷引用:浙江省诸暨市2018-2019学年高二下学期期末考试化学试题
解题方法
3 . a、b、c、d、e是原子序数依次增大的短周期元素,a的最外层电子数是内层电子数的三倍,上述元素中b原子半径最大,a与e形成的多种化合物中一种可用于自来水消毒杀菌,c、d原子序数为奇数。下列说法正确的是
| A.元素非金属性:a>e |
| B.d、e不能形成各原子均达8e—结构的化合物 |
| C.工业上电解c、e形成的化合物制c的单质 |
| D.a、b、e形成的化合物均呈碱性 |
您最近一年使用:0次
2021-12-11更新
|
599次组卷
|
2卷引用:四川省达州市2021-2022学年高三上学期第一次诊断考试理科综合化学试题
名校
解题方法
4 . M是合成高分子材料聚醚砜的一种单体结构式如图所示,其中短周期主族元素R、X、Y、Z、W的原子序数依次增大,Y、Z位于同主族。下列说法正确的是
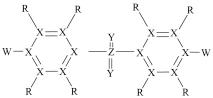

| A.Y元素的最高价态为+6 | B.1molM分子中含有8mol双键结构 |
| C.简单离子结合质子能力:W>Z | D.简单氢化物的稳定性:Y>Z |
您最近一年使用:0次
2022-01-04更新
|
276次组卷
|
2卷引用:江西省大联考2021-2022学年高三上学期12月月考理综化学试题
解题方法
5 . 如图是短周期主族元素电负性与第一电离能的关系。回答下列问题:
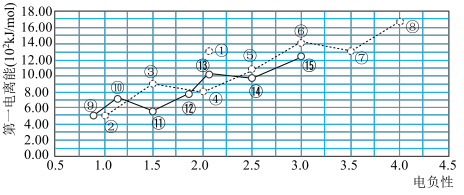
(1)元素③基态原子的电子排布式为___________ ;元素⑪的离子结构示意图为___________ 。
(2)元素①⑤⑧组成的18电子的化合物,其空间构型为___________ 。
(3)元素⑧⑨⑩⑭形成的简单离子,其离子半径由小到大的顺序为___________ (填离子符号),元素⑥⑫⑬形成的简单氢化物,熔沸点由低到高的顺序是___________ (填化学式)。
(4)实验室制备⑮单质的离子方程式为___________ 。
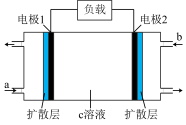
(5)我国研发的新能源汽车燃料电池工作原理如图所示,其中a为元素①与⑤形成的最简单化合物,b为元素⑦的单质,c为元素⑨的最高价氧化物对应水化物,反应后得到元素⑤的最高价含氧酸盐。则电极2上的电极反应式为___________ 。通入标准状况下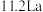 ,测得电路中转移
,测得电路中转移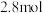 电子,则该电池电能的利用率为
电子,则该电池电能的利用率为___________ 。

(1)元素③基态原子的电子排布式为
(2)元素①⑤⑧组成的18电子的化合物,其空间构型为
(3)元素⑧⑨⑩⑭形成的简单离子,其离子半径由小到大的顺序为
(4)实验室制备⑮单质的离子方程式为
(5)我国研发的新能源汽车燃料电池工作原理如图所示,其中a为元素①与⑤形成的最简单化合物,b为元素⑦的单质,c为元素⑨的最高价氧化物对应水化物,反应后得到元素⑤的最高价含氧酸盐。则电极2上的电极反应式为
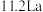 ,测得电路中转移
,测得电路中转移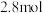 电子,则该电池电能的利用率为
电子,则该电池电能的利用率为
您最近一年使用:0次
解题方法
6 . Ⅰ.颜料是指不溶解、只能以微粒状态分散于粘合剂中的着色剂。颜料混合时的三原色是红、黄、蓝,通过三原色可以调出其他所有颜色。物质A,B,C的溶液颜色类似于这三种颜色。
含铁物质X与HSCN和NaSCN反应得到A(反应①),将固体A置于浓 上方,会逐渐失去9分子结晶水(失重23.51%)。X与含铁物质Y以及KOH反应得到B(反应②),X与HCl反应得到C(反应③),固体C为六水合物,其无水形式可以由单质反应生成。含铁的物质X和Y可以反应生成不溶于水的蓝色物质Z(
上方,会逐渐失去9分子结晶水(失重23.51%)。X与含铁物质Y以及KOH反应得到B(反应②),X与HCl反应得到C(反应③),固体C为六水合物,其无水形式可以由单质反应生成。含铁的物质X和Y可以反应生成不溶于水的蓝色物质Z( ,反应④)。1.000gY可以得到1.327gZ,用相同质量的Y可以得到1.42gB.Y在空气中放置也会生成Z,同时产生剧毒物质(反应⑤)。
,反应④)。1.000gY可以得到1.327gZ,用相同质量的Y可以得到1.42gB.Y在空气中放置也会生成Z,同时产生剧毒物质(反应⑤)。
(1)①推出物质A,B,C,X,Y,Z的化学式,A______ ,B______ ,C______ ,X______ ,Y______ ,Z______
②写出反应①、②、④、⑤的方程式。①______ ,②______ ,④______ ,⑤______
(2)指出物质A、B、C的颜色。A______ ,B______ ,C______ ,
Ⅱ.电子屏幕上千变万化的颜色则是由红、绿、蓝三原色来组成。 、
、 、
、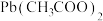 分别经一步反应生成D(青绿色,反应⑥)、E(紫色,反应⑦)、F(黄色,反应⑧)。化合物D,E,F的颜色类似于将红,绿,蓝色的光两两混合后得到。物质D和E为结晶水合物,F为不含氧的二元化合物,其金属元素的质量分数为44.95%。物质D(
分别经一步反应生成D(青绿色,反应⑥)、E(紫色,反应⑦)、F(黄色,反应⑧)。化合物D,E,F的颜色类似于将红,绿,蓝色的光两两混合后得到。物质D和E为结晶水合物,F为不含氧的二元化合物,其金属元素的质量分数为44.95%。物质D(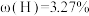 ,
, )的溶液能与银氨溶液发生反应(反应⑨)。物质E为复盐,50g2.50%的E溶液与过量硝酸钡溶液反应,生成1.165g不溶于酸和碱的白色沉淀。
)的溶液能与银氨溶液发生反应(反应⑨)。物质E为复盐,50g2.50%的E溶液与过量硝酸钡溶液反应,生成1.165g不溶于酸和碱的白色沉淀。
(3)①通过计算和推理写出物质D、E、F的化学式。D______ ,E______ ,F______ ,
②写出反应⑨的方程式。______
(4)对物质D,E,F,指出屏幕上是哪两种基本颜色的光可以形成该物质的颜色。______ ,
含铁物质X与HSCN和NaSCN反应得到A(反应①),将固体A置于浓
 上方,会逐渐失去9分子结晶水(失重23.51%)。X与含铁物质Y以及KOH反应得到B(反应②),X与HCl反应得到C(反应③),固体C为六水合物,其无水形式可以由单质反应生成。含铁的物质X和Y可以反应生成不溶于水的蓝色物质Z(
上方,会逐渐失去9分子结晶水(失重23.51%)。X与含铁物质Y以及KOH反应得到B(反应②),X与HCl反应得到C(反应③),固体C为六水合物,其无水形式可以由单质反应生成。含铁的物质X和Y可以反应生成不溶于水的蓝色物质Z( ,反应④)。1.000gY可以得到1.327gZ,用相同质量的Y可以得到1.42gB.Y在空气中放置也会生成Z,同时产生剧毒物质(反应⑤)。
,反应④)。1.000gY可以得到1.327gZ,用相同质量的Y可以得到1.42gB.Y在空气中放置也会生成Z,同时产生剧毒物质(反应⑤)。(1)①推出物质A,B,C,X,Y,Z的化学式,A
②写出反应①、②、④、⑤的方程式。①
(2)指出物质A、B、C的颜色。A
Ⅱ.电子屏幕上千变万化的颜色则是由红、绿、蓝三原色来组成。
 、
、 、
、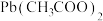 分别经一步反应生成D(青绿色,反应⑥)、E(紫色,反应⑦)、F(黄色,反应⑧)。化合物D,E,F的颜色类似于将红,绿,蓝色的光两两混合后得到。物质D和E为结晶水合物,F为不含氧的二元化合物,其金属元素的质量分数为44.95%。物质D(
分别经一步反应生成D(青绿色,反应⑥)、E(紫色,反应⑦)、F(黄色,反应⑧)。化合物D,E,F的颜色类似于将红,绿,蓝色的光两两混合后得到。物质D和E为结晶水合物,F为不含氧的二元化合物,其金属元素的质量分数为44.95%。物质D(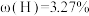 ,
, )的溶液能与银氨溶液发生反应(反应⑨)。物质E为复盐,50g2.50%的E溶液与过量硝酸钡溶液反应,生成1.165g不溶于酸和碱的白色沉淀。
)的溶液能与银氨溶液发生反应(反应⑨)。物质E为复盐,50g2.50%的E溶液与过量硝酸钡溶液反应,生成1.165g不溶于酸和碱的白色沉淀。(3)①通过计算和推理写出物质D、E、F的化学式。D
②写出反应⑨的方程式。
(4)对物质D,E,F,指出屏幕上是哪两种基本颜色的光可以形成该物质的颜色。
您最近一年使用:0次
7 . X是一种有前景的贮氢材料,含有三种短周期元素,高温下加热84gX分解产生0.5mol的离子化合物A和44.8L的气体B(标准状况下),B能使湿润的红色石蕊试纸变蓝,X、A发生水解反应均产生一种白色沉淀和B。
(1)写出B的电子式___________ 。
(2)写出X受热分解的化学方程式___________ 。
(3)B连续氧化可以产生2种常见气体,将这两种氧化物溶于冰水可以得到一种弱酸C,酸性比醋酸略强;向C的钠盐加入某物质也可以得到C,下列不适合使用的是___________。
(4)X在一定条件下能和NaH反应生成H2,计算X材料在该反应中的最大贮氢比________ (贮氢比=氢气质量/贮氢材料质量)。
(5)X能否与Cl2________ 发生反应(填“能”或“不能”),若能,简述理由_________ (若不能,本问不用回答)
(1)写出B的电子式
(2)写出X受热分解的化学方程式
(3)B连续氧化可以产生2种常见气体,将这两种氧化物溶于冰水可以得到一种弱酸C,酸性比醋酸略强;向C的钠盐加入某物质也可以得到C,下列不适合使用的是___________。
| A.SO2 | B.HCl | C.CO2 | D.稀H2SO4 |
(5)X能否与Cl2
您最近一年使用:0次
解题方法
8 . 某离子液体结构如图所示,其中X、Y、Z、M、W均为短周期元素且原子序数依次增大,X是宇宙中最丰富的元素,Z与W同主族,下列说法错误的是


A.氢化物沸点可能 |
B.第一电离能和电负性均有 |
| C.该离子液体中存在配位键和氢键 |
| D.相较于易挥发且有毒的有机溶剂,其更适合做有机合成溶剂 |
您最近一年使用:0次
名校
解题方法
9 . 短周期主族元素X、Y、Z、G、T的原子序数依次增大,Z、G是金属元素且G的氧化物属于两性氧化物,T的原子序数是Y的2倍且T、Y的最低化合价相同。这5种元素的价电子数之和等于20,含Z元素的物质的焰色呈黄色。回答下列问题:
(1)X的最高价氧化物对应水化物的化学式为___________ 。位于元素周期表中s区的元素为___________ (填元素符号)。
(2)Y、Z、G、T的电负性由小到大的顺序为___________ (填元素符号)。
(3) 分子是
分子是___________ (填“极性”或“非极性”)分子。 分子中T的价层电子对数为
分子中T的价层电子对数为___________ 。
(4)Y和Z能形成既含离子键,又含共价键的化合物,其化学式为___________ 。
(5)V是由Y、Z、T组成的化合物,V的水溶液呈中性。则V的阴离子的空间构型___________ 。
(6)T的一种单质的结构如图所示: ,T原子杂化类型是
,T原子杂化类型是________ 。32gT的这种单质含σ键的数目为________ 。这种单质易溶于 ,不溶于水,其原因是
,不溶于水,其原因是_________ 。
(1)X的最高价氧化物对应水化物的化学式为
(2)Y、Z、G、T的电负性由小到大的顺序为
(3)
 分子是
分子是 分子中T的价层电子对数为
分子中T的价层电子对数为(4)Y和Z能形成既含离子键,又含共价键的化合物,其化学式为
(5)V是由Y、Z、T组成的化合物,V的水溶液呈中性。则V的阴离子的空间构型
(6)T的一种单质的结构如图所示:
 ,T原子杂化类型是
,T原子杂化类型是 ,不溶于水,其原因是
,不溶于水,其原因是
您最近一年使用:0次
2023-04-28更新
|
178次组卷
|
3卷引用:江西省南昌市等5地2022-2023学年高二下学期4月期中考试化学试题
解题方法
10 . 化合物甲由两种常见的短周期元素组成,且所有原子均满足8电子稳定结构。某同学用分别 用5.15g甲进行如下两个实验:

其中,气体单质X的水溶液具有漂白性;甲和SO3按上述实验用量恰好完全反应生成乙和丙,其中乙由三种元素组成;混合气Y由两种常见酸性气体丙和丁组成,请回答:
(1)甲的化学式___________ 。
(2)X和丙同时通入水中时发生反应的离子方程式___________ 。
(3)乙和H2O反应生成混合气体Y的化学方程式___________ 。

其中,气体单质X的水溶液具有漂白性;甲和SO3按上述实验用量恰好完全反应生成乙和丙,其中乙由三种元素组成;混合气Y由两种常见酸性气体丙和丁组成,请回答:
(1)甲的化学式
(2)X和丙同时通入水中时发生反应的离子方程式
(3)乙和H2O反应生成混合气体Y的化学方程式
您最近一年使用:0次



