名校
解题方法
1 . X、Y、Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4。请回答下列问题:
(1)Y的元素名称是______ 。
(2)W在周期表中的位置是______ 。
(3)写出化合物Z2R的电子式______ 。
(4)写出化合物X2Y2的结构式______ 。
(5)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是______ (用元素的离子符号表示)。
(6)下列说法能证明非金属性Q强于R的是______ (填序号)。
a.简单阴离子的还原性:Q>R
b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性: Q>R
(7)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是______ 。
(1)Y的元素名称是
(2)W在周期表中的位置是
(3)写出化合物Z2R的电子式
(4)写出化合物X2Y2的结构式
(5)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(6)下列说法能证明非金属性Q强于R的是
a.简单阴离子的还原性:Q>R
b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性: Q>R
(7)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是
您最近一年使用:0次
2021-01-19更新
|
592次组卷
|
5卷引用:辽宁省锦州市2020-2021学年高一上学期期末考试化学试题
2 . 下图为元素周期表的一部分。根据元素①~⑦在周期表中的位置,按要求回答下列问题。
(1)元素①~⑦的单质中氧化性最强的是___________ 。(填化学式)
(2)元素③⑤⑥的原子的半径从大到小的顺序是___________ 。(用元素符号表示)
(3)元素②的简单气态氢化物的沸点高于元素⑥的,原因是___________ 。
(4)元素②④⑦按原子数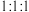 组成化合物甲,甲中所含化学键的类型是
组成化合物甲,甲中所含化学键的类型是___________ 。
(5)元素①与④组成的化合物可与水反应,写出反应的化学方程式___________ 。
(6)元款④⑥⑦的最高价氧化物对应的水化物分别为A、B、C.相同条件下。相同物质的量浓度的A、B、C的水溶液中 最大的是
最大的是___________ 。(填化学式)
(7)元素①与⑦组成的化合物为乙。用电子式表示乙的形成过程___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| ② | ③ | |||||||
| ④ | ⑤ | ⑥ | ⑦ |
(2)元素③⑤⑥的原子的半径从大到小的顺序是
(3)元素②的简单气态氢化物的沸点高于元素⑥的,原因是
(4)元素②④⑦按原子数
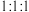 组成化合物甲,甲中所含化学键的类型是
组成化合物甲,甲中所含化学键的类型是(5)元素①与④组成的化合物可与水反应,写出反应的化学方程式
(6)元款④⑥⑦的最高价氧化物对应的水化物分别为A、B、C.相同条件下。相同物质的量浓度的A、B、C的水溶液中
 最大的是
最大的是(7)元素①与⑦组成的化合物为乙。用电子式表示乙的形成过程
您最近一年使用:0次
3 . X、Y、Z、W、R、T都是短周期元素,X的M层有6个电子,Y最外层电子数是次外层电子数的2倍,Z常温下单质为双原子分子,其氢化物M的水溶液呈碱性,W元素最高价为+7价,R单质既能与酸反应,又能与碱反应,T是周期表中原子半径最小的元素。
(1)X、Y、Z、W、R、T的元素符号分别是X:___________ ,Y:___________ ,Z:___________ ,W:___________ ,R:___________ ,T:___________ 。
(2)Y的一种同位素可以测定文物的年代该同位素的符号是___________ ,其与 形成的双原子分子含有的中子数为
形成的双原子分子含有的中子数为___________ 。
(3)Z元素与T元素形成一种离子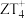 ,写出检验某溶液含有该离子的方法
,写出检验某溶液含有该离子的方法___________ 。
(4)X与W相比,非金属性较强的是W,下列能证明这一事实的是___________ 。
a.常温下W单质与X单质的状态不同
b.W的氢化物比X的氢化物稳定
c.W的最高价氧化物对应的水化物的酸性比X的最高价氧化物对应的水化物酸性强
(1)X、Y、Z、W、R、T的元素符号分别是X:
(2)Y的一种同位素可以测定文物的年代该同位素的符号是
 形成的双原子分子含有的中子数为
形成的双原子分子含有的中子数为(3)Z元素与T元素形成一种离子
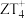 ,写出检验某溶液含有该离子的方法
,写出检验某溶液含有该离子的方法(4)X与W相比,非金属性较强的是W,下列能证明这一事实的是
a.常温下W单质与X单质的状态不同
b.W的氢化物比X的氢化物稳定
c.W的最高价氧化物对应的水化物的酸性比X的最高价氧化物对应的水化物酸性强
您最近一年使用:0次
解题方法
4 . W、X、Y、Z四种短周期元素的原子序数依次增大,W可以与第二周期的四种不同元素结合形成四种不同的10电子的分子,X、Y可形成阴、阳离子个数之比为1:2的两种化合物,其中一种具有强氧化性,Z与X同主族,化合物A、B均由W、X、Y、Z四种元素组成。下列说法错误的是
A.原子半径大小顺序为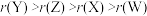 |
| B.W和X、Z均能形成18电子的分子 |
| C.X、Y之间形成的化合物只含离子键 |
| D.A与B之间可以发生反应 |
您最近一年使用:0次
名校
5 . 下表为对部分短周期元素的性质或原子结构的描述。
下列有关说法中正确的是
| 元素编号 | 元素性质或原子结构 |
| T | M层上的电子数是原子核外电子层数的2倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
| A.元素的非金属性:Z>T |
| B.最高价氧化物对应水化物的酸性:X>T |
| C.气态氢化物的热稳定性:X>Y |
| D.Z、T两种元素的原子半径:Z>T |
您最近一年使用:0次
2021-06-21更新
|
782次组卷
|
8卷引用:甘肃省会宁县第一中学2020-2021学年高一下学期期末考试化学试题
解题方法
6 . 短周期主族元素X、Y、Z、W的原子序数依次增大,最外层电子数之和为17,其中X元素形成的单质在自然界中的硬度最大,Z元素的金属性在短周期元素中最强,W单质的水溶液具有酸性和漂白性。下列说法不正确的是
A.原子半径: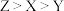 |
| B.Y的最简单气态氢化物的水溶液呈碱性 |
| C.H(氢)、Y、W三种元素形成的化合物中只含有共价键 |
| D.X的最高价氧化物与Z的最高价氧化物能化合生成盐 |
您最近一年使用:0次
解题方法
7 . A、B、C、D四种短周期元素的原子序数依次增大,A的一种核素在考古时常用来鉴定一些文物的年代,B的气态氢化物的水溶液呈碱性;C为金属元素且有两种常见含氧化合物(都含两种元素);若往D单质的水溶液中滴加少量紫色石蕊溶液,可观察到先变红后褪色。下列说法中正确的是
| A.原子半径:D>A>B>C |
| B.简单氢化物的稳定性:A>B |
| C.最高价氧化物对应的水化物的酸性:B>D |
| D.C的两种含氧化合物中阴、阳离子个数比都为1:2 |
您最近一年使用:0次
名校
解题方法
8 . 短周期主族元素X、Y、Z、W的原子序数依次增加,K、L、M均是由这些元素组成的氧化物,甲、乙分别是元素Y、W的单质,甲是常见的固体,乙是常见的气体。K是红棕色气体,丙的浓溶液具有强氧化性,上述物质的转化关系如图所示。下列说法不正确的是( )


| A.Y、Z、W三种元素电负性:W>Z>Y |
| B.Y、Z、W三种元素第一电离能:Z>W>Y |
| C.L的沸点一定比X、Y组成的化合物沸点高 |
| D.由X、Y、Z、W构成的化合物中只能含有共价键 |
您最近一年使用:0次
2020-06-24更新
|
556次组卷
|
6卷引用:山东省德州市宁津县第一中学2019-2020学年高二下学期期末考试化学试题
名校
解题方法
9 . 现有A、B、C、D、E五种元素,它们的质子数依次增多。
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+离子比B3+离子多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于D的下一个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为2:1。试回答:
(1)A元素在周期表中的位置为________ 、E是________ (填元素名称)。
(2)D的单质分子的结构式_______ ,C元素最高价氧化物的水化物的电子式____ 。
(3)写出工业上冶炼B单质的化学方程式_______________ 。
(4)写出CD的溶液中通入氯气的离子方程式________________ 。
(5)比较B、C、E三种元素形成的简单离子氧化性的强弱:(B、C、E离子用实际离子符号表示)氧化性_________ 。
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+离子比B3+离子多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于D的下一个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为2:1。试回答:
(1)A元素在周期表中的位置为
(2)D的单质分子的结构式
(3)写出工业上冶炼B单质的化学方程式
(4)写出CD的溶液中通入氯气的离子方程式
(5)比较B、C、E三种元素形成的简单离子氧化性的强弱:(B、C、E离子用实际离子符号表示)氧化性
您最近一年使用:0次
2020-05-19更新
|
129次组卷
|
3卷引用:湖南省邵东县第一中学2019-2020学年高一下学期期末考试化学试题
16-17高三上·江西南昌·期末
解题方法
10 . W,X,Y,Z四种短周期元素,原子序数依次增大,在周期表中W与X相邻,Y与Z相邻。已知W元素的氢化物与Z元素的氢化物反应只生成一种盐a;X,Y位于同一族,它们能组成YX2,YX3两种常见化合物。请回答下列问题:
(1)X元素位于周期表的位置为_______________ 。
(2)X,Y,Z三种元素形成的单质中,氧化性最弱的是________ (填化学式)。
(3)a溶液的pH____ 7(填“>”、“<”或“=”),用离子方程式解释为:___________ 。
(4)Y与Z可形成共价化合物Y2Z2,分子中Y与Z均满足8电子稳定结构,则Y2Z2的电子式为______ 。Y2Z2遇水很易反应,产生的气体能使品红溶液褪色,则其与水反应的化学方程式为_________ 。
(5)工业上用氧化WH3法制取WO,该反应的热化学方程式为:4WH3(g)+5O2(g)=4WO(g)+6H2O(g)∆H=-905.8kJ/mol;已知W2(g)+O2(g)=2WO(g)∆H=+180kJ/mol,则WH3与氧气反应产生两种无污染物质的热化学方程式为__________________ 。
(1)X元素位于周期表的位置为
(2)X,Y,Z三种元素形成的单质中,氧化性最弱的是
(3)a溶液的pH
(4)Y与Z可形成共价化合物Y2Z2,分子中Y与Z均满足8电子稳定结构,则Y2Z2的电子式为
(5)工业上用氧化WH3法制取WO,该反应的热化学方程式为:4WH3(g)+5O2(g)=4WO(g)+6H2O(g)∆H=-905.8kJ/mol;已知W2(g)+O2(g)=2WO(g)∆H=+180kJ/mol,则WH3与氧气反应产生两种无污染物质的热化学方程式为
您最近一年使用:0次



