1 . 设 表示阿伏加德罗常数的值,下列叙述中正确的是
表示阿伏加德罗常数的值,下列叙述中正确的是
 表示阿伏加德罗常数的值,下列叙述中正确的是
表示阿伏加德罗常数的值,下列叙述中正确的是A. 和 和 的混合物中含 的混合物中含 ,则混合物中质子数为 ,则混合物中质子数为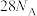 |
B.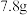 苯分子中,含有碳碳单键的数目为 苯分子中,含有碳碳单键的数目为 |
C.标准状况下, 二氯甲烷( 二氯甲烷( )中含有氯原子的数目为 )中含有氯原子的数目为 |
D.常温下, 的 的 溶液中,由水电离出的 溶液中,由水电离出的 数目为 数目为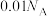 |
您最近半年使用:0次
2 . 石英与焦炭在高温的氮气流中发生反应 可制得高温结构陶瓷氮化硅。
可制得高温结构陶瓷氮化硅。 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 可制得高温结构陶瓷氮化硅。
可制得高温结构陶瓷氮化硅。 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.在20℃和101kPa的条件下,11.2L CO中原子的数目为 |
B.0.05mol  含有中子的数目为0.7 含有中子的数目为0.7 |
C.6g  晶体中含有的Si-O键数目为0.4 晶体中含有的Si-O键数目为0.4 |
D.通过上述反应生成0.05mol  ,电子转移的数目为0.5 ,电子转移的数目为0.5 |
您最近半年使用:0次
名校
3 . 反应 可用于冶金。设
可用于冶金。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 可用于冶金。设
可用于冶金。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.2.0g 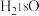 与 与 的混合物中所含质子数与中子数均为 的混合物中所含质子数与中子数均为 |
B.100mL 1 NaCN溶液中阴离子数为0.1 NaCN溶液中阴离子数为0.1 |
C.1mol 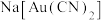 中含 中含 键数目为6 键数目为6 |
D.该反应消耗22.4L  ,转移电子数为4 ,转移电子数为4 |
您最近半年使用:0次
2024-04-21更新
|
315次组卷
|
2卷引用:河北省沧州市沧县中学2023-2024学年高三下学期3月模拟预测化学试题
名校
解题方法
4 . 下列有关化学用语的使用正确的是
A. 的电子式: 的电子式: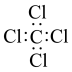 |
B.钠离子结构示意图 |
C.M²⁻核外有a个电子,b个中子,M的原子符号为 |
D.高氯酸的电离方程式 |
您最近半年使用:0次
名校
解题方法
5 . 某天然气电厂对废气回收利用,在催化剂作用下重新合成天然气作为燃料再利用,反应机理如图所示。下列说法错误的是
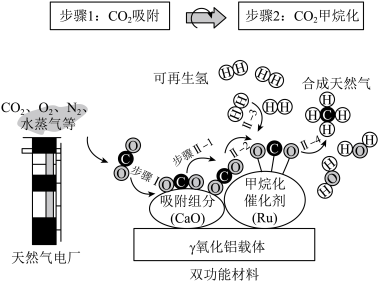
A.步骤 -2中存在极性键的断裂、Ⅱ-3中存在非极性键断裂 -2中存在极性键的断裂、Ⅱ-3中存在非极性键断裂 |
| B.步骤Ⅱ-4存在极性键生成 |
| C.当消耗1molCO2生成1molCH4时,转移8mol电子 |
| D.CO2、N2、CH4分子中各原子均满足8电子稳定结构 |
您最近半年使用:0次
2024-04-03更新
|
220次组卷
|
2卷引用:江西省赣州市兴国中学2023-2024学年高一下学期第一次阶段性考试化学试题
6 . 卢瑟福用α粒子轰击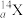 原子,首次用人工实现了核反应:
原子,首次用人工实现了核反应: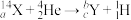 。其中X和Y是原子最外层电子数之和为11的两种短周期元素,下列说法不正确的是
。其中X和Y是原子最外层电子数之和为11的两种短周期元素,下列说法不正确的是
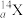 原子,首次用人工实现了核反应:
原子,首次用人工实现了核反应: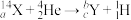 。其中X和Y是原子最外层电子数之和为11的两种短周期元素,下列说法不正确的是
。其中X和Y是原子最外层电子数之和为11的两种短周期元素,下列说法不正确的是| A.原子半径和简单离子半径比较的结果均为X>Y |
| B.Y元素所在主族的各种简单氢化物中,Y的氢化物的沸点和稳定性均最大 |
| C.X元素的最高价氧化物对应的水化物为强酸 |
| D.根据元素非金属性的规律推测,简单离子还原性:X<Y |
您最近半年使用:0次
名校
解题方法
7 . 2021年4月13日,日本政府召开相关阁僚会议,正式决定向海洋排放福岛第一核电站含有对海洋环境有害的核废水,并将核废水主要辐射物质“氚(T)”做成卡通形象,以合理化将放射性核废水排入太平洋的行为,进而引发国内外民众的严重不满。
(1)下列有关氚的说法正确的是

(2)有关 和
和 的说法正确的是
的说法正确的是
(3)已知天然氢元素中:氕,丰度为 、氘,丰度
、氘,丰度 、氚,丰度
、氚,丰度 ;氕、氘、氚原子的质量用
;氕、氘、氚原子的质量用 表示,
表示,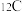 原子的质量用
原子的质量用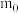 表示.则氢元素的相对原子质量计算表达式
表示.则氢元素的相对原子质量计算表达式_____________ 。
(4) 的质量数常被当作氧元素的近似相对原子质量.这里的“近似”不包括的含义是
的质量数常被当作氧元素的近似相对原子质量.这里的“近似”不包括的含义是
(5)在离子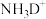 中,电子数、质子数和中子数之比为
中,电子数、质子数和中子数之比为_____________ 。
(6)碳也有一种放射性核素 ,举出一种该核素的应用
,举出一种该核素的应用_____________ 。
(7)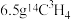 在标况下的体积约为
在标况下的体积约为_____________ 。
(8)一个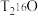 分子的质量是
分子的质量是_____________ (保留3位有效数字)。
(1)下列有关氚的说法正确的是

| A.卡通形象中标“+”号的小球表示中子 | B.氚的核素符号为 |
| C.氚和及其同位素性质完全相同 | D.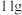 氚水 氚水 所含中子数为 所含中子数为 |
(2)有关
 和
和 的说法正确的是
的说法正确的是 | A.互为同位素 | B.互为同素异形体 |
| C.电子数不同 | D.同温同压下密度之比为 |
(3)已知天然氢元素中:氕,丰度为
 、氘,丰度
、氘,丰度 、氚,丰度
、氚,丰度 ;氕、氘、氚原子的质量用
;氕、氘、氚原子的质量用 表示,
表示,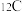 原子的质量用
原子的质量用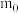 表示.则氢元素的相对原子质量计算表达式
表示.则氢元素的相对原子质量计算表达式(4)
 的质量数常被当作氧元素的近似相对原子质量.这里的“近似”不包括的含义是
的质量数常被当作氧元素的近似相对原子质量.这里的“近似”不包括的含义是 | A.氧的其它同位素的丰度太低,被忽略了 | B.质子和中子的相对质量都很接近于1 |
| C.元素的近似相对原子质量总是取整数 | D.电子的质量太小 |
(5)在离子
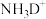 中,电子数、质子数和中子数之比为
中,电子数、质子数和中子数之比为(6)碳也有一种放射性核素
 ,举出一种该核素的应用
,举出一种该核素的应用(7)
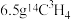 在标况下的体积约为
在标况下的体积约为(8)一个
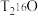 分子的质量是
分子的质量是
您最近半年使用:0次
名校
解题方法
8 . 某化合物由W、X、Y、Z四种前18号元素组成,且原子序数依次增大,X原子的最外层电子数是次外层电子数的3倍,X、Z原子最外层电子数相同;Y元素的负离子核外电子排布和氖原子相同,Y原子的最外层电子数与W原子的核外电子总数相等。
(1)W原子的电子式为_______ ,工业上获得其单质的方法是_______ ;X的离子结构示意图是_______ ,Y的元素名称是_______ 。
(2)Z的元素符号是_______ ,含Z元素的18电子微粒有_______ (写出2种)。
(3)Z单质熔融后加入分散剂,高速搅拌、研磨后离心分离得到上层黄褐色透明分散系,上述过程属于_______ 变化(填“物理”或“化学”),快速鉴定该分散系种类的操作及现象为_______ 。
(4)科学家发现:具有2、8、20、28、50、82、114、126等数目的质子或中子的原子核具有特别的稳定性,并将这些数称为“幻数”,而具有双幻数的 、
、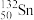 、
、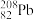 等尤为稳定,写出W、X、Y、Z中质子数为“幻数”的元素的最稳定的核素
等尤为稳定,写出W、X、Y、Z中质子数为“幻数”的元素的最稳定的核素_______ 。
(5)下列关于X、Z及其化合物的说法错误的是_______。
(6)一种含X的化合物名称叫碘酸碘,其中碘元素的化合价有+3和+5价两种,则碘酸碘的化学式应该是_______。
(1)W原子的电子式为
(2)Z的元素符号是
(3)Z单质熔融后加入分散剂,高速搅拌、研磨后离心分离得到上层黄褐色透明分散系,上述过程属于
(4)科学家发现:具有2、8、20、28、50、82、114、126等数目的质子或中子的原子核具有特别的稳定性,并将这些数称为“幻数”,而具有双幻数的
 、
、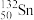 、
、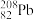 等尤为稳定,写出W、X、Y、Z中质子数为“幻数”的元素的最稳定的核素
等尤为稳定,写出W、X、Y、Z中质子数为“幻数”的元素的最稳定的核素(5)下列关于X、Z及其化合物的说法错误的是_______。
| A.X和Z两元素形成的化合物不止一种 |
| B.X和Z都没有简单正离子 |
| C.H元素和X、Z形成的酸可能是强酸 |
| D.Cu元素和X、Z形成的化合物之一是常见的干燥剂 |
A.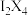 | B.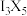 | C.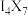 | D.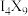 |
您最近半年使用:0次
23-24高三上·上海浦东新·阶段练习
名校
解题方法
9 . 华为Mate 60 Pro手机于2023年8月底发售,它使用了高性能的国产芯片,体现了我国的芯片技术的飞速发展。
Ⅰ.硅在自然界中有三种稳定的核素,相关信息如下:
(1)硅元素的相对原子量为___________ (保留两位小数),12 g SiO2中29Si的质量为___________ (保留两位小数)。
(2)硅与碳化硅(SiC)均可以作为芯片的材料,比较硅与碳化硅的熔点高低,并说明理由___________ 。
(3)下列能说明碳的非金属大于硅的是___________。
Ⅱ.华为Mate 60 Pro手机利用石墨烯薄片液冷散热系统,是全球最强散热手机系统。石墨烯可以看成单层的石墨,它的结构如下:

(4)在石墨烯晶体中,碳原子所形成的六元环数、碳原子数、C-C键数之比为___________ 。
(5)下列关于石墨烯的说法错误的是___________。
Ⅲ.废弃的手机主板中可以提取出Au、Ag等贵金属。主板中的Ag用硝酸溶解后,过滤得到AgNO3溶液,加入NaCl溶液,过滤,向得到固体的加入氨水,得到无色溶液A,A用水合肼( )还原得到银单质,同时生成一种空气中常见的单质。
)还原得到银单质,同时生成一种空气中常见的单质。
已知:水合肼是一种二元弱碱,其电离常数为: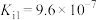 ,
, 。
。
(6)溶液A中含量最高的阳离子的化学式为___________ ,写出水合肼与溶液A反应的离子方程式___________ 。
(7)水合肼在工业上常用作还原剂,广泛用于纳米材料的制备,指出无机制备时水合肼作为还原剂的两个优点___________ 。
(8)写出水合肼一级电离的方程式___________ 。
(9)常温下,向水合肼溶液中加入盐酸,使溶液中的含氮微粒浓度: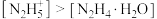 ,需调节的pH范围为
,需调节的pH范围为___________ 。
Ⅰ.硅在自然界中有三种稳定的核素,相关信息如下:
| 核素符号 | 相对原子量 | 丰度(%) |
| 28Si | 27.977 | 92.23 |
| 29Si | 28.976 | 4.67 |
| 30Si | 29.974 | 3.10 |
(2)硅与碳化硅(SiC)均可以作为芯片的材料,比较硅与碳化硅的熔点高低,并说明理由
(3)下列能说明碳的非金属大于硅的是___________。
| A.甲烷的分解温度高于SiH4 | B.碳与SiO2高温下置换出硅 |
| C.二氧化碳通入硅酸钠溶液得到白色沉淀 | D.CH4中氢为+1价,SiH4中氢为-1价 |
Ⅱ.华为Mate 60 Pro手机利用石墨烯薄片液冷散热系统,是全球最强散热手机系统。石墨烯可以看成单层的石墨,它的结构如下:

(4)在石墨烯晶体中,碳原子所形成的六元环数、碳原子数、C-C键数之比为
(5)下列关于石墨烯的说法错误的是___________。
| A.石墨烯是一种多烯烃 |
| B.石墨烯中碳原子与苯环中碳原子杂化类型相同 |
| C.石墨烯与金刚石互为同分异构体 |
| D.石墨烯只存在非极性键 |
Ⅲ.废弃的手机主板中可以提取出Au、Ag等贵金属。主板中的Ag用硝酸溶解后,过滤得到AgNO3溶液,加入NaCl溶液,过滤,向得到固体的加入氨水,得到无色溶液A,A用水合肼(
 )还原得到银单质,同时生成一种空气中常见的单质。
)还原得到银单质,同时生成一种空气中常见的单质。已知:水合肼是一种二元弱碱,其电离常数为:
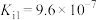 ,
, 。
。(6)溶液A中含量最高的阳离子的化学式为
(7)水合肼在工业上常用作还原剂,广泛用于纳米材料的制备,指出无机制备时水合肼作为还原剂的两个优点
(8)写出水合肼一级电离的方程式
(9)常温下,向水合肼溶液中加入盐酸,使溶液中的含氮微粒浓度:
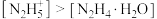 ,需调节的pH范围为
,需调节的pH范围为
您最近半年使用:0次
名校
10 . 日常生活中,佩戴的银饰会逐渐变黑,发生反应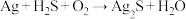 (未配平)。已知
(未配平)。已知 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
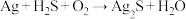 (未配平)。已知
(未配平)。已知 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 分子为直线构型 分子为直线构型 |
B. 中含有的中子数与电子数之比为61∶47 中含有的中子数与电子数之比为61∶47 |
| C.当反应中转移2 mol电子时,被还原的气体体积为11.2 L(标准状况下) |
D.室温下,将0.1 L pH=2的 溶液稀释10倍后,溶液中 溶液稀释10倍后,溶液中 的数目为 的数目为 |
您最近半年使用:0次
2023-06-22更新
|
286次组卷
|
2卷引用:广东省汕尾市2022-2023学年高二下学期学科竞赛化学试题



