解题方法
1 . 各种新型的电池有3000多种,金属常作为电池的电极材料。
(1)关于金属元素在自然界存在情况的叙述,不正确 的是__________ ;
A.金属元素仅存在于矿物中
B.金属元素存在于矿物和动物体内,但植物体内不含
C.少量金属元素以游离态存在,大多数金属元素以化合态存在
D.金属元素不仅存在矿物中,动物和植物体内也存在少量金属元素
(2)30号元素锌常用作电池的电极材料,画出锌的原子结构示意图____________________ ;
(3)碱性锌锰电池是日常生活中消耗量最大的电池,放电时总反应为:Zn+2H2O+2MnO2=Zn(OH)2+2MnOOH。MnOOH中,Mn元素的化合价为__________ ;该电池的负极反应式为______________________ ;若某碱性锌锰电池维持电流强度0.5 A(相当于每秒通过5×10-6mol电子),连续工作80分钟即接近失效。如果制造一节电池所需的锌粉为6 g,则电池失效时仍有__________ %的锌粉未参加反应。
(1)关于金属元素在自然界存在情况的叙述,
A.金属元素仅存在于矿物中
B.金属元素存在于矿物和动物体内,但植物体内不含
C.少量金属元素以游离态存在,大多数金属元素以化合态存在
D.金属元素不仅存在矿物中,动物和植物体内也存在少量金属元素
(2)30号元素锌常用作电池的电极材料,画出锌的原子结构示意图
(3)碱性锌锰电池是日常生活中消耗量最大的电池,放电时总反应为:Zn+2H2O+2MnO2=Zn(OH)2+2MnOOH。MnOOH中,Mn元素的化合价为
您最近一年使用:0次
20-21高一·全国·课时练习
2 . 请在下列问题的横线上填上合适的短周期元素符号:
(1)某元素原子核外最外层电子数是内层电子总数的2倍,该元素可能是___________ 。
(2)某元素原子核外最外层电子数是次外层电子数的2倍,该元素可能是___________ 。
(3)某元素原子核外最外层电子数是内层电子总数的 ,该元素可能是
,该元素可能是___________ 。
(4)某元素原子核外最外层电子数是次外层电子数的 ,该元素可能是
,该元素可能是___________ 。
(1)某元素原子核外最外层电子数是内层电子总数的2倍,该元素可能是
(2)某元素原子核外最外层电子数是次外层电子数的2倍,该元素可能是
(3)某元素原子核外最外层电子数是内层电子总数的
 ,该元素可能是
,该元素可能是(4)某元素原子核外最外层电子数是次外层电子数的
 ,该元素可能是
,该元素可能是
您最近一年使用:0次
名校
解题方法
3 . 请完成下列问题:
(1)画出氯原子结构示意图___ 。
(2)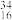 S2-微粒中的质子数是
S2-微粒中的质子数是___ ,中子数是___ 。
(3)49g硫酸的物质的量为___ mol,其完全电离产生H+的个数为___ 。
(4)写出实验室制氯气的离子方程式:___ 。
(1)画出氯原子结构示意图
(2)
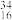 S2-微粒中的质子数是
S2-微粒中的质子数是(3)49g硫酸的物质的量为
(4)写出实验室制氯气的离子方程式:
您最近一年使用:0次
4 . 氢气的生产、存储是氢能应用的核心。目前较成熟的生产、存储路线之一为:利用CH3OH和H2O在某Cu/Zn-Al催化剂存在下生产H2, H2与Mg在一定条件下制得储氢物质X。
回答问题: .
(1) Al在周期表中的位置______________ 。基态Zn的价层电子排布式___________ 。
(2)水分了中氧原子的杂化轨道类型_______________ 。
(3)键能是衡量共价键稳定性的参数之一。 CH3OH键参数中有_________ 种键能数据。CH3OH可以与水以任意比例互溶的原因是___________________ 。
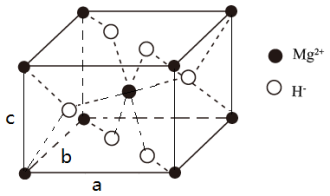
(4) X的晶胞结构如图所示(晶胞参数:α =β =γ=90º,a=b=450.25 pm),密度为1.4g cm-3, H-的配位数为______________ , X的储氢质量分数是______________ ,c= ___________ pm (列出计算式即可)。
回答问题: .
(1) Al在周期表中的位置
(2)水分了中氧原子的杂化轨道类型
(3)键能是衡量共价键稳定性的参数之一。 CH3OH键参数中有
(4) X的晶胞结构如图所示(晶胞参数:α =β =γ=90º,a=b=450.25 pm),密度为1.4g cm-3, H-的配位数为

您最近一年使用:0次
2020-10-12更新
|
4052次组卷
|
5卷引用:2020年海南省高考化学试卷(新高考)
2020年海南省高考化学试卷(新高考)(已下线)2020年海南卷化学高考真题变式题15-19(已下线)难点10 物质结构与性质综合题-2021年高考化学【热点·重点·难点】专练(新高考)(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-练习北京市第一六一中学2021-2022学年高三上学期期中考试化学试题
名校
解题方法
5 . 根据要求填空:
(1)A元素原子的M层电子数是其电子总数的 ,则其原子结构示意图为
,则其原子结构示意图为__ ;其简单离子的电子式为___ 。
(2)下列图示表示同种元素的是___ ;化学性质相似的是___ ;属于离子的是__ 。
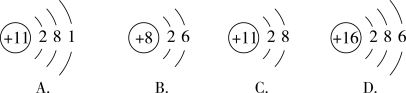
(3)已知Mm+与Nn-具有相同的电子层结构,若N的核电荷数为a,M的质量数为A,则M的中子数为__ ,两者形成的化合物的化学式可能为__ 。
(1)A元素原子的M层电子数是其电子总数的
 ,则其原子结构示意图为
,则其原子结构示意图为(2)下列图示表示同种元素的是
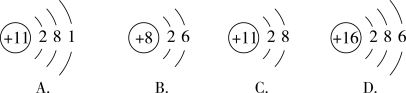
(3)已知Mm+与Nn-具有相同的电子层结构,若N的核电荷数为a,M的质量数为A,则M的中子数为
您最近一年使用:0次
6 . 写出符合下列要求的单原子形成的微粒的结构示意图。
(1)核内有10个质子的原子___ 。
(2)核外有10个电子的一价阴离子___ 。
(3)核外有18个电子的二价阳离子___ 。
(1)核内有10个质子的原子
(2)核外有10个电子的一价阴离子
(3)核外有18个电子的二价阳离子
您最近一年使用:0次
名校
解题方法
7 . 用化学用语回答下列问题
(1)画出钾原子的原子结构示意图:____________ 。
(2)写出氨分子的结构式:__________________ 。
(3)用电子式表示氟化钙(CaF2)的形成过程:_________________ 。
(4)完成下表
(1)画出钾原子的原子结构示意图:
(2)写出氨分子的结构式:
(3)用电子式表示氟化钙(CaF2)的形成过程:
(4)完成下表
| K层为最外层时,最多能容纳的电子数 | |
| 除K层外,其他各层为最外层时,最多能容纳的电子数 | |
| 次外层最多能容纳的电子数 | |
| 倒数第3层最多能容纳的电子数 | |
| 第n层里最多能容纳的电子数 |
您最近一年使用:0次
名校
解题方法
8 . 按要求填空:
(1)在第二周期中(稀有气体除外),第一电离能最大的元素的原子结构示意图是___ ,第一电离能最小的元素的电子排布图为___ 。
(2)以下是一些原子的2p能级和3d能级中电子排布的情况.试判断,哪些违反了泡利不相容原理,哪些违反了洪特规则。
① ②
② ③
③ ④
④ ⑤
⑤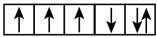 ⑥
⑥
违反泡利不相容原理的有__ ,违反洪特规则的有___ 。
(3)用VSEPR模型和杂化轨道理论相关知识填表:
(1)在第二周期中(稀有气体除外),第一电离能最大的元素的原子结构示意图是
(2)以下是一些原子的2p能级和3d能级中电子排布的情况.试判断,哪些违反了泡利不相容原理,哪些违反了洪特规则。
①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥
违反泡利不相容原理的有
(3)用VSEPR模型和杂化轨道理论相关知识填表:
| 分子或离子 | 中心原子轨道杂化形式 | 分子或离子的立体结构 | 分子有无极性 |
| CH2O | |||
| NH4+ | |||
| CS2 |
您最近一年使用:0次
解题方法
9 . (1)画出下列元素的原子结构示意图。
①核电荷数为13的元素:_______ 。
②最外层电子数等于次外层电子数的元素原子:______ 。
(2)现有粒子:1H、35Cl、2H、14N、2H37Cl,其中:
①有_________ 种元素;
②__________ 之间互称同位素。
①核电荷数为13的元素:
②最外层电子数等于次外层电子数的元素原子:
(2)现有粒子:1H、35Cl、2H、14N、2H37Cl,其中:
①有
②
您最近一年使用:0次
2012·上海浦东新·三模
10 . 硼矿是无机盐工业的重要原料,硼镁石用硫酸分解的反应式为2MgO·B2O3·H2O+2H2SO4→2H3BO3+2MgSO4。
(1)上述反应中,核外电子排布式相同的离子有__ ;原子核外具有五种不同能量电子的元素名称是__ 。
(2)硼元素在元素周期表中的位置是__ ;已知BF3分子的空间构型为平面正三角形,则BF3属于__ 分子(填“极性”或“非极性”)。
(3)Mg元素的原子结构示意图为__ 。Mg(OH)2碱性比Ca(OH)2__ (填“强”或“弱”)。
(4)硼酸[H3BO3或B(OH)3]是一元弱酸,它的水溶液之所以呈弱酸性并非本身电离出H+,而是硼酸与水作用时,与水电离产生的OH-结合,导致溶液中c(H+)>c(OH-)。用离子方程式表示硼酸呈酸性的原因__ 。
(1)上述反应中,核外电子排布式相同的离子有
(2)硼元素在元素周期表中的位置是
(3)Mg元素的原子结构示意图为
(4)硼酸[H3BO3或B(OH)3]是一元弱酸,它的水溶液之所以呈弱酸性并非本身电离出H+,而是硼酸与水作用时,与水电离产生的OH-结合,导致溶液中c(H+)>c(OH-)。用离子方程式表示硼酸呈酸性的原因
您最近一年使用:0次



