名校
解题方法
1 . 前四周期元素A、B、C、D、E原子序数依次增大,其相关性质如表所示:
请根据以上情况,回答下列问题:
(1)E元素基态原子核外有_______ 种能量不同的电子,其价电子排布式为__________ 。
(2)B和C可形成一种同时含有共价键和离子键的化合物,写出此化合物与水反应的化学方程式_______ 。
(3)B、C、D三种元素的简单离子的半径由大到小的顺序为_______ (用离子符号表示)。
(4)A的简单氢化物与最高价氧化物对应的水化物可以发生反应,则生成物中阳离子的结构式为_______ 。
(5)检测元素C的常见方法是____________ 。
| A | 2p能级电子半充满 |
| B | 与A同周期,且原子核外有2个未成对电子 |
| C | 基态原子核外有6个原子轨道排有电子,且只有1个未成对电子 |
| D | 其基态原子外围电子排布式为nsn-1npn+1 |
| E | 前四周期元素中,E元素基态原子未成对电子数最多 |
(1)E元素基态原子核外有
(2)B和C可形成一种同时含有共价键和离子键的化合物,写出此化合物与水反应的化学方程式
(3)B、C、D三种元素的简单离子的半径由大到小的顺序为
(4)A的简单氢化物与最高价氧化物对应的水化物可以发生反应,则生成物中阳离子的结构式为
(5)检测元素C的常见方法是
您最近一年使用:0次
2 . 按要求回答问题。
(1)1 mol HCHO分子中含有σ键的数目为___________ NA。
(2)CS2分子中,共价键的类型有___________ 。
(3)下列物质中:
①MgCl2;②Na2O2; ③CS2 ;④NaOH;⑤H2。
只存在极性键的是___________ (填序号,下同),只存在非极性键的是___________ ,只存在离子键的是___________ ,既存在离子键又存在极性共价键的是___________ ,既存在离子键又存在非极性共价键的是___________ 。
(4)第一电离能比较Mg___________ Al,解释原因___________ 。
(1)1 mol HCHO分子中含有σ键的数目为
(2)CS2分子中,共价键的类型有
(3)下列物质中:
①MgCl2;②Na2O2; ③CS2 ;④NaOH;⑤H2。
只存在极性键的是
(4)第一电离能比较Mg
您最近一年使用:0次
解题方法
3 . 下列物质属于共价化合物的是
A.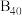 | B.NaOH | C.KF | D. |
您最近一年使用:0次
名校
解题方法
4 .  是一种农业杀虫剂,下列相关说法错误的是
是一种农业杀虫剂,下列相关说法错误的是
 是一种农业杀虫剂,下列相关说法错误的是
是一种农业杀虫剂,下列相关说法错误的是A.该化合物中 的中心原子的杂化轨道类型为 的中心原子的杂化轨道类型为 |
| B.该化合物中存在的化学键有离子键,共价键,配位键和氢键 |
C. 极易溶于 极易溶于 形成氨水,氨水中最多可形成4种氢键 形成氨水,氨水中最多可形成4种氢键 |
D.根据VSEPR模型预测的 的空间结构是正四面体形 的空间结构是正四面体形 |
您最近一年使用:0次
名校
解题方法
5 . 下列各组物质中,都是由极性键构成的极性分子的是
| A.CH4和CCl4 | B.H2S和HCl |
| C.CO2和CS2 | D.NH3和SiO2 |
您最近一年使用:0次
名校
6 . 下列说法中,正确的有
①共价键的成键原子只能是非金属原子
②所有的σ键的强度都比π键的大
③在所有分子中都存在化学键
④碳碳三键和碳碳双键的键能分别是碳碳单键的3倍和2倍
⑤键长等于成键两原子的半径之和
①共价键的成键原子只能是非金属原子
②所有的σ键的强度都比π键的大
③在所有分子中都存在化学键
④碳碳三键和碳碳双键的键能分别是碳碳单键的3倍和2倍
⑤键长等于成键两原子的半径之和
| A.0句 | B.1句 | C.2句 | D.3句 |
您最近一年使用:0次
名校
7 . 以下是中学化学中熟悉的物质:①NH4NO3 ②Cl2 ③HCl ④Na2O2 ⑤MgCl2 ⑥CO2 ⑦AlCl3,请回答下列问题:
(1)只含离子键的是_______ 。
(2)含极性键的离子化合物是_______ 。
(3)由极性键构成的非极性分子的是_______ 。
(4)“神舟”七号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是上述中的______ (填序号),用化学方程式来表示吸收原理:_______ 。
(5)羰基硫(COS)与CO2的结构相似,羰基硫(COS)分子的结构式为_______ 。
(6)NH4NO3中 的空间构型为
的空间构型为_______ 。
(1)只含离子键的是
(2)含极性键的离子化合物是
(3)由极性键构成的非极性分子的是
(4)“神舟”七号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是上述中的
(5)羰基硫(COS)与CO2的结构相似,羰基硫(COS)分子的结构式为
(6)NH4NO3中
 的空间构型为
的空间构型为
您最近一年使用:0次
名校
解题方法
8 . 下列说法中正确的是
①离子化合物中一定有离子键,可能有共价键
②离子化合物熔融状态下都可以导电
③非金属单质中不含离子键,一定只含有共价键
④稳定性:CH4>SiH4,沸点:CH4>SiH4
⑤NaCl 和 HCl 溶于水破坏相同的作用力
⑥非极性键可能存在于非金属单质中,也可能存在于离子化合物或共价化合物中
①离子化合物中一定有离子键,可能有共价键
②离子化合物熔融状态下都可以导电
③非金属单质中不含离子键,一定只含有共价键
④稳定性:CH4>SiH4,沸点:CH4>SiH4
⑤NaCl 和 HCl 溶于水破坏相同的作用力
⑥非极性键可能存在于非金属单质中,也可能存在于离子化合物或共价化合物中
| A.①②⑥ | B.①③④⑥ | C.③④⑤⑥ | D.①④⑤ |
您最近一年使用:0次
名校
解题方法
9 . 过渡金属元素及其化合物的应用广泛,是科学家们进行前沿研究的方向之一、
(1)CuCl的盐酸溶液能够与CO发生反应: 。上述化学方程式中的4种物质含有的化学键类型有
。上述化学方程式中的4种物质含有的化学键类型有___________ 。
A.配位键 B.极性键 C.离子键 D.非极性键 E.氢键 F.金属键
(2) 是一种紫色晶体,其中DMSO为二甲基亚矾,化学式为
是一种紫色晶体,其中DMSO为二甲基亚矾,化学式为 。
。 中C—S—O的键角
中C—S—O的键角___________ (填“大于”“小于”或“等于”) 中C—C—O的键角,理由是
中C—C—O的键角,理由是___________ ;元素S、Cl、O的电负性由大到小的顺序为___________ 。
(3) 溶液与乙二胺(
溶液与乙二胺(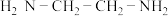 )可形成配离子
)可形成配离子 (En是乙二胺的简写):
(En是乙二胺的简写): 的配位原子为
的配位原子为___________ 。
②乙二胺分子中氮原子轨道的杂化类型为___________ ,乙二胺和三甲胺 均属于胺,但乙二胺比三甲胺的沸点高的多,原因是
均属于胺,但乙二胺比三甲胺的沸点高的多,原因是___________ 。
(1)CuCl的盐酸溶液能够与CO发生反应:
 。上述化学方程式中的4种物质含有的化学键类型有
。上述化学方程式中的4种物质含有的化学键类型有A.配位键 B.极性键 C.离子键 D.非极性键 E.氢键 F.金属键
(2)
 是一种紫色晶体,其中DMSO为二甲基亚矾,化学式为
是一种紫色晶体,其中DMSO为二甲基亚矾,化学式为 。
。 中C—S—O的键角
中C—S—O的键角 中C—C—O的键角,理由是
中C—C—O的键角,理由是(3)
 溶液与乙二胺(
溶液与乙二胺(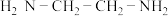 )可形成配离子
)可形成配离子 (En是乙二胺的简写):
(En是乙二胺的简写):
 的配位原子为
的配位原子为②乙二胺分子中氮原子轨道的杂化类型为
 均属于胺,但乙二胺比三甲胺的沸点高的多,原因是
均属于胺,但乙二胺比三甲胺的沸点高的多,原因是
您最近一年使用:0次
10 .  能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。
(1)向 溶液中加入过量
溶液中加入过量 溶液可生成
溶液可生成 。
。
①画出配离子 中的配位键
中的配位键_______________ 。
② 中除了配位键外,还存在的化学键类型有
中除了配位键外,还存在的化学键类型有_____________ (填序号)。
A.离子键 B.金属键 C.极性共价键 D.非极性共价键
(2) 可以与乙二胺
可以与乙二胺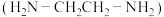 形成配离子:
形成配离子:_____________________ 。
 能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。(1)向
 溶液中加入过量
溶液中加入过量 溶液可生成
溶液可生成 。
。①画出配离子
 中的配位键
中的配位键②
 中除了配位键外,还存在的化学键类型有
中除了配位键外,还存在的化学键类型有A.离子键 B.金属键 C.极性共价键 D.非极性共价键
(2)
 可以与乙二胺
可以与乙二胺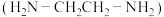 形成配离子:
形成配离子: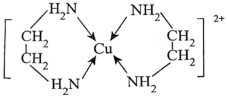
您最近一年使用:0次



