15-16高一下·四川资阳·期末
名校
1 . 下列说法中正确的是
| A.离子键就是使阴、阳离子结合成化合物的静电引力 |
B. 晶体中含共价键,是共价化合物 晶体中含共价键,是共价化合物 |
C.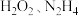 分子中只含有共价键 分子中只含有共价键 |
| D.某化合物在水溶液中能导电,可以证明该化合物内一定存在离子键 |
您最近一年使用:0次
2022-05-23更新
|
238次组卷
|
9卷引用:【2022】【高二上】【期中考】【高中化学】61
(已下线)【2022】【高二上】【期中考】【高中化学】612015-2016学年四川省资阳市高一下学期期末化学试卷四川省自贡市田家炳中学2021届高三上学期开学考试化学试题四川省成都外国语学校2020-2021学年高一下学期第三次(6月)月考化学试题(已下线)第13讲 原子结构 化学键(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)山东师范大学附属中学2021-2022学年高一下学期期中考试(等级考)化学试题浙江省舟山市普陀中学2021-2022学年高一下学期6月月考化学试题(已下线)专题五 元素周期律 能力提升检测卷(测)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第五章 物质结构与性质元素周期律 第29练 化学键 分子的空间结构
解题方法
2 . 1932年美国化学家鲍林首先提出了电负性的概念。电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:
请仔细分析,回答下列有关问题:
(1)预测周期表中电负性最大的元素应为_______ ;估计钙元素的电负性的取值范围:_______ <X<_______ 。
(2)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为_______ 。
(3)请你预测Br与I元素的X数值的大小关系:X(Br)_______ X(I)。
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于_______ 原子(填元素符号)。
(5)根据表中的所给数据分析: 同主族内的不同元素的X值变化的规律是_______ ;
(6)化合物NaH能与水反应产生氢气,所以可用做生氢剂,写出该反应的化学方程式:_______ 。
(7)下列表述中,不能证明氯的非金属性比硫强的是_______ 。
A.气态氢化物的稳定性:HCl>H2S
B.两元素的电负性:S<Cl
C.最高价含氧酸的酸性:HClO4>H2SO4
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应:Cl2+H2S=2HCl+S↓
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
(1)预测周期表中电负性最大的元素应为
(2)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为
(3)请你预测Br与I元素的X数值的大小关系:X(Br)
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于
(5)根据表中的所给数据分析: 同主族内的不同元素的X值变化的规律是
(6)化合物NaH能与水反应产生氢气,所以可用做生氢剂,写出该反应的化学方程式:
(7)下列表述中,不能证明氯的非金属性比硫强的是
A.气态氢化物的稳定性:HCl>H2S
B.两元素的电负性:S<Cl
C.最高价含氧酸的酸性:HClO4>H2SO4
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应:Cl2+H2S=2HCl+S↓
您最近一年使用:0次
22-23高三上·黑龙江双鸭山·阶段练习
名校
解题方法
3 . 下列叙述中正确的是
| A.某物质熔融状态能导电,可以证明该物质内一定存在离子键 |
| B.单质分子中一定含有非极性共价键 |
| C.离子键就是使阴阳离子结合成化合物的静电引力 |
| D.共价化合物中,一定存在极性共价键,可能存在非极性键,一定不存在离子键 |
您最近一年使用:0次
2022-11-19更新
|
453次组卷
|
4卷引用:专题02 分子结构与性质(知识串讲+专题过关)-2022-2023学年高二化学下学期期中期末考点大串讲(人教版2019)
(已下线)专题02 分子结构与性质(知识串讲+专题过关)-2022-2023学年高二化学下学期期中期末考点大串讲(人教版2019)甘肃省兰州第一中学2022-2023学年高二下学期4月期中考试化学试题黑龙江省双鸭山市第一中学2022-2023学年高三10月月考化学试题甘肃省兰州市西北师范大学附属中学2022-2023学年高三上学期期中考试化学试题
名校
解题方法
4 . 下表是元素周期表的一部分,用化学用语回答下列有关问题:
(1)写出下列元素符号:①_______ ,画出原子的结构示意图:④_______ 。
(2)在①—⑫元素中,金属性最强的元素与⑦元素形成化合物中化学键是_______ 。
(3)元素⑦与元素⑧相比,非金属性较强的是_______ (用元素符号表示),下列表述中能证明这一事实的是_______ 。
a.常温下⑦的单质和⑧的单质状态不同
b.③的氢化物比⑦的氢化物稳定
c.一定条件下⑦和③的单质都能与氢氧化钠溶液反应
(4)第三周期中原子半径最大的元素跟它同周期原子半径最小的元素可以形成_______ (填“离子”或“共价”)化合物,用电子式表示其形成过程:_______ 。①的+4价氧化物被烧碱溶液吸收生成两种钠盐的离子方程是_______ 。
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,它可与⑧形成一种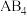 型化合物,请写出该化合物的电子式:
型化合物,请写出该化合物的电子式:_______ 。
(6) 在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成
在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成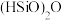 等,写出该反应的化学方程式
等,写出该反应的化学方程式_______ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ⑧ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)在①—⑫元素中,金属性最强的元素与⑦元素形成化合物中化学键是
(3)元素⑦与元素⑧相比,非金属性较强的是
a.常温下⑦的单质和⑧的单质状态不同
b.③的氢化物比⑦的氢化物稳定
c.一定条件下⑦和③的单质都能与氢氧化钠溶液反应
(4)第三周期中原子半径最大的元素跟它同周期原子半径最小的元素可以形成
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,它可与⑧形成一种
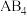 型化合物,请写出该化合物的电子式:
型化合物,请写出该化合物的电子式:(6)
 在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成
在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成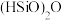 等,写出该反应的化学方程式
等,写出该反应的化学方程式
您最近一年使用:0次
名校
5 . X、Y、Z、M、W、Q、R是7种短周期元素,其性质如下:
完成下列填空:
(1)上述元素中,X在周期表中的位置是__ ,由Y、Q形成的简单离子半径大小关系是Y___ Q(填“>”或“<”)。
(2)由W或Q与R两种元素组成的微粒中,都是10e-体参与的离子反应方程式为___ ,是18e-分子的有__ 种。
(3)写出证明Z、M非金属性强弱的化学方程式为__ 。
(4)Z、W、Q、R四种元素按原子个数比为1:1:4:5形成某化合物,则该化合物中化学键类型为___ 。(填选项)
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
| 元素代号 | X | Y | Z | M | W | Q | R |
| 原子半径/nm | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 | ||
| 主要化合价 | +3 | +6,﹣2 | +7,﹣1 | +5,﹣3 | ﹣2 | ||
| 其它 | 焰色为黄色 | 形成气体单质密度最小 |
(1)上述元素中,X在周期表中的位置是
(2)由W或Q与R两种元素组成的微粒中,都是10e-体参与的离子反应方程式为
(3)写出证明Z、M非金属性强弱的化学方程式为
(4)Z、W、Q、R四种元素按原子个数比为1:1:4:5形成某化合物,则该化合物中化学键类型为
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
您最近一年使用:0次
2020-11-14更新
|
149次组卷
|
2卷引用:福建省莆田第七中学2020-2021学年高二下学期期中考试化学(A卷)试题
名校
解题方法
6 . 价类二维图是学习化学的一种有效归纳方法,关于下图中所涉及物质的说法或推断错误的是
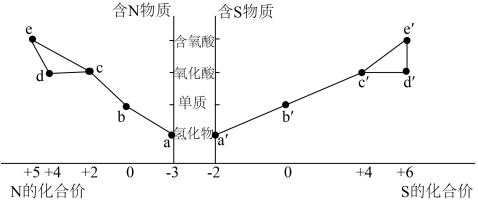
A.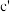 是一种常用的食品添加剂,应合理使用 是一种常用的食品添加剂,应合理使用 |
| B.物质a、c、d全属于非电解质 |
C.液态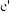 比较粘稠,是因为分子间有氢键 比较粘稠,是因为分子间有氢键 |
| D.a和e反应得到的白色固体中只有极性键 |
您最近一年使用:0次
2024-04-05更新
|
210次组卷
|
2卷引用:湖北省云学名校联盟2023-2024学年高二下学期3月联考化学试卷
名校
解题方法
7 . 侯德榜联合制碱法的原理之一是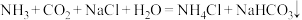 ,下列关于该原理涉及到的物质说法正确的是
,下列关于该原理涉及到的物质说法正确的是
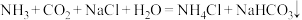 ,下列关于该原理涉及到的物质说法正确的是
,下列关于该原理涉及到的物质说法正确的是A. 晶体中只存在离子键 晶体中只存在离子键 | B. 分子中存在非极性共价键 分子中存在非极性共价键 |
C. 分子中碳原子采取 分子中碳原子采取 杂化 杂化 | D. 分子的空间结构是三角锥形 分子的空间结构是三角锥形 |
您最近一年使用:0次
名校
解题方法
8 . HCHO(g)与O2在催化剂羟基磷灰石(简写为HAP)表面催化生成CO2(g)和H2O(g)的历程示意图如下。下列说法错误的是
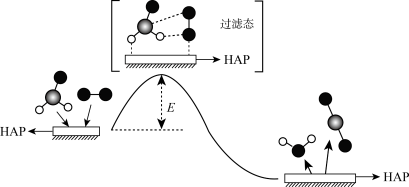

| A.CO2分子的分子空间构型为直线形 |
| B.羟基磷灰石(HAP)的作用是加快反应速率 |
| C.HCHO和H2O分子的VSEPR模型都是四面体形 |
| D.该反应过程既有极性共价键的断裂,也有非极性共价键的断裂 |
您最近一年使用:0次
解题方法
9 . 由X、Y转化为M的反应历程如图所示,下列说法错误的


| A.①→②的总过程放热 | B.催化剂使反应的 降低 降低 |
| C.反应过程中有C-C键形成 | D.M是 |
您最近一年使用:0次
10 . 下列说法中错误的是
| A.根据对角线规则,B和Si的性质具有相似性 |
| B.电负性越大的原子,对键合电子的吸引力越大 |
C.气体单质分子中,一定含有 键 键 |
| D.金属焰色试验的原理是电子跃迁释放能量 |
您最近一年使用:0次



