名校
解题方法
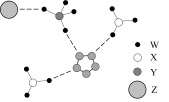
1 . 我国科学家成功合成了世界上首个五氮阴离子盐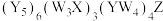 ,X射线衍射测得该化合物的晶体结构局部如图所示。其中Y为氮原子,W与X、W与Y均可形成10电子化合物,Z与其他原子均不同族,且Z的单质可以用于自来水消毒,图中虚线表示氢键。下列说法正确的是
,X射线衍射测得该化合物的晶体结构局部如图所示。其中Y为氮原子,W与X、W与Y均可形成10电子化合物,Z与其他原子均不同族,且Z的单质可以用于自来水消毒,图中虚线表示氢键。下列说法正确的是
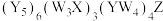 ,X射线衍射测得该化合物的晶体结构局部如图所示。其中Y为氮原子,W与X、W与Y均可形成10电子化合物,Z与其他原子均不同族,且Z的单质可以用于自来水消毒,图中虚线表示氢键。下列说法正确的是
,X射线衍射测得该化合物的晶体结构局部如图所示。其中Y为氮原子,W与X、W与Y均可形成10电子化合物,Z与其他原子均不同族,且Z的单质可以用于自来水消毒,图中虚线表示氢键。下列说法正确的是
| A.该部分结构中共有两种氢键 |
B.若 的立体结构是平面五元环,则阴离子 的立体结构是平面五元环,则阴离子 中的键型为氮氮单键 中的键型为氮氮单键 |
| C.该化合物只存在共价键、氢键和配位键三种作用力 |
| D.该化合物中两种阳离子的空间构型分别为正四面体形和三角锥形 |
您最近一年使用:0次
2 . W、X、Y、Z为族序数依次增大的前四周期主族元素,Y、Z、X、W的原子序数依次增大,它们分别能形成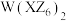 、
、 等化合物,这四种化合物中W、X、Y、Z的化合价不变,且均为它们的最高正价或最低负价,其中Y显-2价。下列叙述正确的是
等化合物,这四种化合物中W、X、Y、Z的化合价不变,且均为它们的最高正价或最低负价,其中Y显-2价。下列叙述正确的是
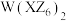 、
、 等化合物,这四种化合物中W、X、Y、Z的化合价不变,且均为它们的最高正价或最低负价,其中Y显-2价。下列叙述正确的是
等化合物,这四种化合物中W、X、Y、Z的化合价不变,且均为它们的最高正价或最低负价,其中Y显-2价。下列叙述正确的是A.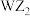 含有共价键 含有共价键 | B.原子半径:W>Z>Y>X |
| C.最简单氢化物的沸点:Y>Z>X | D.X元素最高价氧化物对应的水化物为强酸 |
您最近一年使用:0次
名校
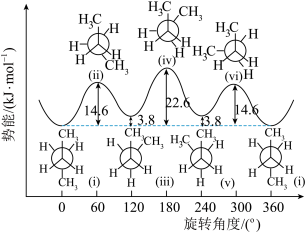
3 . 由单键旋转而产生的异构体称为构象异构体,将正丁烷分子中的 和
和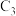 旋转不同的角度可以得到正丁烷的构象势能关系图。下列说法正确的是
旋转不同的角度可以得到正丁烷的构象势能关系图。下列说法正确的是
 和
和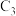 旋转不同的角度可以得到正丁烷的构象势能关系图。下列说法正确的是
旋转不同的角度可以得到正丁烷的构象势能关系图。下列说法正确的是
| A.正丁烷的构象异构体中占比最大的是iv |
| B.原子或基团之间的排斥作用决定了构象异构体的稳定性 |
| C.相同条件下,i转化成iii的速率比逆向转化慢 |
| D.构象异构体间的转化存在化学键的断裂和生成 |
您最近一年使用:0次
4 . 提纯粗硅时可通过反应SiHCl3+H2 Si+3HCl获取晶体硅。下列说法正确的是
Si+3HCl获取晶体硅。下列说法正确的是
 Si+3HCl获取晶体硅。下列说法正确的是
Si+3HCl获取晶体硅。下列说法正确的是| A.1molSi晶体中含有4mol非极性键 |
| B.Si原子的核外有5种不同空间运动状态的电子 |
C.SiHCl3的空间填充模型为 |
| D.硅晶体中1个Si-Si键被6个六元环共用 |
您最近一年使用:0次
名校
5 . 下列有关化学键说法正确的是
| A.化学键是一种作用力,所有的物质都通过化学键形成 |
| B.金属原子和非金属原子间可能形成共价键,非金属元素间也能够形成离子键 |
| C.液态HCl吸热变成HCl气体的过程中有极性键断裂 |
D.硫酸溶于水完全电离成H+和SO ,说明硫酸分子由H+和SO ,说明硫酸分子由H+和SO 组成 组成 |
您最近一年使用:0次
解题方法
6 . 按要求完成下列填空:
(1)将符合的物质进行分类(填字母):
A.石墨和C60 B. 、
、 和
和 C.
C.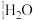 和
和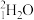 D.H2和D2
D.H2和D2
E.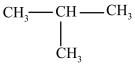 和CH3CH2CH2CH3 F.CH4与CH3CH2CH3
和CH3CH2CH2CH3 F.CH4与CH3CH2CH3
G.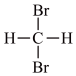 与
与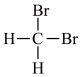
互为同位素___________ ,互为同素异体___________ ,互为同分异构体___________ ,互为同系物的是___________ 。
(2)在下列固体中:
A.CaCl2 B.KOH C.He D.H2SO4 E.NH4Cl F.晶体硅
①其中不含化学键的物质是___________ (填字母)。
②既含有离子键又含有共价键的物质是___________ 。
③只含有共价键的物质是___________ 。
(3)在标准状态下,某气态烃的密度是1.34g/L,将0.1mol该气体充分燃烧生成能得到8.8gCO2和5.4gH2O,试确定该气体的分子式___________ 。(写出计算过程)
(1)将符合的物质进行分类(填字母):
A.石墨和C60 B.
 、
、 和
和 C.
C.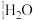 和
和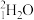 D.H2和D2
D.H2和D2E.
 和CH3CH2CH2CH3 F.CH4与CH3CH2CH3
和CH3CH2CH2CH3 F.CH4与CH3CH2CH3G.
 与
与
互为同位素
(2)在下列固体中:
A.CaCl2 B.KOH C.He D.H2SO4 E.NH4Cl F.晶体硅
①其中不含化学键的物质是
②既含有离子键又含有共价键的物质是
③只含有共价键的物质是
(3)在标准状态下,某气态烃的密度是1.34g/L,将0.1mol该气体充分燃烧生成能得到8.8gCO2和5.4gH2O,试确定该气体的分子式
您最近一年使用:0次
名校
解题方法
7 . 孔雀石是一种碳酸盐矿物,主要成分为Cu2(OH)2CO3,其形成过程的主要化学方程式为2CuSO4+2CaCO3+H2O= Cu2(OH)2CO3+2CaSO4+CO2↑。NA是阿伏加德罗常数的值,下列说法正确的是
| A.0.1mol/L的CuSO4溶液中所含Cu2+的数目小于0.1NA |
| B.常温常压下,18gH2O中所含共用电子对的数目为2NA |
C.1molCaCO3晶体中所含 的数目小于NA 的数目小于NA |
| D.44gCO2溶于水所得溶液中所含H2CO3分子的数目为NA |
您最近一年使用:0次
名校
解题方法
8 . 价类二维图是学习化学的一种有效归纳方法,关于下图中所涉及物质的说法或推断错误的是
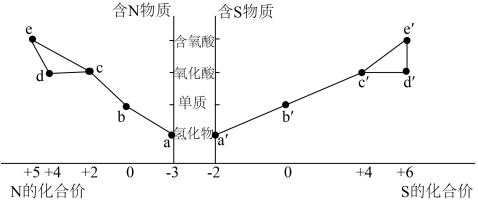
A.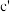 是一种常用的食品添加剂,应合理使用 是一种常用的食品添加剂,应合理使用 |
| B.物质a、c、d全属于非电解质 |
C.液态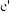 比较粘稠,是因为分子间有氢键 比较粘稠,是因为分子间有氢键 |
| D.a和e反应得到的白色固体中只有极性键 |
您最近一年使用:0次
2024-04-05更新
|
210次组卷
|
2卷引用:湖北省云学名校联盟2023-2024学年高二下学期3月联考化学试卷
名校
9 . 1869年门捷列夫提出元素周期表,根据元素周期表和周期律,回答问题。
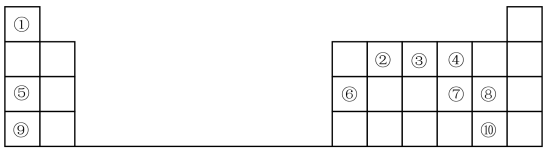
(1)元素⑦在周期表中的位置_______ 。
(2)元素①和⑤形成的化合物中化学键类型是_______ 。
(3)在①~⑧元素中,原子半径最大的是_______ (填元素名称);其某种氧化物可用于潜水艇中的供氧剂,该氧化物中阴离子与阳离子个数比为_______ 。
(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是_______ (用离子符号表示),元素⑨的最高价氧化物对应水化物与元素⑥的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(5)元素的非金属性⑩_______ ⑧(填“>”或“<”);下列事实不能证明上述结论的是_______ 。
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的氢化物的还原性比元素⑩的弱
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
E.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
(6)⑤的最高价氧化物对应的水化物的电子式为_______ ,用电子式表示氯化钠的形成过程_______ 。

(1)元素⑦在周期表中的位置
(2)元素①和⑤形成的化合物中化学键类型是
(3)在①~⑧元素中,原子半径最大的是
(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是
(5)元素的非金属性⑩
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的氢化物的还原性比元素⑩的弱
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
E.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
(6)⑤的最高价氧化物对应的水化物的电子式为
您最近一年使用:0次
名校
解题方法
10 . 现有下列9种物质:① ;②
;② ;③HCl;④
;③HCl;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ ;⑧
;⑧ ;⑨
;⑨ ;按要求填空(填序号)。
;按要求填空(填序号)。
(1)只由离子键构成的物质是_____________ 。
(2)由极性键和非极性键构成的物质是_____________ 。
(3)由离子键和非极性键构成的物质是__________________________ 。
(4)属于共价化合物的物质是_____________ 。
(5)③溶于水时破坏_____________ (填离子键或共价键,下同),⑥熔化时破坏_____________ 。
(6)向⑥的溶液中滴加少量⑧的溶液,反应的离子方程式为_____________________ 。
 ;②
;② ;③HCl;④
;③HCl;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ ;⑧
;⑧ ;⑨
;⑨ ;按要求填空(填序号)。
;按要求填空(填序号)。(1)只由离子键构成的物质是
(2)由极性键和非极性键构成的物质是
(3)由离子键和非极性键构成的物质是
(4)属于共价化合物的物质是
(5)③溶于水时破坏
(6)向⑥的溶液中滴加少量⑧的溶液,反应的离子方程式为
您最近一年使用:0次



