名校
解题方法
1 . 下列说法不正确的是
| A.离子化合物和金属单质的构成粒子中均含有阳离子 |
| B.离子键和金属键本质上都是静电作用,都没有方向性和饱和性 |
| C.熔点:MgO>NaCl>Hg>HBr |
| D.NaHSO4在水溶液中和熔融状态下都能导电,电离方程式相同 |
您最近一年使用:0次
2023-12-30更新
|
263次组卷
|
4卷引用:北京市第一○一中学2021-2022学年高二下学期期末考试化学试卷
北京市第一○一中学2021-2022学年高二下学期期末考试化学试卷(已下线)题型突破05 结构化学基本概念和图示题-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(北京专用)(已下线)3.3.1 金属晶体 离子晶体(提高)福建省三明市第一中学2023-2024学年高二下学期3月月考化学试题
2 . 碘酸碘的化学式可写成: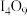 ,已知碘和氯有相似的化学性质。下列有关说法错误的是
,已知碘和氯有相似的化学性质。下列有关说法错误的是
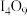 ,已知碘和氯有相似的化学性质。下列有关说法错误的是
,已知碘和氯有相似的化学性质。下列有关说法错误的是A.碘酸碘中碘的化合价是 和 和 |
B.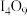 是共价化合物 是共价化合物 |
C.用醋酸和淀粉 溶液可检验加碘盐中的 溶液可检验加碘盐中的 |
D.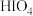 为碘元素的最高价氧化物对应水化物 为碘元素的最高价氧化物对应水化物 |
您最近一年使用:0次
2023-03-10更新
|
264次组卷
|
4卷引用:山东省济宁市2022-2023学年高一上学期期末考试化学试题
山东省济宁市2022-2023学年高一上学期期末考试化学试题山东省济宁市2022-2023学年高一上学期2月期末化学试题(已下线)专项02 离子反应和氧化还原反应的应用-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)山东省济宁市2022-2023学年高一下学期开学考试(上学期期末)化学试题
名校
解题方法
3 . 84 消毒液主要是以次氯酸钠为主要成分的消毒剂,疫情期间,很多人在家里面备上了一些消毒液,方便给家里消毒。84 消毒液制备所需原料可由 NaCl 制备,相关的反应如下图所示,请填写下列空白。
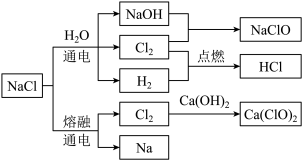
(1)NaClO 含有的化学键类型是_______ ;
(2)氯化钠溶液通电后,发生反应的化学反应方程式为_______ ;
(3)氢气在氯气中燃烧的现象是_______ ;
(4)请写出 Cl2与NaOH反应的化学方程式,并标出电子转移的方向和数目_______ ;
(5)Cl2 与 Ca(OH)2 反应可制备漂白粉,请用化学用语说明原理_______ 。

(1)NaClO 含有的化学键类型是
(2)氯化钠溶液通电后,发生反应的化学反应方程式为
(3)氢气在氯气中燃烧的现象是
(4)请写出 Cl2与NaOH反应的化学方程式,并标出电子转移的方向和数目
(5)Cl2 与 Ca(OH)2 反应可制备漂白粉,请用化学用语说明原理
您最近一年使用:0次
4 . 下列说法正确的是
A.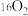 和 和 互为同位素 互为同位素 |
B. 分子的电子式为 分子的电子式为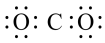 ,每个原子都达到了8电子稳定结构 ,每个原子都达到了8电子稳定结构 |
C.以钙离子撞击锎(Cf)靶,反应可表示为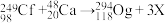 ,则X应为中子 ,则X应为中子 |
D. 与 与 反应生成 反应生成 ,该反应过程中有共价键断裂,同时有共价键和离子键形成 ,该反应过程中有共价键断裂,同时有共价键和离子键形成 |
您最近一年使用:0次
2023-01-04更新
|
838次组卷
|
4卷引用:辽宁省辽南协作体2022-2023学年高一上学期期末考试化学试题
5 . 下表列出了①~⑦共7种元素在元素周期表中的位置。
回答下列问题:
(1)①可以形成原子空间排列方式不同的多种单质,这些不同的单质之间互称为_______ 。
(2)②形成的单质的电子式为_______ 。
(3)⑤的单质在工业上常用于冶炼熔点较高的金属,如用 冶炼
冶炼 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(4)③⑤⑦三种元素的简单离子半径由大到小的顺序是_______ (填离子符号)。
(5)④的单质在③的单质中燃烧形成的化学键有_______ 、_______ 。
(6)根据元素周期律,②的非金属性比⑥强,但②的单质却比⑥的单质稳定,原因是_______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ |
(1)①可以形成原子空间排列方式不同的多种单质,这些不同的单质之间互称为
(2)②形成的单质的电子式为
(3)⑤的单质在工业上常用于冶炼熔点较高的金属,如用
 冶炼
冶炼 ,该反应的化学方程式为
,该反应的化学方程式为(4)③⑤⑦三种元素的简单离子半径由大到小的顺序是
(5)④的单质在③的单质中燃烧形成的化学键有
(6)根据元素周期律,②的非金属性比⑥强,但②的单质却比⑥的单质稳定,原因是
您最近一年使用:0次
名校
解题方法
6 . 推广氢燃料电池汽车有利于实现“碳中和”的宏伟目标,2022年2月北京冬奥会基本实现100%绿电供应。回答下列有关问题:
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。氢气燃烧时断裂的化学键是_______ (填“离子键”或“共价键”),若断开1mol氢气中的化学键消耗的能量为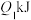 ,断开1mol氧气中的化学键消耗的能量为
,断开1mol氧气中的化学键消耗的能量为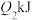 ,形成1mol水中的化学键释放的能量为
,形成1mol水中的化学键释放的能量为 ,则
,则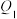 、
、 、
、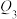 之间的关系为
之间的关系为_______ 。
(2)利用 和
和 在光催化酶作用下可以高效合成甲醇(
在光催化酶作用下可以高效合成甲醇( )。
)。
①甲醇燃烧属于_______ (填“吸热”或“放热”)反应。
②氢气燃料电池在北京冬奥会上得到广泛应用。下图是酸性氢气燃料电池的工作原理示意图:
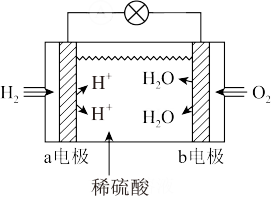
a电极是原电池的_______ (填“正极”或“负极”),该极的电极反应式为_______ ;b电极发生反应_______ (填“氧化”或“还原”);外电路中电子流入的是_______ (填“a”或“b”)电极。
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大量的热。氢气燃烧时断裂的化学键是
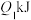 ,断开1mol氧气中的化学键消耗的能量为
,断开1mol氧气中的化学键消耗的能量为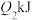 ,形成1mol水中的化学键释放的能量为
,形成1mol水中的化学键释放的能量为 ,则
,则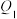 、
、 、
、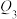 之间的关系为
之间的关系为(2)利用
 和
和 在光催化酶作用下可以高效合成甲醇(
在光催化酶作用下可以高效合成甲醇( )。
)。①甲醇燃烧属于
②氢气燃料电池在北京冬奥会上得到广泛应用。下图是酸性氢气燃料电池的工作原理示意图:

a电极是原电池的
您最近一年使用:0次
2022-07-04更新
|
230次组卷
|
2卷引用:吉林省长春外国语学校2021-2022学年高一下学期期末考试化学试题
解题方法
7 . 已知a、b、c、d是元素周期表中前20号主族元素,其中a是地壳中含量最多的元素,b是元素周期表中非金属性最强的元素,c是短周期中原子半径最大的元素,d原子的N层电子数与K层电子数相等。下列说法正确的是
| A.a、b、c、d形成的简单离子都是10电子微粒 |
B.一定条件下,1molc单质与足量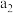 充分反应,转移电子数不一定是 充分反应,转移电子数不一定是 |
| C.与d元素同主族且位于下一周的元素原子序数为38 |
| D.b元素和d元素形成的化合物既含离子键又含共价键 |
您最近一年使用:0次
名校
8 . 锡烯的结构与石墨烯结构相似,其俯视图、侧视图如图所示。已知锡烯的导电性只存在于材料的边缘或表面,随着锡烯层数的增加,显示出超导性。下列说法正确的是


A.SnO2+2C Sn+2CO↑,说明金属性Sn>C Sn+2CO↑,说明金属性Sn>C |
| B.锡烯中的Sn与石墨烯中的C的杂化方式相同 |
| C.锡烯层内存在金属键,层间不存在金属键 |
| D.Sn最外层电子逐级电离能存在关系:I5/I4≫ I4/I3 |
您最近一年使用:0次
2022-05-27更新
|
1085次组卷
|
5卷引用:黑龙江省双鸭山市第一中学2021-2022学年高二下学期期末考试化学试题
黑龙江省双鸭山市第一中学2021-2022学年高二下学期期末考试化学试题湖北省黄冈中学2022届高三第三次模拟考试化学试题(已下线)专题06 物质结构元素周期律-三年(2020-2022)高考真题分项汇编新疆克孜勒苏柯尔克孜自治州阿合奇县2022-2023学年高三上学期11月期中考试化学试题山西省晋中市祁县中学2022-2023学年高三上学期10月月考化学试题
9 . 设NA为阿伏加德罗常数的值。下列关于C、Si及其化合物的叙述错误的是
| A.碳元素存在12C、13C、14C等多种同位素 |
| B.原子半径Si大于C,使得硅原子间难以形成双键 |
| C.碳和二氧化硅反应制粗硅,每生成28g硅有2NA个硅氧键断裂 |
D.12g金刚石中含有的晶胞数目为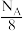 |
您最近一年使用:0次
2022-04-14更新
|
654次组卷
|
3卷引用:山东省滨州市2023届高三上学期期末综合测试化学试题
山东省滨州市2023届高三上学期期末综合测试化学试题山东省青岛市2021-2022学年高三下学期第一次模拟考试化学试题(已下线)考点02 物质的量 气体摩尔体积-备战2023年高考化学一轮复习考点帮(全国通用)
10 . 短周期主族元素A、B、C、D、E的原子序数依次增大,B、E处于同一主族。A的一种同位素在考古研究中用于测定一些文物的年代,B原子的最外层电子数是内层电子总数的3倍,D在同周期元素形成的离子中半径最小,C与B能形成C2B、C2B2型化合物。
请回答下列问题:
(1)A在元素周期表中的位置为______ ,A与原子半径最小的原子形成的10电子分子的空间结构为______ 。
(2)A、E中非金属性较强的是______ (填元素符号),两者可形成AE2型化合物,该化合物的结构式为_______ 。
(3)C、D的最高价氧化物的水化物之间反应的离子方程式为________ 。
(4)C、E可形成化合物M,用电子式表示M的形成过程_______ 。
(5)C2B2中的化学键类型为______ (填“离子键”、“极性键”或“非极性键”)。
请回答下列问题:
(1)A在元素周期表中的位置为
(2)A、E中非金属性较强的是
(3)C、D的最高价氧化物的水化物之间反应的离子方程式为
(4)C、E可形成化合物M,用电子式表示M的形成过程
(5)C2B2中的化学键类型为
您最近一年使用:0次



