1 . 下列说法正确的是
| A.第二能层含有2s、2p和2d三个能级 | B.处于同一能层的电子能量一定相同 |
| C.原子中3d2表示3d能级有两个轨道 | D.F原子中s轨道的电子云轮廓都为球形 |
您最近一年使用:0次
2022-11-02更新
|
443次组卷
|
4卷引用:四川省遂宁中学校2022-2023学年高二上学期10月月考化学试题
名校
2 . 下列说法正确的是
| A.N2、O2和Cl2分子中均既含有σ键,又含有π键 |
| B.Na的核外电子排布由1s22s22p63s1→1s22s22p6的变化需要吸收能量 |
| C.氢原子的电子云图中小黑点表示电子的运动轨迹 |
| D.电离下列状态的铝的最外层一个电子:1s22s22p63s1比1s22s22p63s2所需能量更少 |
您最近一年使用:0次
名校
3 . 合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氨元素主要以分子的形式存在于空气中,是人工固氮的主要来源。基态氮原子核外电子最高能级的电子云轮廓图为_______ 形。
(2) 是
是____ (填“极性”或“非极性”)分子, 的键角
的键角_____ (填“>”或“<”)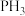 的键角。
的键角。
(3)纯叠氮酸 在常温下是一种液体,沸点较高,为
在常温下是一种液体,沸点较高,为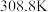 ,主要原因是
,主要原因是_______
(4)我国科研人员研制出了“ ”催化剂,将合成氨的温度、压强分别降到了
”催化剂,将合成氨的温度、压强分别降到了 、
、 ,这是近年来合成氨反应研究中的重要突破。
,这是近年来合成氨反应研究中的重要突破。
①比较 与
与 的半径大小关系:
的半径大小关系: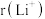
_______  (填“>”或“<”)。
(填“>”或“<”)。
② 的化合物
的化合物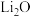 是离子化合物,下图是其
是离子化合物,下图是其 循环,表示其形成过程
循环,表示其形成过程
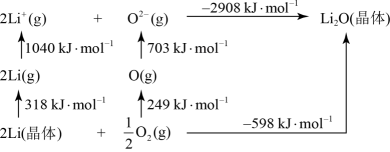
可知, 原子的第一电离能为
原子的第一电离能为_______  ,O=O键键能为
,O=O键键能为_______ 
(1)自然界中的氨元素主要以分子的形式存在于空气中,是人工固氮的主要来源。基态氮原子核外电子最高能级的电子云轮廓图为
(2)
 是
是 的键角
的键角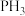 的键角。
的键角。(3)纯叠氮酸
 在常温下是一种液体,沸点较高,为
在常温下是一种液体,沸点较高,为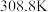 ,主要原因是
,主要原因是(4)我国科研人员研制出了“
 ”催化剂,将合成氨的温度、压强分别降到了
”催化剂,将合成氨的温度、压强分别降到了 、
、 ,这是近年来合成氨反应研究中的重要突破。
,这是近年来合成氨反应研究中的重要突破。①比较
 与
与 的半径大小关系:
的半径大小关系: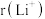
 (填“>”或“<”)。
(填“>”或“<”)。②
 的化合物
的化合物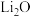 是离子化合物,下图是其
是离子化合物,下图是其 循环,表示其形成过程
循环,表示其形成过程
可知,
 原子的第一电离能为
原子的第一电离能为 ,O=O键键能为
,O=O键键能为
您最近一年使用:0次
2022-10-19更新
|
143次组卷
|
2卷引用:四川省绵阳市南山中学2022-2023学年高二上学期10月月考化学试题
名校
4 . 在现代工业中,锰及其化合物应用于国民经济的各个领域,其中钢铁工业是最重要的领域,用锰量占90%—95%,主要作为炼铁炼钢过程中的脱氧剂和脱硫剂。在自然界中,锰有II、III、IV及VII价态,对于基态锰原子,下列叙述错误的是
| A.基态锰原子核外电子的空间运动状态有15种 |
| B.4s电子能量较高,总是在比3s电子离核更远的地方运动 |
| C.电负性比钾高,原子对键合电子的吸引力比钾大 |
| D.锰元素位于周期表的d区 |
您最近一年使用:0次
2022-09-01更新
|
129次组卷
|
2卷引用:四川省巴中市恩阳区2022-2023学年高二下学期4月期中考试化学试题
名校
5 . 下列有关原子轨道的叙述中正确的是
| A.硅原子的2s轨道能量较3p轨道高 |
| B.锂原子的2s轨道与5s轨道均为球形 |
| C.p能级的原子轨道呈哑铃形,随着能层序数的增加,p能级原子轨道数也在增多 |
| D.第四能层最多可容纳16个电子 |
您最近一年使用:0次
2022-08-28更新
|
626次组卷
|
3卷引用:四川省绵阳市江油中学2022-2023学年高二上学期10月月考化学试题
解题方法
6 . John B.Goodenough等三位科学家因在发展锂离子电池方面做出的贡献而获得了诺贝尔化学奖。回答下列问题:
(1)锰酸锂( LiMn2O4)电池具有原料成本低合成工艺简单等优点。原子中运动的电子有两种相反的身旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态Li原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Li原子,其核外电子自旋磁量子数的代数和为_______ 。基态 Mn原子核外价层电子的运动状态有_______ 种。
(2)锂离子电池的电解液一般为溶有LiPF6的碳酸酯类有机溶剂,LiPF6遇水反应生成PF3和POF , PF
, PF 中心原子的价层电子对数为
中心原子的价层电子对数为_______ ,POF3的空间构型为_______ 。 下列对PF5中心原子杂化方式的推断合理的是_______ (填字母)。
A. sp2 B. sp3 C. sp3d D. sp3d2
(3)三元正极材料LiC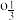 N
N jMnO2掺杂Al3+可使其性能更优,第三电离能:Fe
jMnO2掺杂Al3+可使其性能更优,第三电离能:Fe_______ (填“大于”或“小于”)Mn,原因是_______ 。
(4)链化锂被认为是很有潜力的正极材料,晶胞结构如图所示。
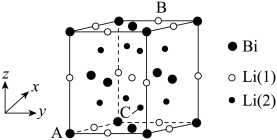
①晶施可以看作是由铋原子构成的面心立方晶格,锂原子填充在其中的四面体和八面体空隙处,晶体的化学式为_______ 。
②图中原子坐标参数:A为(0,0,0),B为(1,0.5,1),则C的坐标为_______ ,Bi与Li(1)和Li(2)之间的最短距离的比值为_______ 。
(1)锰酸锂( LiMn2O4)电池具有原料成本低合成工艺简单等优点。原子中运动的电子有两种相反的身旋状态,若一种自旋状态用+
 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态Li原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Li原子,其核外电子自旋磁量子数的代数和为(2)锂离子电池的电解液一般为溶有LiPF6的碳酸酯类有机溶剂,LiPF6遇水反应生成PF3和POF
 , PF
, PF 中心原子的价层电子对数为
中心原子的价层电子对数为A. sp2 B. sp3 C. sp3d D. sp3d2
(3)三元正极材料LiC
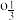 N
N jMnO2掺杂Al3+可使其性能更优,第三电离能:Fe
jMnO2掺杂Al3+可使其性能更优,第三电离能:Fe(4)链化锂被认为是很有潜力的正极材料,晶胞结构如图所示。

①晶施可以看作是由铋原子构成的面心立方晶格,锂原子填充在其中的四面体和八面体空隙处,晶体的化学式为
②图中原子坐标参数:A为(0,0,0),B为(1,0.5,1),则C的坐标为
您最近一年使用:0次
7 . 根据物质结构有关性质和特点,回答下列问题:
(1)钴位于元素周期表的___________ 。
(2)基态铝原子核外电子云轮廓图的形状有(填名称)___________ 。
(3)2020年新冠肺炎疫情席卷全球,酒精(CH3CH2OH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型是___________ 。
(4)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(III),是一种重要的配合物。该化合物中,所含非金属元素C的最高价氧化物的电子式为___________ ;Fe3+比Fe2+更稳定的原因___________ 。
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为___________ 。
(6)高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为___________ ;
(1)钴位于元素周期表的
(2)基态铝原子核外电子云轮廓图的形状有(填名称)
(3)2020年新冠肺炎疫情席卷全球,酒精(CH3CH2OH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型是
(4)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(III),是一种重要的配合物。该化合物中,所含非金属元素C的最高价氧化物的电子式为
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为
(6)高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为
您最近一年使用:0次
8 . 下列说法正确的是
| A.N2、O2和Cl2分子中均既含有σ键,又含有π键 |
| B.核外电子排布由1s22s22p63s1→1s22s22p63p1的变化需要吸收能量 |
| C.氢原子的电子云图中小黑点表示电子的运动轨迹 |
| D.电子从基态跃迁到激发态需要释放能量,光是电子释放能量的重要形式之一 |
您最近一年使用:0次
解题方法
9 . 如图所示是元素周期表中短周期的一部分,X、Y、Z、W四种元素的原子核外最外层电子数之和等于Y、Z元素的原子序数之和。下列说法不正确的是
| X | Y | ||
| Z | W |
| A.四种元素的原子都含有两种形状的电子云 |
| B.W原子的成对电子数最多 |
| C.四种元素的最高正化合价都等于其族序数 |
| D.Z 的最高价氧化物能溶于X的最高价含氧酸中 |
您最近一年使用:0次
10 . 下列现象与原子核外电子的跃迁无关的是
| A.激光笔产生红色光线 |
| B.金属钠在空气中燃烧时火焰呈黄色 |
| C.用光束照射胶体时产生光亮的通路 |
| D.焰火在夜空中呈现五彩缤纷的图案 |
您最近一年使用:0次
2022-05-01更新
|
158次组卷
|
4卷引用:四川省遂宁中学校2022-2023学年高二上学期期中考试化学试题
四川省遂宁中学校2022-2023学年高二上学期期中考试化学试题河南省商开大联考2021-2022学年高二下学期期中考试 化学(B卷)试题湖北省宜昌市协作体2022-2023学年高二下学期期中考试化学试题(已下线)1.1.1 能层与能级 基态与激发态(巩固)



