名校
解题方法
1 . 下列能层中,有9个原子轨道的是
| A.K | B.L | C.M | D.N |
您最近半年使用:0次
2022-01-08更新
|
372次组卷
|
4卷引用:四川省达州市2020-2021学年高二上学期期末检测化学试题
四川省达州市2020-2021学年高二上学期期末检测化学试题(已下线)第1.1.2讲 构造原理与电子排布式 电子云与原子轨道-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)辽宁省辽河油田第二高级中学2021-2022学年高二下学期开学考试化学试题广东省云浮市云安区云安中学2021-2022学年高二下学期第一次统测化学试题
解题方法
2 . N原子核外能量最高的电子具有不同的
| A.电子亚层 | B.电子云伸展方向 | C.电子云形状 | D.自旋方向 |
您最近半年使用:0次
2021-12-31更新
|
640次组卷
|
3卷引用:上海市黄浦区2022届高三一模化学试题
解题方法
3 . 明确宏观现象的微观本质是学习化学的重要思想方法。
(1)如图1是钾原子和硫原子的结构示意图,请回答:___________ 。
②钾原子在化学反应中易___________ 电子(填“得到”或“失去”)。
③钾素和硫元素形成的化合物硫化钾的化学式是___________ 。
(2)图2是硫酸铜溶液与锌粒反应前后溶液中主要离子变化示意图。_______
②反应中过量的物质是________ (写化学式)。
③该反应的化学方程式为_______ ,反应现象为_______
(1)如图1是钾原子和硫原子的结构示意图,请回答:

②钾原子在化学反应中易
③钾素和硫元素形成的化合物硫化钾的化学式是
(2)图2是硫酸铜溶液与锌粒反应前后溶液中主要离子变化示意图。
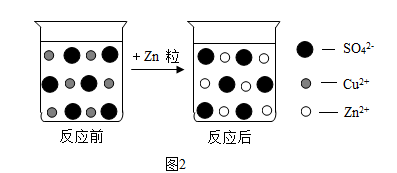
②反应中过量的物质是
③该反应的化学方程式为
您最近半年使用:0次
2021-10-22更新
|
153次组卷
|
2卷引用:新疆柯坪县柯坪湖州国庆中学2021-2022学年高一上学期开学考试理综化学试题
名校
4 . 回答下列问题:
(1)分子(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为___ ,(CN)2称为“拟卤素”,具有类似Cl2的化学性质,则(CN)2与NaOH水溶液反应的化学方程式为___ 。
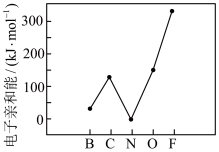
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,氮元素的E1呈现异常的原因是___ 。
(3)基态As原子中,核外电子占据最高能层的符号是___ ,占据该能层电子的电子云轮廓图形状为___ 。
(1)分子(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,氮元素的E1呈现异常的原因是

(3)基态As原子中,核外电子占据最高能层的符号是
您最近半年使用:0次
5 .  能层包含的能级数和最多能容纳的电子数分别为
能层包含的能级数和最多能容纳的电子数分别为
 能层包含的能级数和最多能容纳的电子数分别为
能层包含的能级数和最多能容纳的电子数分别为| A.2 2 | B.2 8 | C.3 8 | D.3 18 |
您最近半年使用:0次
2021-07-07更新
|
828次组卷
|
6卷引用:湖北省十堰市2020-2021学年高二下学期期末调研考试化学试题
湖北省十堰市2020-2021学年高二下学期期末调研考试化学试题(已下线)第1.1.1讲 能层与能级 基态与激发态-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)福建省三明市四地四校2021-2022学年高二下学期期中联考化学试题新疆柯坪县柯坪湖州国庆中学2021-2022学年高二下学期期中考试化学试题广东省湛江市雷州市第二中学2023-2024学年高二下学期开学化学试题新疆霍尔果斯市苏港中学2023-2024学年高二下学期4月月考化学试题
解题方法
6 . 下面有关“核外电子的运动状态”的说法,错误的是
| A.各原子轨道的伸展方向种数按p、d、f的顺序分别为3、5、7 |
| B.只有在电子层、原子轨道、原子轨道伸展方向及电子的自旋方向都确定时,才能准确表示电子的运动状态 |
| C.p轨道呈纺锤形,随着电子层的增加,p轨道的数量也在增多 |
| D.原子轨道伸展方向与能量大小是无关的 |
您最近半年使用:0次
名校
解题方法
7 . 第四周期中的18 种元素具有重要的用途,在现代工业中备受青睐。
(1)其中,未成对电子数最多的元素名称为_______ ,该元素的基态原子中,电子占据的最高能层具有的原子轨道数为_______ 。
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能不符合这一规律原因是_______ 。
(3)AsH3 中心原子杂化的类型为_______ ,分子构型为_______
(4)过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等。基态铁原子核外的价电子排布图为_______ 。
(5)与CN-互为等电子体的一种分子为_______ (填化学式);1.5mol [Fe(CN)6]3-中含有键的数目为_______
(1)其中,未成对电子数最多的元素名称为
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能不符合这一规律原因是
(3)AsH3 中心原子杂化的类型为
(4)过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等。基态铁原子核外的价电子排布图为
(5)与CN-互为等电子体的一种分子为
您最近半年使用:0次
2021-05-29更新
|
112次组卷
|
2卷引用:黑龙江省齐齐哈尔市第八中学校2020-2021学年高二下学期期中考试化学试题
解题方法
8 . 老师在黑板上写出“Cr: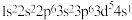 ”,下列各同学的判断中正确的是
”,下列各同学的判断中正确的是
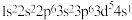 ”,下列各同学的判断中正确的是
”,下列各同学的判断中正确的是| A.甲同学认为是激发态Cr原子的核外电子排布式 |
| B.乙同学认为Cr元素位于第四周期第ⅥB族,处于d区,属过渡金属 |
| C.丙同学认为1s、2s、3s和4s的电子云形状相同,属同一种能级 |
D.丁同学认为Cr原子的价层电子排布式为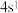 |
您最近半年使用:0次
名校
解题方法
9 . 原子结构与元素周期表存在着内在联系。根据已学知识,请你回答下列问题:
(1)指出31号元素镓(Ga)在元素周期表中的位置:___ 。
(2)写出原子序数最小的第Ⅷ族元素原子的核外的价电子排布图:____ 。其正三价离子的未成对电子数为____
(3)写出3p轨道上有2个未成对电子的元素的符号:____ 。
(4)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为___ 。
(5)基态原子的4s能级中只有1个电子的元素共有___ 种
(6)元素基态原子的M层全充满,N层有且只有一个未成对电子,其基态原子的电子排布式为___ ,属于____ 区元素;[Cu(NH3)4]SO4中所含的化学键有___ ,,[Cu(NH3)4]SO4的外界离子的空间构型为____ 。
(1)指出31号元素镓(Ga)在元素周期表中的位置:
(2)写出原子序数最小的第Ⅷ族元素原子的核外的价电子排布图:
(3)写出3p轨道上有2个未成对电子的元素的符号:
(4)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为
(5)基态原子的4s能级中只有1个电子的元素共有
(6)元素基态原子的M层全充满,N层有且只有一个未成对电子,其基态原子的电子排布式为
您最近半年使用:0次
名校
10 . 以下核外电子的表示方法中,能表示该微粒处于能量最低状态的是
A.N: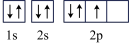 | B.F-: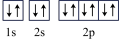 |
| C.Fe:[Ar]3d54s2 | D.Cu:3d94s2 |
您最近半年使用:0次
2021-04-15更新
|
248次组卷
|
2卷引用:四川省成都市新津中学高2020-2021学年高二下学期4月月考试题



