1 . 回答下列问题
(1)基态碘原子的价层电子的运动状态有_____ 种,基态Pb原子的价层电子排布式为_____ 。
(2) 价电子轨道表示式为
价电子轨道表示式为_____ ;
(3)一种磷酸硅铝分子筛常用于催化甲醇制烯烃的反应。由硅原子核形成的三种微粒: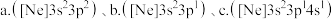 ,半径由大到小的顺序为
,半径由大到小的顺序为_____ (填标号);第三周期元素中,第一电离能介于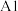 和P之间的元素有
和P之间的元素有_____ 种。
(4)下列状态的铁中,电离最外层一个电子所需能量最大的是_____ (填标号)。
 原子的价电子中,两种自旋状态的电子数之比为
原子的价电子中,两种自旋状态的电子数之比为_____ 。
(6)原子发射光谱法是通过处于激发态的待测元素微粒回到基态时发射的特征谱线对其进行鉴别的方法。下列状态的铁粒子处于激发态的是_____(填标号)。
(1)基态碘原子的价层电子的运动状态有
(2)
 价电子轨道表示式为
价电子轨道表示式为(3)一种磷酸硅铝分子筛常用于催化甲醇制烯烃的反应。由硅原子核形成的三种微粒:
 ,半径由大到小的顺序为
,半径由大到小的顺序为 和P之间的元素有
和P之间的元素有(4)下列状态的铁中,电离最外层一个电子所需能量最大的是
a.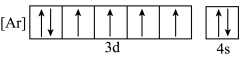
b.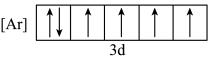
c.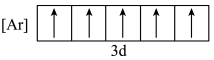
d.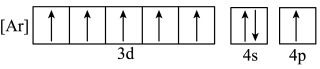
 原子的价电子中,两种自旋状态的电子数之比为
原子的价电子中,两种自旋状态的电子数之比为(6)原子发射光谱法是通过处于激发态的待测元素微粒回到基态时发射的特征谱线对其进行鉴别的方法。下列状态的铁粒子处于激发态的是_____(填标号)。
A.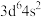 | B.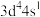 | C.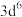 | D.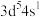 |
您最近一年使用:0次
名校
解题方法
2 . 根据已学知识,请回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是_______ ,占据该能层电子的原子轨道形状为_______ 。
(2)写出3p轨道上有2个未成对电子的元素的符号:_______ 。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的价层电子排布式为4s24p4,该元素的名称是_______ 。
(4)已知铁是26号元素,写出基态Fe的价层电子排布式:_______ ;在元素周期表中,该元素在_______ (填“s”“p”“d”“f”或“ds”)区。
(5)NaAlO2在水溶液中实际上都是以Na[Al(OH)4]形式存在。其中[Al(OH)4]-为配离子,写出A1原子的杂化方式_______ ,该阴离子中存在的化学键有_______ (填字母代号)
A.离子键 B.极性键 C.非极性键
D.金属键 E.配位键 F.氢键
(1)基态N原子中,核外电子占据的最高能层的符号是
(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的价层电子排布式为4s24p4,该元素的名称是
(4)已知铁是26号元素,写出基态Fe的价层电子排布式:
(5)NaAlO2在水溶液中实际上都是以Na[Al(OH)4]形式存在。其中[Al(OH)4]-为配离子,写出A1原子的杂化方式
A.离子键 B.极性键 C.非极性键
D.金属键 E.配位键 F.氢键
您最近一年使用:0次
2024-04-24更新
|
102次组卷
|
2卷引用:河北省衡水市枣强中学2023-2024学年高二下学期第一次调研考试化学试题
3 . A、B、C、D、E、F、G、W是原子序数依次增大的8种元素,A元素原子的2p轨道上有2个未成对电子;B元素在同周期中原子半径最大,与A可形成原子个数比为1∶1和2∶1的两种化合物;C的单质是一种常见的半导体材料;F有9个原子轨道,且只有一个未成对电子,没有空轨道;G的单质是一种常见金属,其 价离子
价离子 有4个未成对电子;W能形成红色(或砖红色)的
有4个未成对电子;W能形成红色(或砖红色)的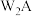 和黑色的WA两种化合物。请回答下列问题:
和黑色的WA两种化合物。请回答下列问题:
(1)C原子最高能级的电子云轮廓图是___________ 形状,W位于元素周期表___________ 区,W的简化电子排布式为___________ 。
(2)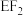 中中心原子的杂化轨道类型为
中中心原子的杂化轨道类型为___________ , 的VSEPR模型为
的VSEPR模型为___________ 。
(3)D、E、F三种元素第一电离能从大到小的顺序是___________ (用元素符号及“>”表示)。
(4)A、B、C、D四种元素电负性由大到小顺序是___________ (用元素符号及“>”表示)。
(5) 比
比 稳定,原因是
稳定,原因是___________ 。
 价离子
价离子 有4个未成对电子;W能形成红色(或砖红色)的
有4个未成对电子;W能形成红色(或砖红色)的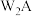 和黑色的WA两种化合物。请回答下列问题:
和黑色的WA两种化合物。请回答下列问题:(1)C原子最高能级的电子云轮廓图是
(2)
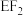 中中心原子的杂化轨道类型为
中中心原子的杂化轨道类型为 的VSEPR模型为
的VSEPR模型为(3)D、E、F三种元素第一电离能从大到小的顺序是
(4)A、B、C、D四种元素电负性由大到小顺序是
(5)
 比
比 稳定,原因是
稳定,原因是
您最近一年使用:0次
解题方法
4 . 原子结构与元素周期表存在着内在联系。根据已学知识,请你回答下列问题:
(1)指出31号元素镓(Ga)在元素周期表中的位置:___________ (写明第几周期第几族)。
(2)第3周期元素的基态原子与基态Cu原子未成对电子数相同,且电负性最大的元素是___________ 。
(3)在P区中,第2周期VA族元素原子电子的轨道表示式为:___________ 。
(4)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为:___________ 。
(5)写出原子序数最小的Ⅷ族元素原子的核外电子排布式:___________ 。
(6)写出3p轨道上有2个未成对电子的元素符号:___________ 。
(7)日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为:___________ 。
(1)指出31号元素镓(Ga)在元素周期表中的位置:
(2)第3周期元素的基态原子与基态Cu原子未成对电子数相同,且电负性最大的元素是
(3)在P区中,第2周期VA族元素原子电子的轨道表示式为:
(4)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为:
(5)写出原子序数最小的Ⅷ族元素原子的核外电子排布式:
(6)写出3p轨道上有2个未成对电子的元素符号:
(7)日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为:
您最近一年使用:0次
5 . 四氯化钛( )主要用于制取海绵钛和钛白粉,也可用作催化剂。工业上以钛铁矿、焦炭、氯气为原料,在高温条件下制取
)主要用于制取海绵钛和钛白粉,也可用作催化剂。工业上以钛铁矿、焦炭、氯气为原料,在高温条件下制取 ,反应的化学方程式为
,反应的化学方程式为
 。请回答下列问题:
。请回答下列问题:
(1)基态钛原子的电子排布式为___________ ,其未成对电子数为___________ 。
(2)已知:H、 、
、 的电负性分别为2.1、3.0、1.5,则
的电负性分别为2.1、3.0、1.5,则 中
中 和
和 之间的化学键类型为
之间的化学键类型为___________ , 中
中 的化合价为
的化合价为___________ 。
(3)基态碳原子中,能量最高的电子位于___________ 轨道,该轨道有___________ 个伸展方向,轨道形状为___________ 。
(4)若用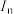 表示元素的第n电离能,碳元素的电离能变化趋势如图所示:
表示元素的第n电离能,碳元素的电离能变化趋势如图所示:

 与
与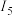 的差值明显大于其他相邻电离能的差值,原因是
的差值明显大于其他相邻电离能的差值,原因是___________ 。
(5)基态铁原子的外围电子轨道表示式为___________ 。 的稳定性强于
的稳定性强于 ,从微观角度解释其原因为
,从微观角度解释其原因为___________ 。
 )主要用于制取海绵钛和钛白粉,也可用作催化剂。工业上以钛铁矿、焦炭、氯气为原料,在高温条件下制取
)主要用于制取海绵钛和钛白粉,也可用作催化剂。工业上以钛铁矿、焦炭、氯气为原料,在高温条件下制取 ,反应的化学方程式为
,反应的化学方程式为
 。请回答下列问题:
。请回答下列问题:(1)基态钛原子的电子排布式为
(2)已知:H、
 、
、 的电负性分别为2.1、3.0、1.5,则
的电负性分别为2.1、3.0、1.5,则 中
中 和
和 之间的化学键类型为
之间的化学键类型为 中
中 的化合价为
的化合价为(3)基态碳原子中,能量最高的电子位于
(4)若用
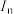 表示元素的第n电离能,碳元素的电离能变化趋势如图所示:
表示元素的第n电离能,碳元素的电离能变化趋势如图所示:
 与
与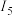 的差值明显大于其他相邻电离能的差值,原因是
的差值明显大于其他相邻电离能的差值,原因是(5)基态铁原子的外围电子轨道表示式为
 的稳定性强于
的稳定性强于 ,从微观角度解释其原因为
,从微观角度解释其原因为
您最近一年使用:0次
名校
解题方法
6 . A、B、C、D、E、F均为36号以前的元素且原子序数依次增大。请完成下列空白:
(1)A元素基态原子的最外层有2个未成对电子,次外层有2个电子,它的原子核外电子共与_____ 种不同的运动状态,原子轨道数目为_______ 。
(2)B元素的原子最外层电子排布式为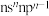 ,其简单氢化物的电子式为
,其简单氢化物的电子式为______ 。
(3)C、D原子核外s能级上的电子总数与p能级上的电子总数均相等。C、D简单离子的半径由大小到的顺序是______ (用离子符号填空)。A、B、C、D四种元素的原子半径由大到小的顺序是_______ (用元素符号填空,下同),四种元素的电负性由到大到小的顺序是________ ,四种元素的第一电离能由大到小的顺序是_______ 。
(4)E、F均位于ds区。则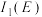
_____ 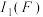 (填“>”或“<”),理由是
(填“>”或“<”),理由是___________ 。
(1)A元素基态原子的最外层有2个未成对电子,次外层有2个电子,它的原子核外电子共与
(2)B元素的原子最外层电子排布式为
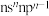 ,其简单氢化物的电子式为
,其简单氢化物的电子式为(3)C、D原子核外s能级上的电子总数与p能级上的电子总数均相等。C、D简单离子的半径由大小到的顺序是
(4)E、F均位于ds区。则
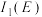
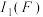 (填“>”或“<”),理由是
(填“>”或“<”),理由是
您最近一年使用:0次
名校
解题方法
7 . 已知五种前四周期的元素X、Y、Z、Q、T。其中,基态X原子的M层上有6种运动状态不同的电子;基态Y原子的简化电子排布式[Ar]3d84s2,基态Z原子的L层的p能级有一个空轨道;基态Q原子的L层的p能级只有一对成对电子;基态T原子的M层上p轨道为半充满状态。根据题给信息,回答有关问题:
(1)试推断这五种元素的符号:X:___________ ,Y:___________ ,Z:___________ ,Q:___________ ,T:___________ 。
(2)Y在元素周期表中的位置为___________ 。
(3)基态Z原子的轨道表示式为___________ 。
(4)对于T原子的p轨道2px、2py、2pz间的差异,下列说法错误的是___________ (填字母)。
a.电子云形状相同 b.原子轨道的对称类型不同
c.电子的能量不同 d.电子云空间伸展方向不同
(5)Z元素的最高价氧化物对应水化物的电离方程式为___________ 。
(1)试推断这五种元素的符号:X:
(2)Y在元素周期表中的位置为
(3)基态Z原子的轨道表示式为
(4)对于T原子的p轨道2px、2py、2pz间的差异,下列说法错误的是
a.电子云形状相同 b.原子轨道的对称类型不同
c.电子的能量不同 d.电子云空间伸展方向不同
(5)Z元素的最高价氧化物对应水化物的电离方程式为
您最近一年使用:0次
名校
解题方法
8 . 已知X、Y、Z、W、Q、R六种元素中,原子序数依次增大,其结构或性质信息如表。
请根据信息回答有关问题:
(1)元素X原子核外共有_______ 种不同运动状态的电子。
(2)元素X、Y的第一电离能较大的是_______ (填元素符号)。
(3)元素X、Y、Z的电负性最小的是_______ (填元素符号)。
(4)元素W的基态原子核外电子排布式为_______ 。
(5)元素Q在周期表中位置为_______ ,元素R基态原子的价电子排布式为 _______ 。
| 元素 | 结构或性质信息 |
| X | 基态原子的最外层电子排布式为nsnnpn+1 |
| Y | 基态原子的L层上有2个未成对的p电子 |
| Z | 基态原子的M层上s、p电子个数相等 |
| W | 位于第4周期VIB族 |
| Q | 元素的正三价离子的3d能级半充满 |
| R | 元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子| |
(1)元素X原子核外共有
(2)元素X、Y的第一电离能较大的是
(3)元素X、Y、Z的电负性最小的是
(4)元素W的基态原子核外电子排布式为
(5)元素Q在周期表中位置为
您最近一年使用:0次
名校
9 . 按要求填空:
(1)①基态A原子的电子排布式为1s22s22p5,则A元素位于周期表______ 。
②化合物M可通过石油工业获取,其产量标志着一个国家石油化工水平,该化合物中σ键与π键个数比为______ 。
③XY2是红棕色气体,X与氢元素可形成XH3,X基态原子的价层电子轨道表示式为______ 。
④1~36号元素的基态原子中,未成对电子数最多的元素是______ (写元素符号)。
(2)蓝矾(CuSO4•5H2O)的结构如图所示,SO 中S原子的杂化轨道类型是
中S原子的杂化轨道类型是_____ 。

(1)①基态A原子的电子排布式为1s22s22p5,则A元素位于周期表
②化合物M可通过石油工业获取,其产量标志着一个国家石油化工水平,该化合物中σ键与π键个数比为
③XY2是红棕色气体,X与氢元素可形成XH3,X基态原子的价层电子轨道表示式为
④1~36号元素的基态原子中,未成对电子数最多的元素是
(2)蓝矾(CuSO4•5H2O)的结构如图所示,SO
 中S原子的杂化轨道类型是
中S原子的杂化轨道类型是
您最近一年使用:0次
2022·河北·高考真题
真题
10 . 含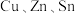 及S的四元半导体化合物(简写为
及S的四元半导体化合物(简写为 ),是一种低价、无污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
),是一种低价、无污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
(1)基态S原子的价电子中,两种自旋状态的电子数之比为_______ 。
(2)Cu与Zn相比,第二电离能与第一电离能差值更大的是_______ ,原因是_______ 。
(3) 的几何构型为
的几何构型为_______ ,其中心离子杂化方式为_______ 。
(4)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列物质中,属于顺磁性物质的是_______(填标号)。
(5)如图是硫的四种含氧酸根的结构:

根据组成和结构推断,能在酸性溶液中将 转化为
转化为 的是
的是_______ (填标号)。理由是_______ 。
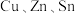 及S的四元半导体化合物(简写为
及S的四元半导体化合物(简写为 ),是一种低价、无污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
),是一种低价、无污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:(1)基态S原子的价电子中,两种自旋状态的电子数之比为
(2)Cu与Zn相比,第二电离能与第一电离能差值更大的是
(3)
 的几何构型为
的几何构型为(4)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列物质中,属于顺磁性物质的是_______(填标号)。
A. | B. | C. | D.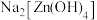 |

根据组成和结构推断,能在酸性溶液中将
 转化为
转化为 的是
的是
您最近一年使用:0次
2022-07-01更新
|
4167次组卷
|
7卷引用:2022年新高考河北省高考真题化学试题(部分试题)
(已下线)2022年新高考河北省高考真题化学试题(部分试题)(已下线)第19练 物质结构与性质综合题难点突破-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)第一部分 二轮专题突破 大题突破4 物质结构与性质大题研究(选考)(已下线)回归教材重难点12 原子、分子和晶体结构再归纳-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)专题20 结构与性质(已下线)专题20 结构与性质(已下线)专题17 物质结构与性质综合题-2023年高考化学真题题源解密(新高考专用)



