名校
解题方法
1 . Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为____ 。
A. B.
B.
C.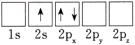 D.
D.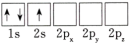
(2)Li+与H-具有相同的电子构型,但r(Li+)小于r(H-),原因是____ 。
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是____ ,中心原子的杂化形式为____ 。LiAlH4中,存在下列给出的____ 。
A.离子键 B.σ键 C.π键 D.氢键
(4)Li2O是离子晶体,其晶格能可通过图中的循环计算得到,由数据可知Li原子的第一电离能为____ kJ/mol,O=O键能为____ kJ/mol,Li2O晶格能为____ kJ/mol。
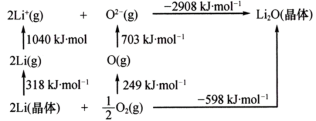
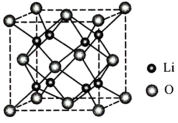
(5)Li2O具有反萤石结构,晶胞如图所示。已知晶胞参数为anm,阿伏加德罗常数的值为NA,则Li2O的密度为____ g•cm-3(列出计算式即可)。
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
 D.
D.
(2)Li+与H-具有相同的电子构型,但r(Li+)小于r(H-),原因是
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是
A.离子键 B.σ键 C.π键 D.氢键
(4)Li2O是离子晶体,其晶格能可通过图中的循环计算得到,由数据可知Li原子的第一电离能为
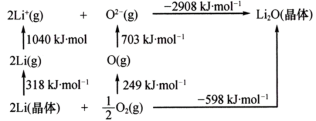
(5)Li2O具有反萤石结构,晶胞如图所示。已知晶胞参数为anm,阿伏加德罗常数的值为NA,则Li2O的密度为

您最近一年使用:0次
2022-09-19更新
|
159次组卷
|
2卷引用:内蒙古达拉特旗第一中学2022-2023学年高三上学期开学考试理综化学试题
解题方法
2 . 金属钛因具有强度高、耐蚀性好、耐热性高等特点而被广泛用于各个领域。
(1)基态 Ti 原子核外电子排布的最高能级符号是____ 。与钛同周期的元素中基态原子未成对电子数与钛相同的有__________ 种。
(2)钛比钢轻,比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是_____ 。
(3)半夹心结构催化剂 M 其结构如图所示:

①组成该物的质元素中,电负性最大的是___________ (填元素符号)
②M中不含_________ (填标号)
a.π键 b.σ键 c.配位键 d.离子键 e.氢键
(4)TiO2能溶于浓硫酸并析出一种离子晶体,已知其中阳离子是以链状聚合物形式存在的钛酰阳离子,其结构如图所示,其化学式是______ 写出一种与阴离子 互为等电子体的分子
互为等电子体的分子______ 。

(5)钛单质的晶胞如图所示,该晶胞为______ 堆积(填堆积方式),钛原子的配位数是_______ ,已知晶胞参数:a=0.295nm,c=0.469nm。则该钛晶体的密度为___________ g·cm-3(NA表示阿伏加 德罗常数的数值,列出计算式即可)

(1)基态 Ti 原子核外电子排布的最高能级符号是
(2)钛比钢轻,比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是
(3)半夹心结构催化剂 M 其结构如图所示:

①组成该物的质元素中,电负性最大的是
②M中不含
a.π键 b.σ键 c.配位键 d.离子键 e.氢键
(4)TiO2能溶于浓硫酸并析出一种离子晶体,已知其中阳离子是以链状聚合物形式存在的钛酰阳离子,其结构如图所示,其化学式是
 互为等电子体的分子
互为等电子体的分子
(5)钛单质的晶胞如图所示,该晶胞为

您最近一年使用:0次
名校
3 . 硼及其化合物广泛应用于高新材料领域,请回答下列有关问题:
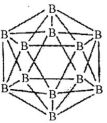
(1)晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图)。
①在基态11B原子中,核外存在______ 对自旋相反的电子。
②若每个单元中有两个原子为l0B,其余为11B,则该单元结构的类型有______ 种。
(2)NaBH4是一种重要的储氢载体,其中涉及元素的电负性由小到大的顺序为________ ,BH4-离子的空间构型是_____________ ,与BH4-互为等电子体的的分子有___________ 。
(3)硼酸(H3BO3)为白色片状晶体,有与石墨相似的层状结构,则硼酸晶体中存在的作用力有共价键、_____ 、_______ 。与H3BO3酸性最接近的是__________ (填字母)。
A.H4SiO4B.H3PO4C.HNO2
(4)磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层。如图是磷化硼晶体的晶胞,B原子的杂化方式是___________ 。立方相氮化硼晶体的熔点要比磷化硼体高,其原因是_____________ 。
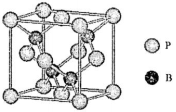
(5)已知磷化硼的晶胞参数a=478 pm,请列式计算该晶体的密度p=_____ g.cm-3(用含NA的代数式表示即可,不需要计算出结果)。晶胞中硼原子和磷原子最近的核间距为_________ pm。
(1)晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图)。

①在基态11B原子中,核外存在
②若每个单元中有两个原子为l0B,其余为11B,则该单元结构的类型有
(2)NaBH4是一种重要的储氢载体,其中涉及元素的电负性由小到大的顺序为
(3)硼酸(H3BO3)为白色片状晶体,有与石墨相似的层状结构,则硼酸晶体中存在的作用力有共价键、
A.H4SiO4B.H3PO4C.HNO2
(4)磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层。如图是磷化硼晶体的晶胞,B原子的杂化方式是

(5)已知磷化硼的晶胞参数a=478 pm,请列式计算该晶体的密度p=
您最近一年使用:0次
2017-05-21更新
|
308次组卷
|
3卷引用:内蒙古北方重工业集团有限公司第三中学2018届高三12月月考化学试题



