1 . 下列化学用语表示正确的是
| A.提取碘水中的碘:分液 |
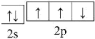
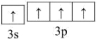
B.碳的基态原子轨道表示式: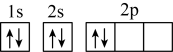 |
C.BF3的空间结构: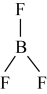 (平面三角形) (平面三角形) |
D.HCl的形成过程: |
您最近一年使用:0次
名校
解题方法
2 . 下列化学用语或图示表达正确的是
A.光导纤维主要成分的分子式: |
B. 的价层电子对互斥模型: 的价层电子对互斥模型: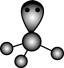 |
C.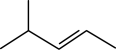 的名称:2-甲基-3-戊烯 的名称:2-甲基-3-戊烯 |
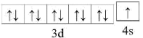
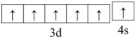
D.基态 的价层电子轨道表示式: 的价层电子轨道表示式: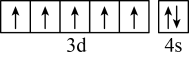 |
您最近一年使用:0次
2024-05-27更新
|
175次组卷
|
2卷引用:广东省名校教研联盟2023-2024学年高三下学期5月测试化学试题
3 . X、Y、Z、Q、T代表五种元素,相关信息如表所示:
请回答下列问题:
(1)X的元素符号为___________ ,其基态原子的电子排布式为___________ 。
(2)Y的元素名称为___________ ,其基态原子的轨道表示式为___________ 。
(3)Z的基态原子的价层电子的轨道表示式为___________ ;
(4)Q其简单离子的结构示意图为___________ 。Q单质在CO2中燃烧的化学方程式___________
(5)T的基态原子的价层电子排布式为___________ ;其单质在X的常见单质中燃烧的化学方程式为___________ 。
请回答下列问题:
| 元素 | 信息 |
| X | 基态原子最外层电子数是其电子层数的3倍 |
| Y | 基态原子的L层上有2个空轨道 |
| Z | 基态原子的M层的p能级上有3个未成对电子 |
| Q | 基态原子的价层电子排布式为3sn3p2n-4 |
| T | 正三价离子的3d能级为半充满状态 |
(2)Y的元素名称为
(3)Z的基态原子的价层电子的轨道表示式为
(4)Q其简单离子的结构示意图为
(5)T的基态原子的价层电子排布式为
您最近一年使用:0次
解题方法
4 . A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其基态原子的电子排布图为___________ 。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B-的结构示意图为___________ ,C元素在元素周期表的___________ 区,写出常温下B的单质与C的最高价氧化物对应水化物反应的化学方程式:___________ 。
(3)D元素的正三价离子的3d能级为半充满状态,其基态原子的电子排布式为___________ 。
试根据原子核外电子排布所遵循的原理解释D的二价阳离子具有较强的还原性,易被氧化为正三价离子的原因:___________ 。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的价电子排布式为___________ 。
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其基态原子的电子排布图为
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B-的结构示意图为
(3)D元素的正三价离子的3d能级为半充满状态,其基态原子的电子排布式为
试根据原子核外电子排布所遵循的原理解释D的二价阳离子具有较强的还原性,易被氧化为正三价离子的原因:
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的价电子排布式为
您最近一年使用:0次
解题方法
5 . 现有六种元素A、B、C、D、E、F,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)某同学根据上述信息,推断A基态原子的轨道表示式为 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了___________ 。
(2)B元素的电负性___________ (填“大于”“小于”或“等于”)C元素的电负性。
(3)C与D形成的化合物所含有的化学键类型为___________ 。
(4)ABCD四种元素的第一电离能由大到小(用元素符号回答):___________ 。
(5)E基态原子中能量最高的电子,其电子云在空间有___________ 个伸展方向。
(6)写出F原子的价电子轨道表示式___________ 。
(7)点燃D的单质,放入A、C两种元素组成的一种化合物中,可以生成一种白色固体和一种黑色固体,俗称“白加黑实验”,请写出该反应的化学方程式___________ 。
| A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| B元素原子的核外p电子数比s电子数少1 |
| C元素是地壳中含量最多的元素 |
D元素原子的第一至第四电离能分别是: ; ;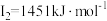 ; ;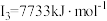 ; ; |
| E原子核外所有p轨道全满或半满 |
| F的基态原子4s和3d轨道半充满 |
 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了(2)B元素的电负性
(3)C与D形成的化合物所含有的化学键类型为
(4)ABCD四种元素的第一电离能由大到小(用元素符号回答):
(5)E基态原子中能量最高的电子,其电子云在空间有
(6)写出F原子的价电子轨道表示式
(7)点燃D的单质,放入A、C两种元素组成的一种化合物中,可以生成一种白色固体和一种黑色固体,俗称“白加黑实验”,请写出该反应的化学方程式
您最近一年使用:0次
6 . 磷锡青铜合金广泛用于仪器仪表中的耐磨零件和抗磁元件等,其晶胞结构如图所示。下列说法不正确的是

A.基态P原子的价层电子轨道表示式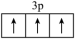 |
| B.磷锡青铜合金具有各向异性的特点 |
C.磷锡青铜合金的化学式为 |
| D.该晶胞中与Sn原子最近且等距离的Sn原子有6个 |
您最近一年使用:0次
名校
解题方法
7 . 对下列基态原子的价电子排布图正确的是
| 选项 | A | B |
| 原子 | N | Si |
| 价电子排布图 |
|
|
| 选项 | C | D |
| 原子 | K | Cr |
| 价电子排布图 |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 根据原子核外电子排布规则,回答下列问题:
(1)写出基态 原子的简化核外电子排布式:
原子的简化核外电子排布式:___________ ;写出基态 原子的价层电子排布式:
原子的价层电子排布式:___________ 。
(2)写出基态 原子的价层电子轨道表示式:
原子的价层电子轨道表示式:___________ 。
(3)若将基态 的电子排布式写成
的电子排布式写成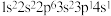 ,则它违背了
,则它违背了___________ 。
(4)已知 比
比 的稳定性更强,用电子排布解释其原因:
的稳定性更强,用电子排布解释其原因:___________ 。
(5)某基态原子的 能级中有一个电子,该原子为
能级中有一个电子,该原子为___________ (写元素符号)。
(1)写出基态
 原子的简化核外电子排布式:
原子的简化核外电子排布式: 原子的价层电子排布式:
原子的价层电子排布式:(2)写出基态
 原子的价层电子轨道表示式:
原子的价层电子轨道表示式:(3)若将基态
 的电子排布式写成
的电子排布式写成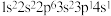 ,则它违背了
,则它违背了(4)已知
 比
比 的稳定性更强,用电子排布解释其原因:
的稳定性更强,用电子排布解释其原因:(5)某基态原子的
 能级中有一个电子,该原子为
能级中有一个电子,该原子为
您最近一年使用:0次
名校
9 . 下列化学用语表示不正确的是
A.水分子的VSEPR模型: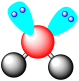 |
B.基态Cr的价层电子轨道表示式: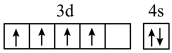 |
C.甲烷分子的空间填充模型: |
D. 的 的 键的电子云图形: 键的电子云图形: |
您最近一年使用:0次
名校
10 . 现有部分短周期元素的性质或原子结构如下表:
(1)写出元素X离子的电子轨道表示式 ___________ 。
(2)写出Y元素最高价氧化物的水化物与NaOH溶液反应的离子方程式___________ 。
(3)写出Z的电子排布式___________ 。
(4)元素T与氯元素相比,非金属性较强的是___________ (用元素符号表示),下列表述中能证明这一事实的是___________ 。
A.气态氢化物的挥发性和稳定性 B.单质分子中的键能
C.两元素单质的氧化性 D.含氧酸的酸性
E.氢化物中X—H键的键长(X代表T和Cl两种元素)
F.两元素在自然界中的存在形式
(5)探寻物质的性质差异性是学习的重要方法之一、T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是___________ (填元素符号),理由是___________ 。
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
(2)写出Y元素最高价氧化物的水化物与NaOH溶液反应的离子方程式
(3)写出Z的电子排布式
(4)元素T与氯元素相比,非金属性较强的是
A.气态氢化物的挥发性和稳定性 B.单质分子中的键能
C.两元素单质的氧化性 D.含氧酸的酸性
E.氢化物中X—H键的键长(X代表T和Cl两种元素)
F.两元素在自然界中的存在形式
(5)探寻物质的性质差异性是学习的重要方法之一、T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是
您最近一年使用:0次