1 . 我国科研工作者研究的金属-氮-碳优异电催化CO2 还原催化剂取得新进展。回答下列问题:
(1)14C 可用于考古,该基态原子价层电子轨道表示式为_______ 。
(2)研究发现钴-氮-碳优异电催化CO2 还原催化剂活性最高,金属钴的核外电子排布式为_______ ;基态Co中未成对电子数为_______ 。
(3)基态N原子中,电子占据的最高能层符号为_______ ,该能层具有的原子轨道数为_______ ,电子数为_______ 。
(4)基态铝原子核外共有_______ 种不同能级的电子,有_______ 种不同运动状态的电子。
(1)14C 可用于考古,该基态原子价层电子轨道表示式为
(2)研究发现钴-氮-碳优异电催化CO2 还原催化剂活性最高,金属钴的核外电子排布式为
(3)基态N原子中,电子占据的最高能层符号为
(4)基态铝原子核外共有
您最近一年使用:0次
2 . 按要求回答下列问题:
(1)基态O2-核外电子排布式为_______ 。
(2)基态P原子核外电子排布式为_______ 。
(3)基态Al原子核外电子排布式为_______ 。
(4)基态As原子核外电子简化的轨道表示式为_______ 。
(5)基态Fe3+核外电子简化的轨道表示式为_______ 。
(6)基态Se原子价电子轨道表示式为_______ 。
(1)基态O2-核外电子排布式为
(2)基态P原子核外电子排布式为
(3)基态Al原子核外电子排布式为
(4)基态As原子核外电子简化的轨道表示式为
(5)基态Fe3+核外电子简化的轨道表示式为
(6)基态Se原子价电子轨道表示式为
您最近一年使用:0次
3 . 材料是入类进步的基石,深入认识物质的结构有助于进一步开发新的材料。回答下列问题。
(1)B和Ni均为新材料的主角。
①按照杂化轨道理论,基态B原子的价电子先激发,再杂化成键形成 。杂化前,处于激发态的B原子的价电子轨道表示式为
。杂化前,处于激发态的B原子的价电子轨道表示式为___________ (填编号)。
A.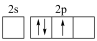 B.
B.  C.
C.  D.
D.
② 常温下呈液态,其分子空间构型为正四面体形。其易溶
常温下呈液态,其分子空间构型为正四面体形。其易溶 、苯等有机溶剂的原因是
、苯等有机溶剂的原因是___________ 。
(2)亚铁氰化钾具有防止食盐结块、保持食盐松散等作用,其化学式为 ,所含元素电负性由大到小的顺序为
,所含元素电负性由大到小的顺序为___________ ,1mol  含有σ键的物质的量为
含有σ键的物质的量为___________ 。
(3)铀氮化合物是核燃料循环系统中的重要物质。已知 。反应所得的气态产物中属于非极性分子的有
。反应所得的气态产物中属于非极性分子的有___________ (填化学式);反应中断裂的化学键有___________ 。(填编号)。
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
(4)某锂电池的负极材料是锂原子嵌入石墨烯层间,其晶胞结构(底边为平行四边形)如图所示。

该晶体的化学式为___________ 。
(1)B和Ni均为新材料的主角。
①按照杂化轨道理论,基态B原子的价电子先激发,再杂化成键形成
 。杂化前,处于激发态的B原子的价电子轨道表示式为
。杂化前,处于激发态的B原子的价电子轨道表示式为A.
 B.
B.  C.
C.  D.
D.
②
 常温下呈液态,其分子空间构型为正四面体形。其易溶
常温下呈液态,其分子空间构型为正四面体形。其易溶 、苯等有机溶剂的原因是
、苯等有机溶剂的原因是(2)亚铁氰化钾具有防止食盐结块、保持食盐松散等作用,其化学式为
 ,所含元素电负性由大到小的顺序为
,所含元素电负性由大到小的顺序为 含有σ键的物质的量为
含有σ键的物质的量为(3)铀氮化合物是核燃料循环系统中的重要物质。已知
 。反应所得的气态产物中属于非极性分子的有
。反应所得的气态产物中属于非极性分子的有a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
(4)某锂电池的负极材料是锂原子嵌入石墨烯层间,其晶胞结构(底边为平行四边形)如图所示。

该晶体的化学式为
您最近一年使用:0次
2023-10-04更新
|
283次组卷
|
2卷引用:广东省广州大学附属中学2023-2024学年高二下学期开学测化学试题
名校
解题方法
4 . 下列表示物质结构的化学用语或模型正确的是
A.Se的原子结构示意图: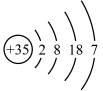 |
B.基态铬原子的价电子排布式: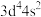 |
C.基态氧原子的轨道表示式: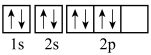 |
D.铜氨配离子的结构式: |
您最近一年使用:0次
2023-10-04更新
|
343次组卷
|
2卷引用:广东省广州大学附属中学2023-2024学年高二下学期开学测化学试题
名校
解题方法
5 . 下列说法正确的是
| A.多电子原子不同能级能量高低的比较中:4s>3d>3p |
| B.某元素基态原子的最外层电子数是次外层电子数的1.5倍,,则该元素基态原子的核外电子排布式为:1s22s22p1 |
| C.基态K原子的核外电子的空间运动状态共有19种 |
D.根据洪特规则可知1s22s22p2的价层电子的轨道表示为: |
您最近一年使用:0次
名校
解题方法
6 . 下列化学用语或图示表达正确的是
A. 、 、 、 、 都是碱性氧化物 都是碱性氧化物 |
B.顺-2-丁烯的结构简式: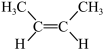 |
C.中子数为10的氧原子: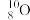 |
D.基态 的价层电子的轨道表示式: 的价层电子的轨道表示式: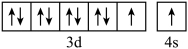 |
您最近一年使用:0次
2023-08-08更新
|
262次组卷
|
3卷引用:广东省湛江市第一中学2023-2024学年高三上学期开学考试化学试题
名校
7 . 反应 用于捕捉废气中
用于捕捉废气中 ,有关化学用语正确的是
,有关化学用语正确的是
 用于捕捉废气中
用于捕捉废气中 ,有关化学用语正确的是
,有关化学用语正确的是A.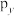 轨道的电子云轮廓图: 轨道的电子云轮廓图: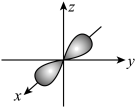 |
B. 的结构示意图: 的结构示意图: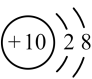 |
C.基态C原子最外层电子的轨道表示式: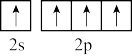 |
D. 的空间填充模型: 的空间填充模型: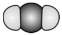 |
您最近一年使用:0次
2023-08-05更新
|
354次组卷
|
5卷引用:广东省梅州市大埔县虎山中学2023-2024学年高二下学期开学化学试题
广东省梅州市大埔县虎山中学2023-2024学年高二下学期开学化学试题河北省保定市定州市2022-2023学年高二上学期期末考试化学试题(已下线)期末押题卷02-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)山东省泰安市2023-2024学年高二上学期第四次调研测试化学试题山东省济南市历城第二中学2023-2024学年高二上学期期末化学模拟试题
名校
8 . 四钼酸铵[(NH4)2 Mo4O13·2H2O]微溶于水,常用作石油工业的催化剂、微量元素肥料、织物防火及阻燃剂等。从富钼精矿中(主要成分为MoS2,还含有少量NiS、SiO2、As2O3)制备四钼酸铵的一种流程如图所示:

已知:“浸出”所得浸出液中主要存在的离子为Na+、OH-、MoO 、SO
、SO 、SiO
、SiO 、AsO
、AsO
(1)钼(Mo)在周期表中位于第五周期ⅥB族,画出钼的价电子轨道表示式____________
(2)氧化焙烧时,MoS2发生反应的化学方程式为__________________________________
(3)“滤渣Ⅱ”的主要成分为__________________ (写化学式)
(4)实验室进行萃取分液操作时,需要用到的玻璃仪器主要有_________ 、_________ 。
(5)“萃取”的原理为2R3N(叔胺N-235)+2H++MoO ⇌(R3NH)2MoO4 ,则“反萃取”工序中的试剂X最适宜选用
⇌(R3NH)2MoO4 ,则“反萃取”工序中的试剂X最适宜选用__________ (填选项字母)
a.NaOH溶液 b.氨水 c.稀硫酸 d.(NH4)2SO4溶液
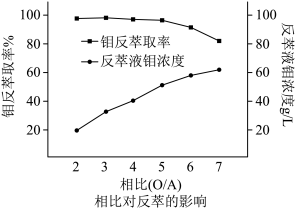
(6)在“反萃取”工序中相比(有机相与水相的体积比)如图所示。则反萃取时应选择的相比为____________ 。
(7)在“酸沉结晶”前,钼酸铵溶液中c(MoO )=0.80mol·L-1,c(SO
)=0.80mol·L-1,c(SO )=0.05mol·L-1,在结晶前应加入Ba(OH)2固体以除去溶液中的SO
)=0.05mol·L-1,在结晶前应加入Ba(OH)2固体以除去溶液中的SO 。当BaMoO4开始沉淀时,SO
。当BaMoO4开始沉淀时,SO 的去除率是
的去除率是__________ %(保留1位小数)。[Ksp(BaSO4)=1.1×10-10、Ksp(BaMoO4)=4.0×10-8,忽略溶液体积变化]

已知:“浸出”所得浸出液中主要存在的离子为Na+、OH-、MoO
 、SO
、SO 、SiO
、SiO 、AsO
、AsO
(1)钼(Mo)在周期表中位于第五周期ⅥB族,画出钼的价电子轨道表示式
(2)氧化焙烧时,MoS2发生反应的化学方程式为
(3)“滤渣Ⅱ”的主要成分为
(4)实验室进行萃取分液操作时,需要用到的玻璃仪器主要有
(5)“萃取”的原理为2R3N(叔胺N-235)+2H++MoO
 ⇌(R3NH)2MoO4 ,则“反萃取”工序中的试剂X最适宜选用
⇌(R3NH)2MoO4 ,则“反萃取”工序中的试剂X最适宜选用a.NaOH溶液 b.氨水 c.稀硫酸 d.(NH4)2SO4溶液
(6)在“反萃取”工序中相比(有机相与水相的体积比)如图所示。则反萃取时应选择的相比为

(7)在“酸沉结晶”前,钼酸铵溶液中c(MoO
 )=0.80mol·L-1,c(SO
)=0.80mol·L-1,c(SO )=0.05mol·L-1,在结晶前应加入Ba(OH)2固体以除去溶液中的SO
)=0.05mol·L-1,在结晶前应加入Ba(OH)2固体以除去溶液中的SO 。当BaMoO4开始沉淀时,SO
。当BaMoO4开始沉淀时,SO 的去除率是
的去除率是
您最近一年使用:0次
名校
9 . 合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)基态N原子中,能量最高的电子的电子云在空间有___________ 个伸展方向,原子轨道呈___________ 形。
(2) 分子中,N、H电负性大小顺序为
分子中,N、H电负性大小顺序为___________ 。从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为___________ 。
(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有 、
、 、CaO、MgO、
、CaO、MgO、 等氧化物中的几种。
等氧化物中的几种。
①Cr原子的价电子排布图为___________ 。
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________ 。
(4)目前合成氨通常采用的压强为10MPa-30MPa、温度为400-500℃,十分耗能。我国科研人员研制出了“Fe-LiH”等催化剂,温度,压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①第三电离能
___________ 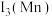 (填“>”或“<”),原因是
(填“>”或“<”),原因是___________ 。
②比较 与
与 的半径大小关系:
的半径大小关系: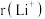
___________  。(填“>”或“<”)
。(填“>”或“<”)
(1)基态N原子中,能量最高的电子的电子云在空间有
(2)
 分子中,N、H电负性大小顺序为
分子中,N、H电负性大小顺序为(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
 、
、 、CaO、MgO、
、CaO、MgO、 等氧化物中的几种。
等氧化物中的几种。①Cr原子的价电子排布图为
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
(4)目前合成氨通常采用的压强为10MPa-30MPa、温度为400-500℃,十分耗能。我国科研人员研制出了“Fe-LiH”等催化剂,温度,压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①第三电离能

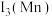 (填“>”或“<”),原因是
(填“>”或“<”),原因是②比较
 与
与 的半径大小关系:
的半径大小关系: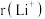
 。(填“>”或“<”)
。(填“>”或“<”)
您最近一年使用:0次
2022-11-12更新
|
826次组卷
|
4卷引用:广东番禺中学2022-2023学年高二下学期科开学考试化学试题
10 . 在牙膏中添加氟化物能起到预防龋齿的作用,原理是生成了更能抵抗酸蚀的氟磷灰石 ,下列有关化学用语正确的是
,下列有关化学用语正确的是
 ,下列有关化学用语正确的是
,下列有关化学用语正确的是A.基态F原子价电子排布图: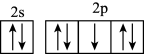 | B. 的结构示意图: 的结构示意图: |
C.中子数为16的磷核素: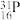 | D. 的电子式为: 的电子式为: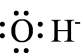 |
您最近一年使用:0次
2022-05-12更新
|
496次组卷
|
4卷引用:广东省信宜市第二中学2022-2023学年高三上学期开学考试化学试题



