名校
1 . 下列化学用语正确的是
A. 的结构示意图: 的结构示意图: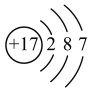 |
B.基态钙原子的简化电子排布式: |
C. 的空间填充模型: 的空间填充模型: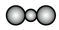 |
D.基态氧原子的核外电子轨道表示式: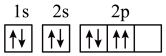 |
您最近一年使用:0次
解题方法
2 . 《天工开物》记载火药涉及的主要反应为: .下列相关微粒的化学用语正确的是
.下列相关微粒的化学用语正确的是
 .下列相关微粒的化学用语正确的是
.下列相关微粒的化学用语正确的是A.中子数为8的碳原子: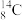 |
B.基态 原子 原子 能级电子轨道表示式: 能级电子轨道表示式: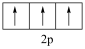 |
C. 的结构示意图: 的结构示意图: |
D.钾原子价层电子排布式: |
您最近一年使用:0次
3 . 如图是元素周期表中的前四周期,回答下列问题:

(1)a的简单氢化物的实验室制备方程式为:___________ 。
(2)a、f、g的最高价氧化物对应水化物中酸性最强的是___________ 。
(3)b元素的正二价离子的核外价电子轨道表示式是___________ 。
(4)b、e两种元素的第四电离能大小关系为_________ (填元素符号),原因是___________ 。
(5)已知元素c、f的最简单的化合物中共用电子对偏向f,元素c、g的最简单的化合物中共用电子对偏向c,则元素c、f、g的电负性由大到小的顺序为___________ (填元素符号)。

(1)a的简单氢化物的实验室制备方程式为:
(2)a、f、g的最高价氧化物对应水化物中酸性最强的是
(3)b元素的正二价离子的核外价电子轨道表示式是
(4)b、e两种元素的第四电离能大小关系为
(5)已知元素c、f的最简单的化合物中共用电子对偏向f,元素c、g的最简单的化合物中共用电子对偏向c,则元素c、f、g的电负性由大到小的顺序为
您最近一年使用:0次
解题方法
4 . 锰酸锂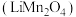 是锂电池的正极材料,有望取代
是锂电池的正极材料,有望取代 。一种以废旧电池正极材料(主要成分为
。一种以废旧电池正极材料(主要成分为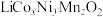 ,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备
,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备 的流程如下:
的流程如下:
(1)Ni位于元素周期表中_______ 区;基态Mn原子的价层电子轨道表示式为________ 。
(2)“灼烧”的目的是________ 。
(3)根据“酸浸”前后物质价态的变化,推测双氧水的作用是________ 。
(4)“沉锰”过程中,溶液先变为紫红色,一段时间后紫红色褪去。溶液变为紫红色的原因是___________ (用离子方程式表示,加入 溶液之前,锰以
溶液之前,锰以 形式存在)。“紫红色褪去”后,还可能有的实验现象是
形式存在)。“紫红色褪去”后,还可能有的实验现象是___________ 。
(5) 材料在脱锂过程中形成的某种晶体为六方晶系,结构如图,晶胞底面边长为
材料在脱锂过程中形成的某种晶体为六方晶系,结构如图,晶胞底面边长为 、高为
、高为 ,
,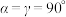 ,
,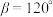 ,设
,设 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。___________ 。
②该晶体的密度为___________  。
。
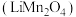 是锂电池的正极材料,有望取代
是锂电池的正极材料,有望取代 。一种以废旧电池正极材料(主要成分为
。一种以废旧电池正极材料(主要成分为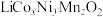 ,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备
,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备 的流程如下:
的流程如下: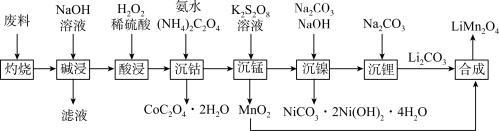
(1)Ni位于元素周期表中
(2)“灼烧”的目的是
(3)根据“酸浸”前后物质价态的变化,推测双氧水的作用是
(4)“沉锰”过程中,溶液先变为紫红色,一段时间后紫红色褪去。溶液变为紫红色的原因是
 溶液之前,锰以
溶液之前,锰以 形式存在)。“紫红色褪去”后,还可能有的实验现象是
形式存在)。“紫红色褪去”后,还可能有的实验现象是(5)
 材料在脱锂过程中形成的某种晶体为六方晶系,结构如图,晶胞底面边长为
材料在脱锂过程中形成的某种晶体为六方晶系,结构如图,晶胞底面边长为 、高为
、高为 ,
,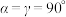 ,
,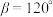 ,设
,设 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
②该晶体的密度为
 。
。
您最近一年使用:0次
5 . 下列化学用语表示正确的是
A.基态钠离子的电子排布图为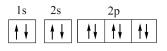 |
B.次氯酸的电子式为 |
C.含18个中子的氯原子的符号为 |
D.空间结构模型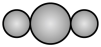 可以表示 可以表示 或 或 |
您最近一年使用:0次
6 . 以软锰矿与黄铁矿为主要原料制备高品质 的工艺流程:
的工艺流程:
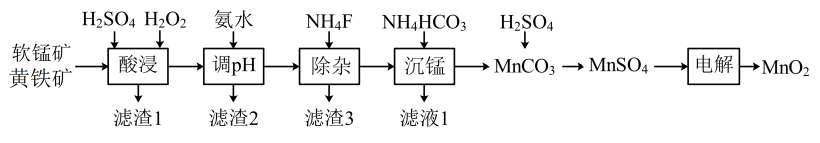
已知:①软锰矿与黄铁矿的主要成分分别为 、
、 ,还均含少量Fe、Ca、Mg、Al、Si等元素的氧化物;
,还均含少量Fe、Ca、Mg、Al、Si等元素的氧化物;
②该工艺条件下,相关金属离子形成氢氧化物沉淀的pH:
回答下列问题:
(1)基态 的价层电子排布图为
的价层电子排布图为___________ 。
(2)“酸浸”过程中,为提高反应速率可以采取的措施有___________ (写一条)。
(3)“酸浸”加入 后,主要反应的离子方程式:
后,主要反应的离子方程式:
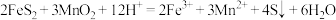

滤渣1的主要成分为S、___________ ,加入 后迅速产生大量气泡,可减少滤渣1在矿粉表面的附着,有利于酸浸。分析迅速产生气泡的原因:
后迅速产生大量气泡,可减少滤渣1在矿粉表面的附着,有利于酸浸。分析迅速产生气泡的原因:___________ 。
(4)“调pH”操作中需调节溶液pH范围为4.7~6.0,此时滤渣2的主要成分为___________ (填化学式)。
(5)“沉锰”步骤发生主要反应的离子方程式为___________ 。
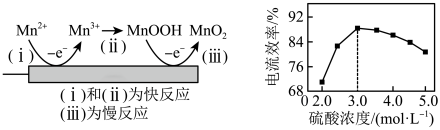
(6)利用惰性电极电解 体系获得
体系获得 的机理如图所示,硫酸浓度与电流效率η的关系如图所示。硫酸浓度超过
的机理如图所示,硫酸浓度与电流效率η的关系如图所示。硫酸浓度超过 时,电流效率η降低的原因是
时,电流效率η降低的原因是___________ 。( )
)
 的工艺流程:
的工艺流程:
已知:①软锰矿与黄铁矿的主要成分分别为
 、
、 ,还均含少量Fe、Ca、Mg、Al、Si等元素的氧化物;
,还均含少量Fe、Ca、Mg、Al、Si等元素的氧化物;②该工艺条件下,相关金属离子形成氢氧化物沉淀的pH:
| 金属离子 |  |  |  |  |  |
| 开始沉淀的pH | 6.9 | 1.9 | 6.6 | 9.1 | 3.4 |
沉淀完全( )的pH )的pH | 8.3 | 3.2 | 10.1 | 10.9 | 4.7 |
(1)基态
 的价层电子排布图为
的价层电子排布图为(2)“酸浸”过程中,为提高反应速率可以采取的措施有
(3)“酸浸”加入
 后,主要反应的离子方程式:
后,主要反应的离子方程式: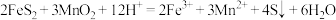

滤渣1的主要成分为S、
 后迅速产生大量气泡,可减少滤渣1在矿粉表面的附着,有利于酸浸。分析迅速产生气泡的原因:
后迅速产生大量气泡,可减少滤渣1在矿粉表面的附着,有利于酸浸。分析迅速产生气泡的原因:(4)“调pH”操作中需调节溶液pH范围为4.7~6.0,此时滤渣2的主要成分为
(5)“沉锰”步骤发生主要反应的离子方程式为
(6)利用惰性电极电解
 体系获得
体系获得 的机理如图所示,硫酸浓度与电流效率η的关系如图所示。硫酸浓度超过
的机理如图所示,硫酸浓度与电流效率η的关系如图所示。硫酸浓度超过 时,电流效率η降低的原因是
时,电流效率η降低的原因是 )
)
您最近一年使用:0次
7 . 符号表征是化学学习不可或缺的媒介和工具,如水的分子式H2O,氢氧根离子符号OH-。下列化学用语或图示表达正确的是
A.NH3的VSEPR模型为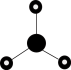 |
B.HClO的电子式为 |
C.2pz电子云图为 |
D.基态氧原子的电子排布图为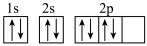 |
您最近一年使用:0次
2024-01-18更新
|
258次组卷
|
4卷引用:广东省潮州市2023-2024学年高三上学期期末教学质量检测化学试题
解题方法
8 . 下列化学用语表达正确的是
A.氮原子的L层电子轨道表示式: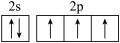 | B.质量数为127的碘原子: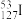 |
C.K+的结构示意图: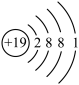 | D.HClO的电子式: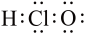 |
您最近一年使用:0次
名校
解题方法
9 . 下列表达式正确的是
A.基态氮原子的价电子轨道表示式为 |
B.基态As原子的电子排布式为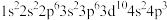 |
C.基态溴原子的价电子排布式为 |
D.基态 的价电子排布式为 的价电子排布式为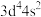 |
您最近一年使用:0次
名校
解题方法
10 . 下列叙述中,正确的是
A.电石( )和储氢材料氢化钙( )和储氢材料氢化钙( )都存在非极性键 )都存在非极性键 |
B.该电子排布图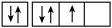 违背了泡利原理 违背了泡利原理 |
| C.核酸可以看作磷酸、戊糖和碱基通过一定方式结合而成的生物大分子 |
D. 属于共价晶体,熔化时需破坏共价键和分子间作用力 属于共价晶体,熔化时需破坏共价键和分子间作用力 |
您最近一年使用:0次
2023-07-13更新
|
228次组卷
|
2卷引用:广东省广州市番禺区2022-2023学年高二下学期期末教学质量监测化学试题



