名校
解题方法
1 . 下列状态的Li原子中,能量最低的是
A.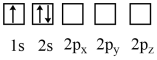 | B.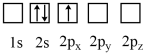 |
C.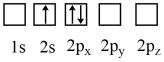 | D.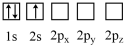 |
您最近一年使用:0次
2022-04-22更新
|
713次组卷
|
4卷引用:陕西省陕西师范大学附属中学2020-2021学年高二下学期期中考试化学试题
2 . A、B、C、D、E六种元素:
(1)A元素基态原子最外层有3个未成对电子,次外层有2个电子。该元素在周期表中的位置是_______ 。基态原子电子排布式式_______ 。
(2)B元素是周期表前四周期中未成对电子数最多的元素,B元素名称为_______ ,B的价电子排布式_______ 。
(3)C元素的+3价离子的3d能级半充满,C元素位于周期表中_______ 区,具体位置是_______ ,C元素的+3价离子的符号_______ ,该离子结构示意图_______ ,C元素的核外电子排布式_______ 。
(4)D元素基态原子M层全充满,N层没有成对电子,只有一个未成对电子,该元素简化电子排布式_______ ,位于周期表_______ 区,价电子排布图_______ 。
(5)E元素的最外层电子排布式为nsnnpn+1,则n等于_______ ,原子中能量最高的是_______ 电子。
(1)A元素基态原子最外层有3个未成对电子,次外层有2个电子。该元素在周期表中的位置是
(2)B元素是周期表前四周期中未成对电子数最多的元素,B元素名称为
(3)C元素的+3价离子的3d能级半充满,C元素位于周期表中
(4)D元素基态原子M层全充满,N层没有成对电子,只有一个未成对电子,该元素简化电子排布式
(5)E元素的最外层电子排布式为nsnnpn+1,则n等于
您最近一年使用:0次
3 . 下列描述中正确的是
A.氮原子的价电子排布图: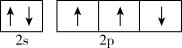 |
| B.2p和3p轨道形状均为哑铃形,能量也相等 |
C.价电子排布为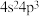 的元素位于第四周期ⅤA族,是p区元素 的元素位于第四周期ⅤA族,是p区元素 |
D.钠原子由 时,原子释放能量,由基态转化成激发态 时,原子释放能量,由基态转化成激发态 |
您最近一年使用:0次
2022-03-16更新
|
403次组卷
|
23卷引用:辽宁省清原满族自治县第二高级中学2020-2021学年高二下学期期中考试化学试题
辽宁省清原满族自治县第二高级中学2020-2021学年高二下学期期中考试化学试题安徽省蚌埠市第二中学2016-2017学年高二下学期期中考试化学试题江苏省南京师范大学苏州实验学校2019-2020学年高二上学期期中考试化学试题福建省三明市五县2021-2022学年高二下学期联合质检考试(期中)化学试题新疆精河县高级中学2021-2022学年高二下学期期中考试化学试题宁夏育才中学2022-2023学年高二下学期5月期中考试化学试题湖北省武汉西藏中学2023-2024学年高二下学期5月期中考试化学试题2014-2015宁夏银川市唐徕回民中学高二下学期3月月考化学试卷2015届上海市青浦区高考二模化学试卷吉林省吉林市第五十五中学2018-2019学年高二下学期3月月考化学试题新疆石河子第二中学2018-2019学年高二下学期期末考试化学试题2020届高三化学选修三二轮专题复习——能级、能层、原子轨道第1章 原子结构——B拓展区综合拓展(鲁科版选修3)安微蚌埠二中2019-2020学年高二4月检测化学试题湖北省荆州市八县市2021-2022学年高二上学期期末质量检测化学试题湖北省荆门市2021-2022学年高二上学期期末质量检测化学试题重庆市第七中学2021-2022学年高二下学期第一次月考化学试题宁夏银川市景博中学2021-2022学年高二下学期第二次月考化学试题安徽省宿州市第二中学2022-2023学年高二下学期第一次月考化学试题安徽省蚌埠第二中学2022-2023学年高二下学期第一次月考化学试题安徽省安庆市第一中学2022-2023学年高二下学期第一次月考化学试题安徽省亳州市第一中学2022-2023学年高二下学期第一次月考化学试题广东番禺中学2022-2023学年高二下学期科开学考试化学试题
解题方法
4 . 下列有关化学用语表述或性质比较正确的是
A.基态氧原子核外价电子排布轨道表示式 |
| B.基态氧原子核外有8种空间运动状态的电子 |
C.用原子轨道描述氢分子中化学键的形成: |
| D.第三周期的元素中,第一电离能介于Mg和S之间只有1种元素 |
您最近一年使用:0次
5 . FeCl3可通过反应3FeCl2+HNO3+3HCl→3FeCl3+NO↑+2H2O制得。完成下列填空:
(1)上述反应式中由三个原子组成的极性分子,其结构式为____ 。
(2)限于上述反应式,原子最外层有3个未成对电子的主族元素是____ (填写名称),其最外层的电子轨道表示式为____ ;与它同周期、非金属性比它强的元素有____ 、____ (填写元素符号),请写一个能说明它们非金属性较强弱的化学反应方程式:____ 。
(3)向FeCl2溶液中滴加氯水也可制得FeCl3,请写出反应的化学方程式:____ 。
(4)FeCl3浓溶液可用于蚀刻金属铜制作电路板。写出该反应的离子方程式____ 。实验室里,某同学将FeCl3(s)置于烧杯中,加水溶解配制溶液。为了加速固体溶解,边搅拌边加热,发现烧杯中出现浑浊。请用平衡移动原理解释出现浑浊的原因____ 。为防止出现浑浊现象,可适量加入____ 。
(1)上述反应式中由三个原子组成的极性分子,其结构式为
(2)限于上述反应式,原子最外层有3个未成对电子的主族元素是
(3)向FeCl2溶液中滴加氯水也可制得FeCl3,请写出反应的化学方程式:
(4)FeCl3浓溶液可用于蚀刻金属铜制作电路板。写出该反应的离子方程式
您最近一年使用:0次
6 . 下列化学用语表达正确的是
A.SO3的VSEPR模型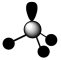 |
B.铍原子最外层原子轨道示意图: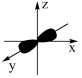 |
| C.铬原子价电子排布式:3d54s1 |
D.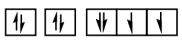 违反了洪特规则 违反了洪特规则 |
您最近一年使用:0次
2021-12-30更新
|
444次组卷
|
4卷引用:山东省威海乳山市2021-2022学年高二上学期期中考试化学试题
山东省威海乳山市2021-2022学年高二上学期期中考试化学试题(已下线)2.2.1 分子结构的测定和多样性 价层电子对互斥模型-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)广东省梅州市大埔县实验中学2021-2022学年高二下学期第一次段考(4月)化学试题山东省滨州市阳信县第一中学2023-2024学年高二上学期第三次月考化学试题
名校
7 . 已知A、B、C、D、E是原子序数依次增大的前四周期元素,其元素性质成原子结构如表:
下列说法错误的是
| A | 原子核外电子分占3个不同能级,且每个能级上排布的电子数相同 |
| B | 原子最高能级的不同轨道都有电子,且自旋方向相同 |
| C | 电子排布式为 |
| D | 位于周期表中第4纵列 |
| E | 基态原子M层全充满,N层只有一个电子 |
| A.B有3个未成对电子 |
| B.A、B、C三种元素的原子半径由大到小的顺序:A>B>C |
C.D元素基态原子的价电子排布图为: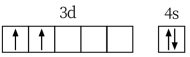 |
D.E的基态原子的简化电子排布式为: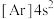 |
您最近一年使用:0次
2021-12-15更新
|
562次组卷
|
3卷引用:辽宁省辽河油田第一高级中学2021-2022学年高二上学期期中考试化学试题
辽宁省辽河油田第一高级中学2021-2022学年高二上学期期中考试化学试题(已下线)第十一单元 物质结构与性质(A卷 新题基础练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)福建省永安市第三中学高中校2022-2023学年高三下学期第一次月考(3月)化学试题
8 . 下列说法不正确的是
| A.基态原子的核外电子填充在6个轨道中的元素有两种 |
B.碳原子的核外电子轨道表示式: |
| C.基态钾离子(K+),电子占据的最高能级共有3个原子轨道,其形状是哑铃形 |
| D.基态铜原子的电子占有5种能量不同的原子轨道 |
您最近一年使用:0次
2021-12-15更新
|
1326次组卷
|
5卷引用:辽宁省辽河油田第一高级中学2021-2022学年高二上学期期中考试化学试题
辽宁省辽河油田第一高级中学2021-2022学年高二上学期期中考试化学试题(已下线)第1.1.3讲 泡利原理、洪特规则、能量最低原理 -2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)(已下线)1.1.2 构造原理与电子排布式-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)黑龙江省哈尔滨市宾县第二中学2021-2022学年高二下学期期末考试化学试题(已下线)1.1.2 电子云与原子轨道-同步学习必备知识
名校
9 . 已知A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素,E是第四周期的p区元素且最外层只有2对成对电子,F元素的基态原子第四能层只有一个电子,其它能层均已充满电子。G元素最大能层符号为N,有4个单电子。
(1)基态E原子的价电子排布图___________ 。
(2)B、C、D三元素第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3) 中心原子为
中心原子为___________ 杂化,空间构型为___________ ,键角___________  (用“>、<、=”填空)。
(用“>、<、=”填空)。
(4) 与C2为等电子体结构相似,1mol
与C2为等电子体结构相似,1mol 中含有
中含有 键的数目为
键的数目为___________ 。
(5)D、E元素最简单氢化物的稳定性___________ (填化学式)。
(6)基态G2+离子的电子排布式为:___________ 。
(1)基态E原子的价电子排布图
(2)B、C、D三元素第一电离能由大到小的顺序为
(3)
 中心原子为
中心原子为 (用“>、<、=”填空)。
(用“>、<、=”填空)。(4)
 与C2为等电子体结构相似,1mol
与C2为等电子体结构相似,1mol 中含有
中含有 键的数目为
键的数目为(5)D、E元素最简单氢化物的稳定性
(6)基态G2+离子的电子排布式为:
您最近一年使用:0次
10 . 2019年诺贝尔化学奖授予三位开发锂离子电池的科学家。TiS2、LiCoO2和LiMnO2等都是锂离子电池的载体。回答下列问题:
(1)基态Co原子中电子占据的最高能层符号为_______ ,价电子轨道排布图为_______ 。
(2)已知第三电离能的数据:I3(Mn)=3246 kJ·mol−1,I3(Fe)=2957 kJ·mol−1。I3(Mn)>I3(Fe)的主要原因____________________________________________________ 。
(3)Co3+、Co2+能与NH3、H2O、SCN-等配体形成配合物。
①1 mol [Co(NH3)6]3+含___________ mol σ键。
②SCN−的结构式为[S=C=N]−, SCN−与Co2+形成的配离子中配位原子是____ (填元素符号)。
(4)工业上采用电解熔融LiCl制备金属Li,Na还原TiCl4制备Ti。已知LiCl、TiCl4的熔点分别为605 ℃、-24 ℃,它们的熔点相差很大,其主要原因是____________________ 。
(5)金属Ti中,Ti原子采取________ 堆积,Ti的原子半径为r nm,则晶胞的高为_____ nm。
(1)基态Co原子中电子占据的最高能层符号为
(2)已知第三电离能的数据:I3(Mn)=3246 kJ·mol−1,I3(Fe)=2957 kJ·mol−1。I3(Mn)>I3(Fe)的主要原因
(3)Co3+、Co2+能与NH3、H2O、SCN-等配体形成配合物。
①1 mol [Co(NH3)6]3+含
②SCN−的结构式为[S=C=N]−, SCN−与Co2+形成的配离子中配位原子是
(4)工业上采用电解熔融LiCl制备金属Li,Na还原TiCl4制备Ti。已知LiCl、TiCl4的熔点分别为605 ℃、-24 ℃,它们的熔点相差很大,其主要原因是
(5)金属Ti中,Ti原子采取
您最近一年使用:0次



