名校
1 . 磷和砷的相关化合物在化工、医药、材料等领域有着广泛应用。回答下列问题:
(1)红磷是巨型共价分子,无定形结构,下列方法能证明红磷是非晶体的是___________。
(2)第一电离能介于Al、P之间的第三周期元素有___________ 种。
(3)如图所示,每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是___________ 。

(4)黑磷是新型二维半导体材料,具有片层结构(如图所示),P在元素周期表分区中属于___________ 区,层与层之间的相互作用力为___________ 。

(5)N、P、As、Sb均是第ⅤA族的元素,As原子的逐级电离能数据如下:
第五电离能与第六电离能相差较大的原因:___________ 。
(1)红磷是巨型共价分子,无定形结构,下列方法能证明红磷是非晶体的是___________。
| A.质谱法 | B.原子发射光谱法 |
| C.核磁共振谱法 | D.X射线衍射法 |
(3)如图所示,每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

(4)黑磷是新型二维半导体材料,具有片层结构(如图所示),P在元素周期表分区中属于

(5)N、P、As、Sb均是第ⅤA族的元素,As原子的逐级电离能数据如下:
| 第一电离能 | 第二电离能 | 第三电离能 | 第四电离能 | 第五电离能 | 第六电离能 |
| 947.0 | 1 798 | 2 735 | 4 837 | 6 043 | 12 310 |
第五电离能与第六电离能相差较大的原因:
您最近一年使用:0次
2 . 碳是地球上组成生命的最基本元素之一。不仅能形成丰富多彩的有机化合物,还能形成多种无机化合物,碳及其化合物的用途广泛。根据要求回答下列问题:
(1)在基态14C原子中,核外存在_______ 对自旋相反的电子;第二周期的元素中,第一电离能介于B和C之间的是_______ ( 写元素符号)。
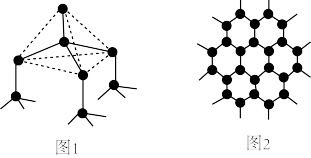
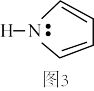
(2)下图中分别代表了碳单质的两种常见晶体,图1晶体中C原子的杂化方式为_______ ,图2晶体中,每个六元环占有_______ 个 C原子。
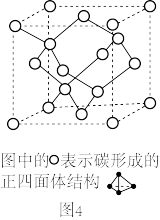
(3)碳可以形成多种有机化合物,如图3所示是一种吡咯的结构,分子中所有原子都在一个平面上。吡咯中所有元素的电负性由大到小的顺序为_______ 。
(4)碳可形成CO、CO2等多种无机化合物,在CO转化成CO2的反应过程中,下列说法正确的是_______。
(5)碳酸盐在一定温度下会发生分解生成二氧化碳和对应氧化物,实验证明:碳酸盐的阳离子不同分解温度不同,如表所示:
随着阳离子半径的增大,碳酸盐的分解温度逐步升高,原因是_______ 。
(6)在2017年,中外科学家团队共同合成了碳的一种新型同素异形体:T-碳。 T-碳的结构是:将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代,形成碳的一种新型三维立方晶体结构,如图4。已知T-碳晶胞参数为apm,阿伏加德罗常数为NA,则T -碳的密度为_______ g/cm3(列出计算式)。
(1)在基态14C原子中,核外存在
(2)下图中分别代表了碳单质的两种常见晶体,图1晶体中C原子的杂化方式为

(3)碳可以形成多种有机化合物,如图3所示是一种吡咯的结构,分子中所有原子都在一个平面上。吡咯中所有元素的电负性由大到小的顺序为

(4)碳可形成CO、CO2等多种无机化合物,在CO转化成CO2的反应过程中,下列说法正确的是_______。
| A.分子中孤对电子数不变 | B.分子极性发生变化 | C.原子间成键方式改变 | D.分子间作用力减弱 |
| 碳酸盐 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
| 热分解温度/°C | 402 | 900 | 1 172 | 1360 |
| 阳离子半径/pm | 66 | 99 | 112 | 135 |
(6)在2017年,中外科学家团队共同合成了碳的一种新型同素异形体:T-碳。 T-碳的结构是:将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代,形成碳的一种新型三维立方晶体结构,如图4。已知T-碳晶胞参数为apm,阿伏加德罗常数为NA,则T -碳的密度为

您最近一年使用:0次
名校
解题方法
3 . 氢能被视为21世纪最具发展潜力的清洁能源,开发高效储氢材料是氢能利用的重要研究方向。
(1)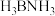 是一种潜在的储氢材料,其中N原子的价电子排布图为
是一种潜在的储氢材料,其中N原子的价电子排布图为______ 。
(2)制备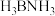 的化学反应为
的化学反应为 。其中
。其中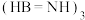 是六元环状物质,与其互为等电子体的有机物分子式为
是六元环状物质,与其互为等电子体的有机物分子式为______ 。 、
、 、
、 的键角由大到小的顺序为
的键角由大到小的顺序为______ 。B、C、N、O第一电离能由大到小的顺序为______ 。
(3) 是新型环烯类储氢材料,研究证明其分子呈平面结构,如图所示。
是新型环烯类储氢材料,研究证明其分子呈平面结构,如图所示。

① 分子中C原子和S原子的杂化轨道类型分别为
分子中C原子和S原子的杂化轨道类型分别为_____ 。
②测得 中碳硫键的键长介于C-S键和
中碳硫键的键长介于C-S键和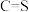 键之间,其原因可能是
键之间,其原因可能是______ 。
(4)某种铜银合金晶体具有储氢功能,它是面心立方最密堆积结构,Cu原子位于面心,Ag原子位于顶点,H原子可进入由Cu原子和Ag原子构成的四面体空隙中。若将Cu、Ag原子等同看待,该晶体储氢后的晶胞结构与 (如图)相似,该晶体储氢后的化学式为
(如图)相似,该晶体储氢后的化学式为______ 。

(5) 是金属氢化物储氢材料,其晶胞如图所示,已知该晶体的密度为
是金属氢化物储氢材料,其晶胞如图所示,已知该晶体的密度为 ,则该晶胞的体积为
,则该晶胞的体积为___________  (用含ρ、NA的代数式表示)。
(用含ρ、NA的代数式表示)。

(1)
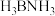 是一种潜在的储氢材料,其中N原子的价电子排布图为
是一种潜在的储氢材料,其中N原子的价电子排布图为(2)制备
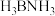 的化学反应为
的化学反应为 。其中
。其中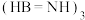 是六元环状物质,与其互为等电子体的有机物分子式为
是六元环状物质,与其互为等电子体的有机物分子式为 、
、 、
、 的键角由大到小的顺序为
的键角由大到小的顺序为(3)
 是新型环烯类储氢材料,研究证明其分子呈平面结构,如图所示。
是新型环烯类储氢材料,研究证明其分子呈平面结构,如图所示。
①
 分子中C原子和S原子的杂化轨道类型分别为
分子中C原子和S原子的杂化轨道类型分别为②测得
 中碳硫键的键长介于C-S键和
中碳硫键的键长介于C-S键和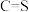 键之间,其原因可能是
键之间,其原因可能是(4)某种铜银合金晶体具有储氢功能,它是面心立方最密堆积结构,Cu原子位于面心,Ag原子位于顶点,H原子可进入由Cu原子和Ag原子构成的四面体空隙中。若将Cu、Ag原子等同看待,该晶体储氢后的晶胞结构与
 (如图)相似,该晶体储氢后的化学式为
(如图)相似,该晶体储氢后的化学式为
(5)
 是金属氢化物储氢材料,其晶胞如图所示,已知该晶体的密度为
是金属氢化物储氢材料,其晶胞如图所示,已知该晶体的密度为 ,则该晶胞的体积为
,则该晶胞的体积为 (用含ρ、NA的代数式表示)。
(用含ρ、NA的代数式表示)。
您最近一年使用:0次
2021-10-14更新
|
271次组卷
|
2卷引用:广东省广州市第六中学2022届高三第二次月考化学试题
名校
解题方法
4 . 下图为一种结构有趣的“糖葫芦”分子,其中 、
、 、
、 、
、 四种元素位于同一主族的相邻周期,
四种元素位于同一主族的相邻周期, 的电负性大于
的电负性大于 ,工业上利用沸点差异从空气中分离出
,工业上利用沸点差异从空气中分离出 的单质。
的单质。 是短周期元素,
是短周期元素, 与
与 的价电子数之和与
的价电子数之和与 的质子数相同,
的质子数相同,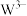 与
与 的电子结构相同。下列说法错误的是
的电子结构相同。下列说法错误的是

 、
、 、
、 、
、 四种元素位于同一主族的相邻周期,
四种元素位于同一主族的相邻周期, 的电负性大于
的电负性大于 ,工业上利用沸点差异从空气中分离出
,工业上利用沸点差异从空气中分离出 的单质。
的单质。 是短周期元素,
是短周期元素, 与
与 的价电子数之和与
的价电子数之和与 的质子数相同,
的质子数相同,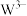 与
与 的电子结构相同。下列说法错误的是
的电子结构相同。下列说法错误的是
| A.分子中W、Y的杂化轨道类型不相同 |
B.第一电离能: |
C. 的氢化物 的氢化物 的VSEPR模型为四面体形 的VSEPR模型为四面体形 |
D.简单离子半径: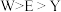 |
您最近一年使用:0次
7日内更新
|
246次组卷
|
3卷引用:广东省华南师范大学附属中学2024届高三下学期高考适应性练习(4月)化学试题
5 . 近期,营养快线中烟酰胺营养素参考值达7%冲上热搜,烟酰胺是一种维生素 ,具有调节血脂、改善皮肤、增强记忆等多种功效,其结构简式如图所示。下列关于烟酰胺的说法不正确的是
,具有调节血脂、改善皮肤、增强记忆等多种功效,其结构简式如图所示。下列关于烟酰胺的说法不正确的是
 ,具有调节血脂、改善皮肤、增强记忆等多种功效,其结构简式如图所示。下列关于烟酰胺的说法不正确的是
,具有调节血脂、改善皮肤、增强记忆等多种功效,其结构简式如图所示。下列关于烟酰胺的说法不正确的是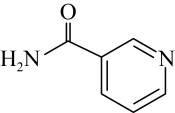
A.C、N、O的第一电离能: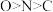 | B.环上的一氯代物有4种(不考虑立体异构) |
C.所有的碳原子都是 杂化 杂化 | D. 烟酰胺最多能与 烟酰胺最多能与 反应 反应 |
您最近一年使用:0次
2024-05-28更新
|
375次组卷
|
3卷引用:广东省部分学校2024届高三下学期5月份大联考化学试题
6 . W、X、Y、Z是原子序数依次增大的主族元素,在前三周期均有分布,基态X原子有四种不同空间运动状态的电子;Y为地壳中含量最多的元素,其简单离子与Z的简单离子具有相同电子数;工业上常通过电解Z的氧化物制取其单质,下列说法不正确的是
A.元素电负性: |
B.简单氢化物的沸点: |
| C.W2Y2和XY2都是极性分子 |
| D.Z同周期且第一电离能小于Z的元素有1种 |
您最近一年使用:0次
7 . 催化剂(XYZ6ME5)的组成元素均为主族元素且在每个短周期均有分布,X的基态原子p轨道电子总数比s轨道电子总数多1个;仅Y、M、E处于同一周期,原子序数依次增大且相邻;E在地壳中含量最多。下列说法不正确的是
| A.第一电离能:M>E>X | B.简单氢化物的稳定性:E>M |
| C.氧化物的熔点:X>Y>Z | D.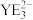 和 和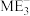 的空间结构相同 的空间结构相同 |
您最近一年使用:0次
2024-04-12更新
|
405次组卷
|
2卷引用:广东省茂名市2024届高三下学期第二次综合测试化学试卷
8 . Q、R、X、Y是原子序数依次增大的同周期不同主族的非金属元素,Q的基态原子p轨道电子数是s轨道电子数的一半,同周期元素基态原子中R的未成对电子数最多。下列说法不正确的是
A.简单氢化物的沸点: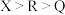 | B.元素电负性: |
C.第一电离能: | D.简单离子半径: |
您最近一年使用:0次
2024-03-26更新
|
425次组卷
|
3卷引用:广东省梅州市2023-2024学年高三下学期总复习质检试题(一模)化学试卷
名校
解题方法
9 . 氨氧化法是工业制硝酸的重要途径,其中氨氧化过程如下图所示。下列说法错误的是
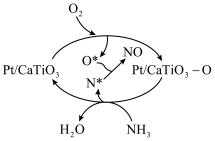
A.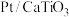 能降低 能降低 氧化的活化能 氧化的活化能 |
B.该过程的总反应式为: |
| C.第一电离能:O>N>H |
| D.可用氨还原法处理硝酸工业的尾气 |
您最近一年使用:0次
2024-03-22更新
|
605次组卷
|
3卷引用:广东省佛山市2024届高三教学质量检测(一)化学试题
名校
10 . 某种离子液体的结构如图所示,其中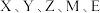 为原子序数依次增大的短周期元素,基态
为原子序数依次增大的短周期元素,基态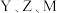 原子的未成对电子数之比为
原子的未成对电子数之比为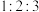 ,基态E原子p能级电子数比
,基态E原子p能级电子数比 能级电子数多1。下列说法不正确的是
能级电子数多1。下列说法不正确的是
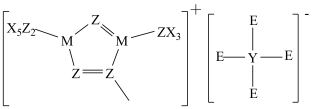
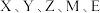 为原子序数依次增大的短周期元素,基态
为原子序数依次增大的短周期元素,基态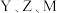 原子的未成对电子数之比为
原子的未成对电子数之比为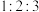 ,基态E原子p能级电子数比
,基态E原子p能级电子数比 能级电子数多1。下列说法不正确的是
能级电子数多1。下列说法不正确的是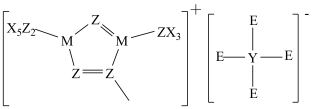
A.原子半径: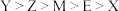 | B.第一电离能: |
C.简单氢化物沸点: | D.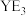 和 和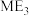 的空间结构均为平面三角形 的空间结构均为平面三角形 |
您最近一年使用:0次



