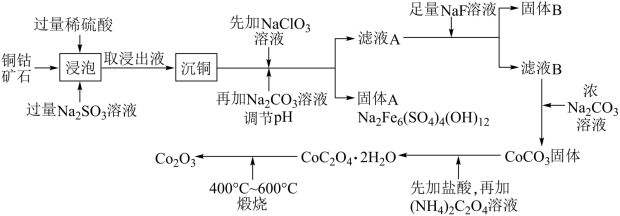
1 . 三氧化二钴主要用作颜料、釉料及磁性材料,利用铜钴矿石制备 的工艺流程如图所示:
的工艺流程如图所示:
已知:铜钴矿石主要含有 ,其中还含有一定量的
,其中还含有一定量的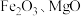 和
和 等。请回答下列问题:
等。请回答下列问题:
(1) 元素的价层电子排布式是
元素的价层电子排布式是___________ ,铁、钴均为第四周期第Ⅷ族元素, 和
和 的第三电离能
的第三电离能
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2)“浸泡”过程中,加入 溶液的主要作用是
溶液的主要作用是___________ 。
(3)向“沉铜”后的滤液中加入 溶液,写出滤液中的金属离子与
溶液,写出滤液中的金属离子与 反应的离子方程式:
反应的离子方程式:___________ 。
(4)过滤出的 固体经洗涤后,证明固体已洗净的操作是
固体经洗涤后,证明固体已洗净的操作是___________ 。
(5) 在空气中高温煅烧得到
在空气中高温煅烧得到 的化学方程式是
的化学方程式是___________ 。
(6)一定温度下,向滤液 中加入足量的
中加入足量的 溶液可将
溶液可将 沉淀而除去,若所得滤液
沉淀而除去,若所得滤液 中
中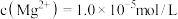 ,则滤液
,则滤液 中
中 为
为___________ [已知该温度下 ,
, ]。
]。
 的工艺流程如图所示:
的工艺流程如图所示:
已知:铜钴矿石主要含有
 ,其中还含有一定量的
,其中还含有一定量的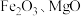 和
和 等。请回答下列问题:
等。请回答下列问题:(1)
 元素的价层电子排布式是
元素的价层电子排布式是 和
和 的第三电离能
的第三电离能
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)“浸泡”过程中,加入
 溶液的主要作用是
溶液的主要作用是(3)向“沉铜”后的滤液中加入
 溶液,写出滤液中的金属离子与
溶液,写出滤液中的金属离子与 反应的离子方程式:
反应的离子方程式:(4)过滤出的
 固体经洗涤后,证明固体已洗净的操作是
固体经洗涤后,证明固体已洗净的操作是(5)
 在空气中高温煅烧得到
在空气中高温煅烧得到 的化学方程式是
的化学方程式是(6)一定温度下,向滤液
 中加入足量的
中加入足量的 溶液可将
溶液可将 沉淀而除去,若所得滤液
沉淀而除去,若所得滤液 中
中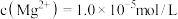 ,则滤液
,则滤液 中
中 为
为 ,
, ]。
]。
您最近一年使用:0次
2 . 如图是部分元素的第一电离能随原子序数变化的曲线(其中12~17号元素的有关数据缺失)。

(1)请写出 区铜原子基态电子排布式
区铜原子基态电子排布式_______
(2)同主族元素的第一电离能的变化规律是_______
(3)图中第一电离能最小的元素在周期表中的位置是_______
(4)根据对角线规则,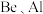 的最高价氧化物对应水化物的性质相似,它们都具有
的最高价氧化物对应水化物的性质相似,它们都具有_______ 性,能证明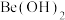 该性质的实验结论是
该性质的实验结论是_______
(5) 元素中,某元素M电离能如表所示:
元素中,某元素M电离能如表所示:
①由此判断该元素是_______ (填元素符号);
②分析图中同周期元素第一电离能的变化规律,推断: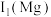
_______  。
。

(1)请写出
 区铜原子基态电子排布式
区铜原子基态电子排布式(2)同主族元素的第一电离能的变化规律是
(3)图中第一电离能最小的元素在周期表中的位置是
(4)根据对角线规则,
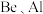 的最高价氧化物对应水化物的性质相似,它们都具有
的最高价氧化物对应水化物的性质相似,它们都具有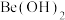 该性质的实验结论是
该性质的实验结论是(5)
 元素中,某元素M电离能如表所示:
元素中,某元素M电离能如表所示: | 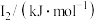 | 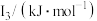 | 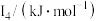 | 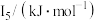 |
| 578 | 1817 | 2745 | 11575 | 14830 |
②分析图中同周期元素第一电离能的变化规律,推断:
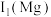
 。
。
您最近一年使用:0次
名校
解题方法
3 . 前四周期元素A、B、C、D、E、F原子序数依次增大,其相关性质如表所示:
请根据以上情况,回答下列问题:
(1)B元素在周期表中的位置_________ 。
(2)E元素元素基态原子核外有_________ 种空间运动状态不同的电子,其价电子轨道排布式为_________ 。
(3)F元素基态原子的价电子排布式_________ 。高温条件下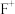 比
比 稳定的原因
稳定的原因_________ (涉及物质写元素符号)。
(4)写出一个化学方程式证明元素B和D的非金属性强弱_________ 。(涉及物质写元素符号)
(5)A、B、C、D四种元素第一电离能由大到小的顺序为_________ (用元素符号表示)。
| A |  能级电子半充满 能级电子半充满 |
| B | 与A同周期,且原子核外有2个未成对电子 |
| C | 基态原子核外有6个原子轨道排有电子,且只有1个未成对电子 |
| D | 其基态原子价电子排布式为 |
| E | 前四周期元素中,E元素基态原子未成对电子数最多 |
| F | 基态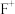 各能级电子全充满 各能级电子全充满 |
(1)B元素在周期表中的位置
(2)E元素元素基态原子核外有
(3)F元素基态原子的价电子排布式
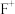 比
比 稳定的原因
稳定的原因(4)写出一个化学方程式证明元素B和D的非金属性强弱
(5)A、B、C、D四种元素第一电离能由大到小的顺序为
您最近一年使用:0次
名校
解题方法
4 . 氢能被视为21世纪最具发展潜力的清洁能源,开发高效储氢材料是氢能利用的重要研究方向。
(1)H3BNH3是一种潜在的储氢材料,其中N原子的价电子轨道表达式为____ 。
(2)制备H3BNH3的化学原料为(HB=NH)3,为六元环状物质,与其互为等电子体的有机物分子式为__ ,CH4、H2O、CO2的键角由大到小的顺序为____ ,B、C、N、O的第一电离能由大到小的顺序为_ 。
(3)C16S8是新型环烯类储氢材料,研究证明其分子呈平面结构(如图所示)。

①C16S8分子中C原子和S原子的杂化轨道类型分别为____ 。
②测得C16S8中碳硫键的键长介于C─S和C=S之间,其原因可能是______ 。
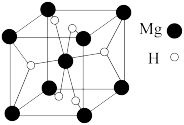
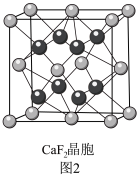
(4)某种铜银合金晶体具有储氢功能,它是面心立方最密堆积结构,Cu原子位于面心,Ag原子位于顶点,H原子可进入由Cu原子和Ag原子构成的四面体空隙中。若将Cu、Ag原子等同看待,该晶体储氢后的晶胞结构与CaF2(如图)相似,该晶体储氢后的化学式为_____ 。

(5)MgH2是金属氢化物储氢材料,其晶胞如图所示,该晶体的密度为 ρ g/cm3,则该晶胞的体积为_____ 。(用含ρ、NA的代数式表示即可)
(1)H3BNH3是一种潜在的储氢材料,其中N原子的价电子轨道表达式为
(2)制备H3BNH3的化学原料为(HB=NH)3,为六元环状物质,与其互为等电子体的有机物分子式为
(3)C16S8是新型环烯类储氢材料,研究证明其分子呈平面结构(如图所示)。

①C16S8分子中C原子和S原子的杂化轨道类型分别为
②测得C16S8中碳硫键的键长介于C─S和C=S之间,其原因可能是
(4)某种铜银合金晶体具有储氢功能,它是面心立方最密堆积结构,Cu原子位于面心,Ag原子位于顶点,H原子可进入由Cu原子和Ag原子构成的四面体空隙中。若将Cu、Ag原子等同看待,该晶体储氢后的晶胞结构与CaF2(如图)相似,该晶体储氢后的化学式为

(5)MgH2是金属氢化物储氢材料,其晶胞如图所示,该晶体的密度为 ρ g/cm3,则该晶胞的体积为

您最近一年使用:0次
2020-09-01更新
|
273次组卷
|
5卷引用:湖南省湘乡市第一中学2022届高三下学期第三次仿真考化学试题
5 . 超导现象一直吸引着广大科学家的关注。某超导材料的晶体结构属于四方晶系,其晶胞如图所示。下列说法错误的是
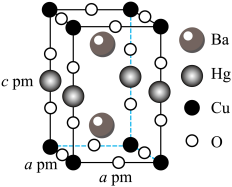
A.第一电离能: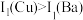 | B.与 等距且最近的 等距且最近的 有12个 有12个 |
C.该超导材料的化学式为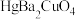 | D.该晶体的密度为 |
您最近一年使用:0次
昨日更新
|
136次组卷
|
2卷引用:2024届湖南省益阳市安化县第二中学高三下学期三模化学试题
解题方法
6 . 通过给电子主体Y和吸电子客体Z作用,可制备一种延迟荧光材料的通用超分子主客体共晶,制备路线如下。下列说法错误的是

| A.X与足量H2反应后,所得产物中含有4个手性碳原子 |
| B.Z中所含元素的第一电离能:F>N>C>H |
| C.Y与Z通过分子间相互作用和尺寸匹配形成超分子 |
| D.该超分子材料发射荧光的原理与原子核外电子跃迁释放能量有关 |
您最近一年使用:0次
名校
解题方法
7 . 卤族元素组成的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识它们。
(1)如图1为碘晶体的晶胞结构。下列有关说法正确的是___________ 填序号
填序号 。
。
(2)如图2为晶体的晶胞结构。其中黑色球表示___________ ,晶体中与F-最近且等距离的Ca2+数目为___________ 。 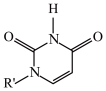 或Cu(I)(I表示化合价为+1)时,分别形成如下图所示A和B:
或Cu(I)(I表示化合价为+1)时,分别形成如下图所示A和B:___________ (填“σ”或“π”)键的特性。
②微粒间的相互作用包括化学键和分子间相互作用,比较A和B中微粒间相互作用力的差异:___________ 。
(4)含氟牙膏预防龋齿的原理是生成更难溶的氟磷灰石[Ca5(PO4)3F],S、P、O、F四种元素第一电离能从小到大的顺序是___________ ,其中PO 的空间构型为
的空间构型为___________ 。
(1)如图1为碘晶体的晶胞结构。下列有关说法正确的是___________
 填序号
填序号 。
。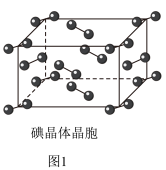
| A.平均每个晶胞中有4个碘分子 |
| B.平均每个晶胞中有4个碘原子 |
| C.碘晶体为无限延伸的空间结构,是共价晶体 |
| D.碘晶体中存在的相互作用有非极性键和范德华力 |
(2)如图2为晶体的晶胞结构。其中黑色球表示
 或Cu(I)(I表示化合价为+1)时,分别形成如下图所示A和B:
或Cu(I)(I表示化合价为+1)时,分别形成如下图所示A和B: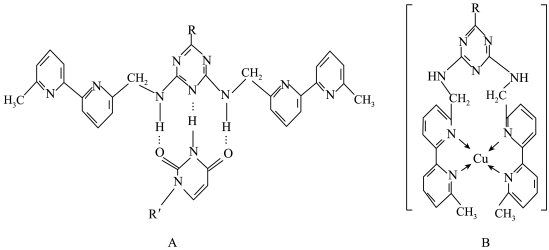
②微粒间的相互作用包括化学键和分子间相互作用,比较A和B中微粒间相互作用力的差异:
(4)含氟牙膏预防龋齿的原理是生成更难溶的氟磷灰石[Ca5(PO4)3F],S、P、O、F四种元素第一电离能从小到大的顺序是
 的空间构型为
的空间构型为
您最近一年使用:0次
名校
解题方法
8 . 2022年5月15日,“天问一号”探测器成功着陆于火星。据了解火星上存在大量的含氮化合物,一种含氮鸟嘌呤和吡啶(下图右)的结构如图。已知吡啶为平面结构;分子中的大π键可以用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。下列说法不正确的是
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。下列说法不正确的是
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。下列说法不正确的是
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。下列说法不正确的是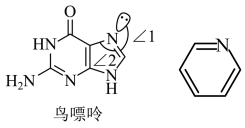
A.鸟嘌呤中元素的第一电离能: |
B.鸟嘌呤中C原子杂化方式都为 |
| C.鸟嘌呤中轨道之间的夹角∠1大于∠2 |
D.该吡啶中的大π键可表示为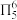 |
您最近一年使用:0次
名校
9 . 氨基酸是构成人体必备蛋白质的基础,某氨基酸的结构简式如图所示。下列有关说法错误的是


A.该分子中碳原子的杂化类型有sp、 和 和 |
B.该分子的分子式为 |
C.键的极性大小: |
D.第一电离能: |
您最近一年使用:0次
名校
解题方法
10 . 某储氢材料前驱体结构如下图,M、W、X、Y、Z五种元素原子序数依次增大,基态Z原子的电子填充了3个能级,其中有2个未成对电子。下列说法错误的是
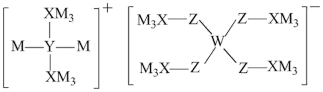
A.简单氢化物沸点高低: | B.Y和W位于同一主族 |
C.第一电离能大小: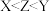 | D.阴、阳离子中均有配位键 |
您最近一年使用:0次
2024-01-09更新
|
1025次组卷
|
9卷引用:湖南省株洲市2024届高三上学期教学质量统一检测化学试题
湖南省株洲市2024届高三上学期教学质量统一检测化学试题湖南省株洲市2023-2024学年高三上学期教学质量统一检测化学试卷(已下线)化学(九省联考考后提升卷,吉林、黑龙江卷)-2024年1月“九省联考”真题完全解读与考后提升(已下线)热点12 元素推断与元素周期律河北省石家庄市第二中学2023-2024学年高三上学期期末考试化学试题北京市第二中学2023-2024学年高三下学期开学考试化学试卷(已下线)专题04 物质结构与性质 元素推断-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)2024届吉林省通化市梅河口市第五中学高三下学期一模化学试题2024届宁夏回族自治区银川一中高三下学期第二次模拟考试理科综合试卷-高中化学



