1 . 三氧化二钴主要用作颜料、釉料及磁性材料,利用铜钴矿石制备 的工艺流程如图所示:
的工艺流程如图所示:
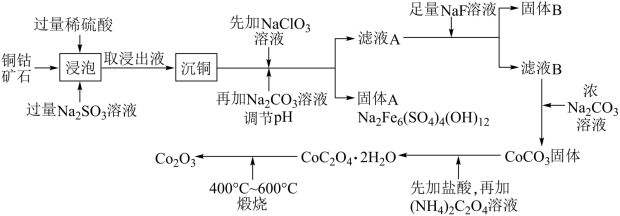
已知:铜钴矿石主要含有 ,其中还含有一定量的
,其中还含有一定量的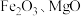 和
和 等。请回答下列问题:
等。请回答下列问题:
(1) 元素的价层电子排布式是
元素的价层电子排布式是___________ ,铁、钴均为第四周期第Ⅷ族元素, 和
和 的第三电离能
的第三电离能
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2)“浸泡”过程中,加入 溶液的主要作用是
溶液的主要作用是___________ 。
(3)向“沉铜”后的滤液中加入 溶液,写出滤液中的金属离子与
溶液,写出滤液中的金属离子与 反应的离子方程式:
反应的离子方程式:___________ 。
(4)过滤出的 固体经洗涤后,证明固体已洗净的操作是
固体经洗涤后,证明固体已洗净的操作是___________ 。
(5) 在空气中高温煅烧得到
在空气中高温煅烧得到 的化学方程式是
的化学方程式是___________ 。
(6)一定温度下,向滤液 中加入足量的
中加入足量的 溶液可将
溶液可将 沉淀而除去,若所得滤液
沉淀而除去,若所得滤液 中
中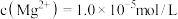 ,则滤液
,则滤液 中
中 为
为___________ [已知该温度下 ,
, ]。
]。
 的工艺流程如图所示:
的工艺流程如图所示:
已知:铜钴矿石主要含有
 ,其中还含有一定量的
,其中还含有一定量的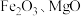 和
和 等。请回答下列问题:
等。请回答下列问题:(1)
 元素的价层电子排布式是
元素的价层电子排布式是 和
和 的第三电离能
的第三电离能
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)“浸泡”过程中,加入
 溶液的主要作用是
溶液的主要作用是(3)向“沉铜”后的滤液中加入
 溶液,写出滤液中的金属离子与
溶液,写出滤液中的金属离子与 反应的离子方程式:
反应的离子方程式:(4)过滤出的
 固体经洗涤后,证明固体已洗净的操作是
固体经洗涤后,证明固体已洗净的操作是(5)
 在空气中高温煅烧得到
在空气中高温煅烧得到 的化学方程式是
的化学方程式是(6)一定温度下,向滤液
 中加入足量的
中加入足量的 溶液可将
溶液可将 沉淀而除去,若所得滤液
沉淀而除去,若所得滤液 中
中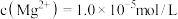 ,则滤液
,则滤液 中
中 为
为 ,
, ]。
]。
您最近一年使用:0次
2 . 如图是部分元素的第一电离能随原子序数变化的曲线(其中12~17号元素的有关数据缺失)。

(1)请写出 区铜原子基态电子排布式
区铜原子基态电子排布式_______
(2)同主族元素的第一电离能的变化规律是_______
(3)图中第一电离能最小的元素在周期表中的位置是_______
(4)根据对角线规则,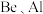 的最高价氧化物对应水化物的性质相似,它们都具有
的最高价氧化物对应水化物的性质相似,它们都具有_______ 性,能证明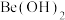 该性质的实验结论是
该性质的实验结论是_______
(5) 元素中,某元素M电离能如表所示:
元素中,某元素M电离能如表所示:
①由此判断该元素是_______ (填元素符号);
②分析图中同周期元素第一电离能的变化规律,推断: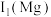
_______  。
。

(1)请写出
 区铜原子基态电子排布式
区铜原子基态电子排布式(2)同主族元素的第一电离能的变化规律是
(3)图中第一电离能最小的元素在周期表中的位置是
(4)根据对角线规则,
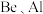 的最高价氧化物对应水化物的性质相似,它们都具有
的最高价氧化物对应水化物的性质相似,它们都具有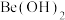 该性质的实验结论是
该性质的实验结论是(5)
 元素中,某元素M电离能如表所示:
元素中,某元素M电离能如表所示: | 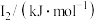 | 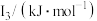 | 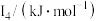 | 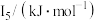 |
| 578 | 1817 | 2745 | 11575 | 14830 |
②分析图中同周期元素第一电离能的变化规律,推断:
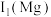
 。
。
您最近一年使用:0次
名校
解题方法
3 . 前四周期元素A、B、C、D、E、F原子序数依次增大,其相关性质如表所示:
请根据以上情况,回答下列问题:
(1)B元素在周期表中的位置_________ 。
(2)E元素元素基态原子核外有_________ 种空间运动状态不同的电子,其价电子轨道排布式为_________ 。
(3)F元素基态原子的价电子排布式_________ 。高温条件下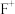 比
比 稳定的原因
稳定的原因_________ (涉及物质写元素符号)。
(4)写出一个化学方程式证明元素B和D的非金属性强弱_________ 。(涉及物质写元素符号)
(5)A、B、C、D四种元素第一电离能由大到小的顺序为_________ (用元素符号表示)。
| A |  能级电子半充满 能级电子半充满 |
| B | 与A同周期,且原子核外有2个未成对电子 |
| C | 基态原子核外有6个原子轨道排有电子,且只有1个未成对电子 |
| D | 其基态原子价电子排布式为 |
| E | 前四周期元素中,E元素基态原子未成对电子数最多 |
| F | 基态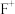 各能级电子全充满 各能级电子全充满 |
(1)B元素在周期表中的位置
(2)E元素元素基态原子核外有
(3)F元素基态原子的价电子排布式
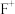 比
比 稳定的原因
稳定的原因(4)写出一个化学方程式证明元素B和D的非金属性强弱
(5)A、B、C、D四种元素第一电离能由大到小的顺序为
您最近一年使用:0次
名校
解题方法
4 . 氢能被视为21世纪最具发展潜力的清洁能源,开发高效储氢材料是氢能利用的重要研究方向。
(1)H3BNH3是一种潜在的储氢材料,其中N原子的价电子轨道表达式为____ 。
(2)制备H3BNH3的化学原料为(HB=NH)3,为六元环状物质,与其互为等电子体的有机物分子式为__ ,CH4、H2O、CO2的键角由大到小的顺序为____ ,B、C、N、O的第一电离能由大到小的顺序为_ 。
(3)C16S8是新型环烯类储氢材料,研究证明其分子呈平面结构(如图所示)。

①C16S8分子中C原子和S原子的杂化轨道类型分别为____ 。
②测得C16S8中碳硫键的键长介于C─S和C=S之间,其原因可能是______ 。
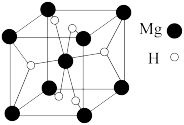
(4)某种铜银合金晶体具有储氢功能,它是面心立方最密堆积结构,Cu原子位于面心,Ag原子位于顶点,H原子可进入由Cu原子和Ag原子构成的四面体空隙中。若将Cu、Ag原子等同看待,该晶体储氢后的晶胞结构与CaF2(如图)相似,该晶体储氢后的化学式为_____ 。

(5)MgH2是金属氢化物储氢材料,其晶胞如图所示,该晶体的密度为 ρ g/cm3,则该晶胞的体积为_____ 。(用含ρ、NA的代数式表示即可)
(1)H3BNH3是一种潜在的储氢材料,其中N原子的价电子轨道表达式为
(2)制备H3BNH3的化学原料为(HB=NH)3,为六元环状物质,与其互为等电子体的有机物分子式为
(3)C16S8是新型环烯类储氢材料,研究证明其分子呈平面结构(如图所示)。

①C16S8分子中C原子和S原子的杂化轨道类型分别为
②测得C16S8中碳硫键的键长介于C─S和C=S之间,其原因可能是
(4)某种铜银合金晶体具有储氢功能,它是面心立方最密堆积结构,Cu原子位于面心,Ag原子位于顶点,H原子可进入由Cu原子和Ag原子构成的四面体空隙中。若将Cu、Ag原子等同看待,该晶体储氢后的晶胞结构与CaF2(如图)相似,该晶体储氢后的化学式为

(5)MgH2是金属氢化物储氢材料,其晶胞如图所示,该晶体的密度为 ρ g/cm3,则该晶胞的体积为

您最近一年使用:0次
2020-09-01更新
|
275次组卷
|
5卷引用:湖南省湘乡市第一中学2022届高三下学期第三次仿真考化学试题
5 . 根据下列五种元素的电离能数据(单位: ),判断下列说法不正确的是
),判断下列说法不正确的是
 ),判断下列说法不正确的是
),判断下列说法不正确的是| 元素代号 |  |  |  |  |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
| A.Q元素可能是0族元素 |
| B.R和S均可能与U在同一主族 |
| C.U元素可能在元素周期表的s区 |
D.原子的外围电子排布式为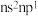 的可能是T元素 的可能是T元素 |
您最近一年使用:0次
2024-03-03更新
|
146次组卷
|
4卷引用:湖南省娄底市涟源市行知高级中学2023-2024学年高二上学期1月期末化学试题
湖南省娄底市涟源市行知高级中学2023-2024学年高二上学期1月期末化学试题江苏无锡市第三高级中学2023-2024学年高二上学期期中考试化学试卷(已下线)1.2.2 元素周期律课堂例题(已下线)猜想01 原子结构与性质 【考题猜想】(8大题型)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)
6 . 化合物 可作肥料,其中X、Y、Z、M、N为原子序数依次增大的短周期元素,且在每个短周期均有分布,仅有Y和N同族。Y的基态原子价层p轨道半充满,M的基态原子价层电子排布式为
可作肥料,其中X、Y、Z、M、N为原子序数依次增大的短周期元素,且在每个短周期均有分布,仅有Y和N同族。Y的基态原子价层p轨道半充满,M的基态原子价层电子排布式为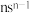 ,Z在地壳中含量最多。下列说法不正确的是
,Z在地壳中含量最多。下列说法不正确的是
 可作肥料,其中X、Y、Z、M、N为原子序数依次增大的短周期元素,且在每个短周期均有分布,仅有Y和N同族。Y的基态原子价层p轨道半充满,M的基态原子价层电子排布式为
可作肥料,其中X、Y、Z、M、N为原子序数依次增大的短周期元素,且在每个短周期均有分布,仅有Y和N同族。Y的基态原子价层p轨道半充满,M的基态原子价层电子排布式为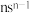 ,Z在地壳中含量最多。下列说法不正确的是
,Z在地壳中含量最多。下列说法不正确的是| A.元素电负性:Z>Y>X | B.最简单氢化物沸点:Z>Y>N |
| C.第一电离能:Y>Z>M | D. 和 和 的空间结构均为三角锥形 的空间结构均为三角锥形 |
您最近一年使用:0次
2024-02-14更新
|
687次组卷
|
3卷引用:2024届湖南省岳阳市高三教学质量监测考试一模化学试题
2024届湖南省岳阳市高三教学质量监测考试一模化学试题(已下线)专题04 物质结构与性质 元素推断-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)2024届江西省上饶市高三下学期第二次高考模拟考试化学试卷
名校
解题方法
7 . X、Y、Z、W四种元素,原子序数依次增大。Y与X、Z均相邻,元素Y的原子最外层电子数是其内层电子数的3倍,元素Z基态原子的3p轨道上有4个电子。元素W基态原子的内层轨道全部排满电子,且最外层电子数为1。下列说法不正确 的是
A.第一电离能: |
B.电负性: |
| C.元素Y和Z能形成含有极性键的非极性分子 |
| D.元素Z和W的单质加热反应后产物的化学式为WZ |
您最近一年使用:0次
2023-10-03更新
|
178次组卷
|
4卷引用:湖南省长沙麓山国际实验学校2023-2024学年高二下学期第一次学情检测化学试卷
湖南省长沙麓山国际实验学校2023-2024学年高二下学期第一次学情检测化学试卷 浙江省嘉兴市2023-2024学年高三上学期 9月基础测试化学试题(已下线)专题04 物质结构与性质(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)广东省汕尾市陆河县河田中学2023-2024学年高二下学期4月期中考试化学试题
8 . 某种镁盐具有良好的电化学性能,其阴离子结构如下图所示:

W、X、Y、Z、Q是核电荷数依次增大的短周期元素,W、Y原子序数之和等于Z,Y原子价电子数是Q原子价电子数的2倍。下列说法错误的是

W、X、Y、Z、Q是核电荷数依次增大的短周期元素,W、Y原子序数之和等于Z,Y原子价电子数是Q原子价电子数的2倍。下列说法错误的是
| A.W与X的化合物不一定为极性分子 |
| B.第一电离能Z>X>Y |
| C.Q的氧化物是两性氧化物 |
| D.该阴离子中含有配位键 |
您最近一年使用:0次
解题方法
9 . 前四周期主族元素X、Y、Z、W、Q的原子序数依次增大,X是空气中含量最多的元素,Y元素的原子的最外层电子数与其K层的电子数相等,Z的周期序数与族序数相等,基态W原子的3p原子轨道上有5个电子,Q与W处于同主族。下列说法错误的是
| A.X的第一电离能比同周期相邻元素的大 | B.原子半径大小顺序是Q>W>Z>Y |
| C.Q元素位于周期表中的p区 | D.基态Z原子有13种不同运动状态的电子 |
您最近一年使用:0次
10 . 晶体结构的缺陷美与对称美同样受关注。某种超导材料的晶胞结构如图所示,其中O原子有缺陷。晶胞参数分别如图, ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。下列说法错误的是
。下列说法错误的是
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。下列说法错误的是
。下列说法错误的是
A.该晶体的最简化学式为 |
B.晶体中与 最近且距离相等的 最近且距离相等的 有6个 有6个 |
C.晶体的密度为 |
D.第一电离能: |
您最近一年使用:0次
2024-01-30更新
|
551次组卷
|
6卷引用:湖南省常德市第一中学2023-2024学年高三上学期第六次月考化学试题



