解题方法
1 . 科学家发现对一种亲水有机盐LiTFSI进行掺杂和改进,能显著提高锂离子电池传输电荷的能力。LiTFSI的结构如图所示,其中A、B、C、D为同一短周期元素,E与C同主族,E的原子序数是B、D的原子序数之和。下列说法正确的是
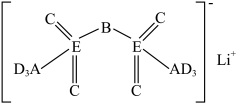
A.元素B的杂化方式为 | B.元素的第一电离能:D>C>B>A |
| C.含有元素E的钠盐水溶液不可能呈酸性 | D.简单氢化物的沸点:E>C |
您最近半年使用:0次
2 . 按要求回答问题。
(1)1 mol HCHO分子中含有σ键的数目为___________ NA。
(2)CS2分子中,共价键的类型有___________ 。
(3)下列物质中:
①MgCl2;②Na2O2; ③CS2 ;④NaOH;⑤H2。
只存在极性键的是___________ (填序号,下同),只存在非极性键的是___________ ,只存在离子键的是___________ ,既存在离子键又存在极性共价键的是___________ ,既存在离子键又存在非极性共价键的是___________ 。
(4)第一电离能比较Mg___________ Al,解释原因___________ 。
(1)1 mol HCHO分子中含有σ键的数目为
(2)CS2分子中,共价键的类型有
(3)下列物质中:
①MgCl2;②Na2O2; ③CS2 ;④NaOH;⑤H2。
只存在极性键的是
(4)第一电离能比较Mg
您最近半年使用:0次
名校
解题方法
3 . 某种离子液体的阴离子结构如图,Q、W、X、Y、Z五种短周期元素的原子半径依次增大,基态Q原子的电子填充3个能级,有4对成对电子,Z与其他元素不在同一周期,下列说法正确的是
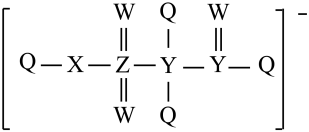
| A.最高价氧化物对应水化物的酸性:Q>X |
| B.Q、W、X的第一电离能依次减小 |
| C.氢化物的沸点:W>Y |
| D.X、Y、Z均至少有两种氧化物 |
您最近半年使用:0次
7日内更新
|
131次组卷
|
2卷引用:湖南省衡阳市衡阳县第一中学2023-2024学年高二下学期4月期中考试化学试题
名校
解题方法
4 . 卤族元素组成的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识它们。
(1)如图1为碘晶体的晶胞结构。下列有关说法正确的是___________ 填序号
填序号 。
。
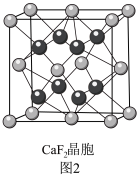
(2)如图2为晶体的晶胞结构。其中黑色球表示___________ ,晶体中与F-最近且等距离的Ca2+数目为___________ 。 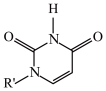 或Cu(I)(I表示化合价为+1)时,分别形成如下图所示A和B:
或Cu(I)(I表示化合价为+1)时,分别形成如下图所示A和B:___________ (填“σ”或“π”)键的特性。
②微粒间的相互作用包括化学键和分子间相互作用,比较A和B中微粒间相互作用力的差异:___________ 。
(4)含氟牙膏预防龋齿的原理是生成更难溶的氟磷灰石[Ca5(PO4)3F],S、P、O、F四种元素第一电离能从小到大的顺序是___________ ,其中PO 的空间构型为
的空间构型为___________ 。
(1)如图1为碘晶体的晶胞结构。下列有关说法正确的是___________
 填序号
填序号 。
。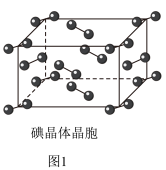
| A.平均每个晶胞中有4个碘分子 |
| B.平均每个晶胞中有4个碘原子 |
| C.碘晶体为无限延伸的空间结构,是共价晶体 |
| D.碘晶体中存在的相互作用有非极性键和范德华力 |
(2)如图2为晶体的晶胞结构。其中黑色球表示
 或Cu(I)(I表示化合价为+1)时,分别形成如下图所示A和B:
或Cu(I)(I表示化合价为+1)时,分别形成如下图所示A和B: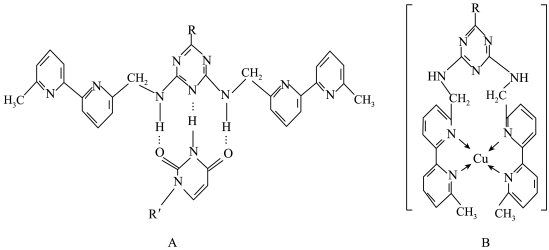
②微粒间的相互作用包括化学键和分子间相互作用,比较A和B中微粒间相互作用力的差异:
(4)含氟牙膏预防龋齿的原理是生成更难溶的氟磷灰石[Ca5(PO4)3F],S、P、O、F四种元素第一电离能从小到大的顺序是
 的空间构型为
的空间构型为
您最近半年使用:0次
5 . 前四周期元素X、Y、Z、W的原子数依次增大,X原子中有6个运动状态不同的电子,Y是地壳中含量最多的元素,基态Z原子K、L层上的电子总数是3p原子轨道上电子数的两倍,基态W原子中有6个未成对电子。下列说法错误的是
| A.同周期中,元素Z的第一电离能最大 |
| B.电负性:Y>Z;原子半径:Z>X>Y |
C.在一定条件下,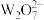 和 和 可以相互转化 可以相互转化 |
| D.Y与Z形成的一种化合物可用于自来水消毒 |
您最近半年使用:0次
解题方法
6 . YX4Z(WR4)2常用于抗酸、治疗慢性胃炎。它所含的五种元素均为短周期元素,基态R原子的价层电子排布式为nsnnp2n,R和W位于同主族,Y的最高价氧化物对应的水化物和其最简单氢化物能反应生成离子化合物,Z的周期序数和主族序数相等。下列叙述错误的是
| A.沸点:X2R<X2W |
| B.第一电离能:X<R<Y |
| C.Z元素的最高价氧化物为两性氧化物 |
| D.W元素最高价氧化物的水化物的浓溶液在常温下可以使铁钝化 |
您最近半年使用:0次
7 . 元素及其化合物因其结构的差异导致性质各异。请回答:
(1)某激发态磷原子的电子排布式为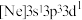 ,该磷原子中有
,该磷原子中有_______ 种空间运动状态不同的电子。
(2)NCl3的空间结构为_______ ,和BCl3相比二者中沸点更高的物质是______ ,原因是_______ 。第一电离能介于B、N之间的第二周期元素有_______ 种。
(3)N、P位于同一主族,但 间的夹角比
间的夹角比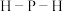 间的大,其主要原因是
间的大,其主要原因是_______ 。
(4)FeS2晶体的晶胞形状为立方体,边长为anm,结构如图。_______ 个。
②FeS2的摩尔质量为120g∙mol-1,阿伏加德罗常数为NA。该晶体的密度为_______ g∙cm-3。
(1)某激发态磷原子的电子排布式为
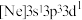 ,该磷原子中有
,该磷原子中有(2)NCl3的空间结构为
(3)N、P位于同一主族,但
 间的夹角比
间的夹角比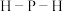 间的大,其主要原因是
间的大,其主要原因是(4)FeS2晶体的晶胞形状为立方体,边长为anm,结构如图。
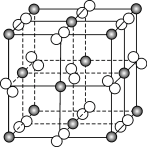
②FeS2的摩尔质量为120g∙mol-1,阿伏加德罗常数为NA。该晶体的密度为
您最近半年使用:0次
名校
8 . 短周期主族元素 、
、 、
、 、
、 原子序数依次增大,四种元素组成的一种食品添加剂结构如图所示。
原子序数依次增大,四种元素组成的一种食品添加剂结构如图所示。 的原子半径在短周期中最大,
的原子半径在短周期中最大, 基态原子的
基态原子的 能级电子总数是
能级电子总数是 能级电子总数的
能级电子总数的 。下列说法不正确的是
。下列说法不正确的是
 、
、 、
、 、
、 原子序数依次增大,四种元素组成的一种食品添加剂结构如图所示。
原子序数依次增大,四种元素组成的一种食品添加剂结构如图所示。 的原子半径在短周期中最大,
的原子半径在短周期中最大, 基态原子的
基态原子的 能级电子总数是
能级电子总数是 能级电子总数的
能级电子总数的 。下列说法不正确的是
。下列说法不正确的是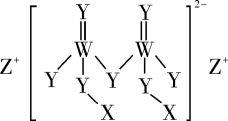
A. 、 、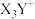 两种粒子的VSEPR模型相同 两种粒子的VSEPR模型相同 |
B.简单离子半径: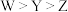 |
C.第一电离能: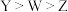 |
D.该化合物中 的杂化轨道类型为 的杂化轨道类型为 |
您最近半年使用:0次
名校
9 . 某离子与其检验试剂GBHA的反应如下图所示,其中M、W、X、Y、Z为电负性依次增大的分属不同三个周期的前20号元素,下列说法正确的是
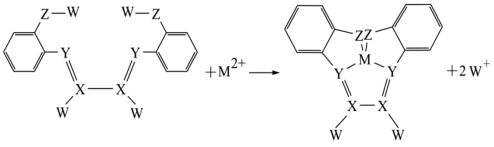
| A.键角:XZ2<YW3 |
| B.氢化物的沸点:X<Z |
| C.可通过电解熔融MCl2 获得 M的单质 |
| D.同周期第一电离能介于X和Z之间的元素有1种 |
您最近半年使用:0次
2024-04-13更新
|
462次组卷
|
2卷引用:湖南省永州市第一中学2023-2024学年高二下学期3月月考化学试题
名校
10 . X、Y、Z、W、Q五种短周期主族元素在元素周期表中的相对位置如下表所示。已知:①Y元素的最高价氧化物对应水化物与其简单气态氢化物通过化合反应生成一种盐;②通常情况下,W与Q形成的化合物甲为白色晶体,常作调味品。下列判断错误的是
| …… | X | Y | Z | ||
| W | …… | Q |
| A.第一电离能:Y<Z |
| B.电负性:X<Q |
| C.Y形成的双原子分子中σ键与π键的个数之比为1∶2 |
| D.甲的一个晶胞中含4个阳离子 |
您最近半年使用:0次



