9-10高二下·江苏泰州·期末
名校
解题方法
1 . 对Na、Mg、Al的有关性质的叙述正确的是:
| A.碱性:NaOH< Mg(OH)2< Al(OH)3 | B.第一电离能:Na< Mg <Al |
| C.还原性:Na> Mg >Al | D.电负性:Na> Mg >Al |
您最近一年使用:0次
2020-11-12更新
|
572次组卷
|
63卷引用:黑龙江省哈尔滨市第三中学校2019-2020学年高二上学期期末考试化学试题
黑龙江省哈尔滨市第三中学校2019-2020学年高二上学期期末考试化学试题黑龙江省哈尔滨市第三中学2019-2020学年高二上学期第一模块(期末)考试化学试题(已下线)09—10年泰州中学高二下学期期末考试化学卷(已下线)2013-2014宁夏银川一中高二下学期期末考试化学试卷2014-2015学年陕西省宝鸡中学高二下学期期末化学试卷A2014-2015学年吉林省汪清县第六中学高二下学期期末考试化学试卷2015-2016学年福建省泉州市晋江市平山中学高二上期末化学试卷2015-2016学年吉林东北师大附属实验高二下期末化学试卷2015-2016学年吉林梅河口五中高二下期末化学试卷2015-2016吉林东北师大附属实验学校净月实验学校高二下期末化学卷湖北省孝感市七校教学联盟2016-2017学年高二下学期期末考试化学试题新疆呼图壁县第一中学2016-2017学年高二下学期期末考试化学试题福建省福州市八县(市)协作校2016-2017学年高二下学期期末考试化学试题河北省深州中学2016-2017学年高二下学期期末考试化学试题内蒙古包头市第三十三中学2016-2017学年高二下学期期末考试化学试题福建省福州市八县协作校2016-2017学年高二下学期期末化学试题福建省福州三中2017-2018学年高二上学期期末考试化学试题黑龙江省鸡西市鸡东县第二中学2018-2019学年高二5月月考化学试题福建省泉州市泉港区第一中学2018-2019学年高二下学期期末考试化学试题吉林省长春市第二十九中学2019-2020学年高二上学期期末考试化学试题新疆乌鲁木齐市第四中学2019-2020学年高二下学期期末考试化学试题内蒙古集宁新世纪中学2020-2021学年高二下学期期末考试化学试题新疆乌鲁木齐市第101中学2021-2022学年高二下学期期末考试化学试题2014-2015学年宁夏宁大附中高二上学期期中考试化学试卷2014-2015宁夏银川市唐徕回民中学高二下学期3月月考化学试卷2014-2015吉林省吉林市第五十五中学高二下学期期中考试化学试卷2015-2016学年宁夏六盘山中学高二下第一次月考化学卷2015-2016学年山西太原五中高二下3月第二次周练化学卷2015-2016学年陕西西藏民族学院附中高二4月月考化学卷2015-2016学年山东省淄博市高青一中高二4月月考化学试卷2015-2016学年山西省右玉一中高二5月月考化学试卷2015-2016学年山西省朔州市右玉一中高二下5月月考化学试卷2016-2017学年四川省阆中中学高二上教学质检化学试卷2016-2017学年宁夏吴忠中学高二下学期第一次月考化学试卷2016-2017学年宁夏育才中学孔德校区高二下学期第一次(3月)月考化学试卷安徽省蚌埠市第二中学2016-2017学年高二下学期期中考试化学试题河北省馆陶县第一中学2016-2017学年高二下学期期中考试化学试题吉林省辽源五中2017-2018学年高二下学期第一次月考化学试题云南省玉溪市易门中学2017-2018学年高二上学期期中考试化学试题云南省玉溪市通海三中2018-2019学年高二上学期10月考试化学试题甘肃省玉门市第一中学2018-2019学年高二上学期期中考试化学试题山东省泰安市宁阳一中2018-2019学年高二上学期阶段性考试三(12月)化学试题贵州省剑河县第二高级中学2018-2019学年高二上学期12月份考试化学试题新疆兵团八师一四三团一中2018-2019学年高二下学期期中考试化学试题新疆石河子第二中学2018-2019学年高二下学期第一次月考化学试题2020届高三化学二轮物质结构题型专攻——原子结构与性质【基础专练】吉林省延边市长白山第一高级中学2019-2020学年高二下学期验收考试化学试卷安徽省安庆市太湖县太湖中学2019-2020学年高二下学期3月线上考试化学试题广西防城港市防城中学2019-2020学年高二下学期期中考试化学试题四川省平昌县驷马中学2020-2021学年高二上学期九月月考化学试题江苏省东台创新高级中学2019-2020学年高二下学期4月份月检测化学试题山东省淄博市般阳中学2020-2021学年高二上学期期中考试化学试题四川省乐山十校2020-2021学年高二上学期半期联考化学试题宁夏青铜峡市高级中学2020-2021学年高二下学期第一次月考化学试题河南省宏力学校2018-2019学年高二下学期期中考试化学试题广西蒙山县第一中学2018-2019学年高二下学期第二次月考化学试题新疆博尔塔拉蒙古自治州蒙古中学2020-2021学年高二下学期期中考试化学试题 四川省绵阳第一中学2022-2023学年高二上学期9月教学质量监测理科化学试题福建省永春美岭中学2021-2022学年高二下学期期中测试化学试题四川省乐山市沫若中学2022-2023学年高二上学期第一次月考化学试题云南省广南县二中2021-2022年学年高二下学期开学考试化学试题河南省焦作市2022-2023学年第四中学高二下学期3月月考 化学试卷新疆阿克苏市实验中学2022-2023学年高二下学期第一次月考化学试题
9-10高二下·黑龙江鹤岗·期末
解题方法
2 . 下列说法正确的有____________ 。
(1)每一周期元素都是从碱金属开始,以稀有气体结束
(2)f区都是副族元素,s区和p区的都是主族元素
(3)铝的第一电离能大于K的第一电离能
(4)B电负性和Si相近
(5)Ge的电负性为1.8,则其是典型的非金属
(6)半径:K+>Cl—
(7)酸性 HClO>H2SO4,碱性:NaOH > Mg(OH)2
(8)元素的最高正化合价=其最外层电子数=族序数
(1)每一周期元素都是从碱金属开始,以稀有气体结束
(2)f区都是副族元素,s区和p区的都是主族元素
(3)铝的第一电离能大于K的第一电离能
(4)B电负性和Si相近
(5)Ge的电负性为1.8,则其是典型的非金属
(6)半径:K+>Cl—
(7)酸性 HClO>H2SO4,碱性:NaOH > Mg(OH)2
(8)元素的最高正化合价=其最外层电子数=族序数
您最近一年使用:0次
3 . A、B、C、D、E、F六种常见元素且原子序数依次增大:A元素的一种原子的原子核内没有中子,B的基态原子2p轨道中有三个未成对电子,C是所有元素中电负性最大的元素,D是短周期且最外层只有一个未成对电子的非金属元素,E是主族元素且与F同周期,其最外能层上有两个运动状态不同的电子,F能形成红色(或砖红色)的F2O和黑色的FO两种氧化物。请回答下列问题:
(1)写出F元素原子基态时价层的电子排布式___
(2)B元素的第一电离能比氧元素的第一电离___ (填“大”或“小”),原因是____
(3)C元素与A元素形成的最简单氢化物比D元素与A元素形成的氢化物沸点高,原因是____ 。
(4)与E元素同周期且未成对电子数最多的元素的价层电子排布图___ 。
(5)A、B、F三种元素可形成[F(BA3)4]2+配离子,其中存在的化学键类型有____ (填字母)。
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若[F(BA3)4]2+配离子具有对称的空间构型, 且当[F(BA3)4]2+中的两个BA3被两个Br-取代时,能得到两种不同结构的产物,则[F(BA3)4]2+的空间构型为___ (填字母)。
a.平面正方形 b.正四面体形 c.三角锥形 d.V形
(6)D元素形成四种常见的含氧酸酸性由小到大的顺序___ ,且原因是___
(7)C和E能够形成化合物M,其晶胞结构如图所示,晶胞参数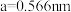 ,求晶体M的密度(
,求晶体M的密度( )
)____ 。(只列表达式即可)

(1)写出F元素原子基态时价层的电子排布式
(2)B元素的第一电离能比氧元素的第一电离
(3)C元素与A元素形成的最简单氢化物比D元素与A元素形成的氢化物沸点高,原因是
(4)与E元素同周期且未成对电子数最多的元素的价层电子排布图
(5)A、B、F三种元素可形成[F(BA3)4]2+配离子,其中存在的化学键类型有
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若[F(BA3)4]2+配离子具有对称的空间构型, 且当[F(BA3)4]2+中的两个BA3被两个Br-取代时,能得到两种不同结构的产物,则[F(BA3)4]2+的空间构型为
a.平面正方形 b.正四面体形 c.三角锥形 d.V形
(6)D元素形成四种常见的含氧酸酸性由小到大的顺序
(7)C和E能够形成化合物M,其晶胞结构如图所示,晶胞参数
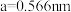 ,求晶体M的密度(
,求晶体M的密度( )
)
您最近一年使用:0次



