1 . 杂环化合物数量巨大、种类丰富、性能多样、应用广泛。
(1)由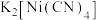 、
、 和吡嗪(
和吡嗪( 可用pyz表示)反应制得晶体,其化学式为
可用pyz表示)反应制得晶体,其化学式为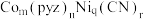 ,四方晶胞结构如图所示。基态Co原子的简化电子排布式为
,四方晶胞结构如图所示。基态Co原子的简化电子排布式为_______ ,C、N、O的第二电离能由大到小顺序为_______ ,晶体中 与
与 的配位数之比为
的配位数之比为_______ ,上述制得晶体的化学方程式为_______ 。 )分子中存在
)分子中存在 离域
离域 键,氮原子的杂化方式
键,氮原子的杂化方式_______ ;吡嗪的熔点_______ (填“大于”、“等于”、“小于”)哒嗪( );哒嗪在水中的溶解度大于苯的原因
);哒嗪在水中的溶解度大于苯的原因_______ 。
(3)休克尔规则可用于判断共轭结构的环状有机化合物是否有芳香性。若参与构成共轭 键电子的个数为
键电子的个数为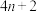 ,其中n为自然数,则此化合物就具有芳香性。下列物质中C、N、O均采用
,其中n为自然数,则此化合物就具有芳香性。下列物质中C、N、O均采用 杂化,其中具有芳香性的是
杂化,其中具有芳香性的是_______ 。
(1)由
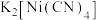 、
、 和吡嗪(
和吡嗪( 可用pyz表示)反应制得晶体,其化学式为
可用pyz表示)反应制得晶体,其化学式为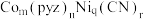 ,四方晶胞结构如图所示。基态Co原子的简化电子排布式为
,四方晶胞结构如图所示。基态Co原子的简化电子排布式为 与
与 的配位数之比为
的配位数之比为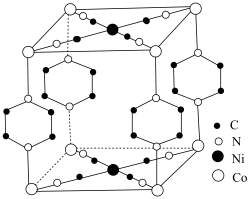
 )分子中存在
)分子中存在 离域
离域 键,氮原子的杂化方式
键,氮原子的杂化方式 );哒嗪在水中的溶解度大于苯的原因
);哒嗪在水中的溶解度大于苯的原因(3)休克尔规则可用于判断共轭结构的环状有机化合物是否有芳香性。若参与构成共轭
 键电子的个数为
键电子的个数为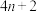 ,其中n为自然数,则此化合物就具有芳香性。下列物质中C、N、O均采用
,其中n为自然数,则此化合物就具有芳香性。下列物质中C、N、O均采用 杂化,其中具有芳香性的是
杂化,其中具有芳香性的是a. 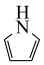 b.
b.  c.
c.  d.
d.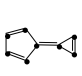
您最近一年使用:0次
名校
解题方法
2 . M、W、X、Y为原子序数依次增大的短周期主族元素,最外层电子数之和为16。W与Y的质子数之和是X的2倍。Z元素的基态原子未成对电子数为2,且价层电子的空间运动状态有6种。由5种元素形成的一种配位化合物结构如图所示。
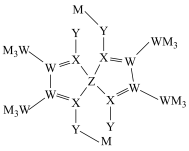
| A.同周期中第一电离能小于X的元素有4种 |
| B.简单氢化物的还原性:X<Y |
| C.1mol该物质中含配位键的数目为4NA |
| D.元素Z的化合价为0价 |
您最近一年使用:0次
2024-03-21更新
|
886次组卷
|
3卷引用:山东省济宁市2024届高三下学期一模考试化学试题
山东省济宁市2024届高三下学期一模考试化学试题辽宁省实验中学2023-2024学年高二下学期第一次月考化学试题(已下线)压轴题05?“位-构-性”元素推断(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
名校
解题方法
3 . 下列关于物质结构和性质的说法正确的是
A.第2周期元素中,第一电离能介于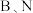 之间的有1种 之间的有1种 |
B.酸性: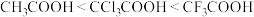 |
C. 与 与 中心原子的杂化方式相同,均为 中心原子的杂化方式相同,均为 形结构 形结构 |
D.乙二胺 的沸点比三甲胺 的沸点比三甲胺 高的原因是乙二胺存在分子间氢键,三甲胺存在分子内氢键 高的原因是乙二胺存在分子间氢键,三甲胺存在分子内氢键 |
您最近一年使用:0次
2024-03-21更新
|
617次组卷
|
4卷引用:2024届山东省邹城市北大新世纪高级中学高三下学期第三次模拟考试化学试题
2024届山东省邹城市北大新世纪高级中学高三下学期第三次模拟考试化学试题山东省菏泽市2024届高三一模考试化学试题(已下线)化学(山东卷02)-2024年高考押题预测卷山东省滕州市第一中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
4 . 一种有机物催化剂由原子序数依次递增的前20号元素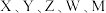 组成,结构式如下图。下列说法正确的是
组成,结构式如下图。下列说法正确的是
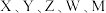 组成,结构式如下图。下列说法正确的是
组成,结构式如下图。下列说法正确的是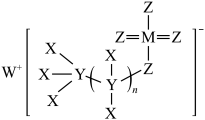
A.简单离子半径: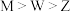 |
B.简单气态氢化物稳定性: |
C. 元素所在周期中,第一电离能大于 元素所在周期中,第一电离能大于 的元素有2种 的元素有2种 |
D.基态 原子电子占据的最高能层有9个原子轨道 原子电子占据的最高能层有9个原子轨道 |
您最近一年使用:0次
2024-03-15更新
|
1075次组卷
|
6卷引用:2024届山东省邹城市北大新世纪高级中学高三下学期第三次模拟考试化学试题
2024届山东省邹城市北大新世纪高级中学高三下学期第三次模拟考试化学试题山东省潍坊市2023-2024学年高三下学期一模化学试题(已下线)化学(山东卷02)-2024年高考押题预测卷山东省枣庄市第十六中学等校2023-2024学年高三下学期5月(一模)考试化学试题(已下线)第一章 原子结构与性质(B卷) 四川省成都市石室中学2023-2024学年高二下学期4月月考化学试卷
名校
5 . 铁镁合金储氢材料,晶胞结构如图所示,晶胞参数为apm,储氢后H原子以正八面体的配位模式有序分布在Fe原子的周围,H原子与Fe原子之间的最短距离为晶胞参数的1/4。

回答下列问题
(1)同周期中,第一电离能小于Mg的元素有_______ 种,基态Fe原子的价电子排布式为_______ ,Fe位于元素周期表中的_______ 区。
(2)储氢后晶体的化学式为_______ ,Mg原子占据Fe原子形成的_______ 空隙,两个H原子之间的最短距离为_______ ,该储氢材料中氢的密度ρ为_______  (用含a的代数式表示)。
(用含a的代数式表示)。
(3) (氨硼烷)也是具有潜力的化学储氢材料之一,
(氨硼烷)也是具有潜力的化学储氢材料之一, 中
中 的键角
的键角_______  中
中 的键角(填>,<或=)。
的键角(填>,<或=)。

回答下列问题
(1)同周期中,第一电离能小于Mg的元素有
(2)储氢后晶体的化学式为
 (用含a的代数式表示)。
(用含a的代数式表示)。(3)
 (氨硼烷)也是具有潜力的化学储氢材料之一,
(氨硼烷)也是具有潜力的化学储氢材料之一, 中
中 的键角
的键角 中
中 的键角(填>,<或=)。
的键角(填>,<或=)。
您最近一年使用:0次
2023-03-03更新
|
781次组卷
|
3卷引用:山东省济宁市2023届高三一模考试(3月)化学试题
名校
解题方法
6 . W、X、Y、Z均为周期表中前两周期元素,其原子序数依次增大,X原子基态电子排布中无单电子。四种元素可以组成 型离子化合物,阴阳离子皆由两种元素组成,且均为正四面体形。下列说法错误的是
型离子化合物,阴阳离子皆由两种元素组成,且均为正四面体形。下列说法错误的是
 型离子化合物,阴阳离子皆由两种元素组成,且均为正四面体形。下列说法错误的是
型离子化合物,阴阳离子皆由两种元素组成,且均为正四面体形。下列说法错误的是| A.阴阳离子中都含有配位键 | B.第一电离能:X<Y<Z |
| C.Y与Z可形成三角锥形的分子 | D.简单氢化物的还原性:Y<Z |
您最近一年使用:0次
2023-03-03更新
|
1038次组卷
|
6卷引用:山东省济宁市2023届高三一模考试(3月)化学试题
山东省济宁市2023届高三一模考试(3月)化学试题河北省部分学校2023届高三下学期二模联考化学试题(已下线)专题07 元素周期表和元素周期律(已下线)元素周期表 元素周期律山东省烟台市第一中学2023-2024学年高三下学期3月月考化学试题(已下线)单项选择题1-5
7 . W、X、Y、Z为原子序数依次增大的短周期元素,W位于s区,并且和X、Y、Z分别形成原子个数为4、3、2的 分子A、B、C,常温下A呈液态。下列说法错误的是
分子A、B、C,常温下A呈液态。下列说法错误的是
 分子A、B、C,常温下A呈液态。下列说法错误的是
分子A、B、C,常温下A呈液态。下列说法错误的是| A.由W、X、Z三种元素组成的化合物酸性比WZ弱 |
| B.元素Y的第一电离能小于同周期相邻两种元素 |
| C.原子半径:W<X<Z<Y |
| D.元素X的一种单质可用于自来水的杀菌消毒 |
您最近一年使用:0次
8 . 短周期主族元素X、Y、Z、W原子序数依次增大,X原子核外电子只有一种自旋取向,Y、Z两种原子核外s能级上的电子总数与p能级上电子总数相等,W原子的价电子中,在不同形状的原子轨道中运动的电子数之比为2:1。下列说法正确的是
| A.W的第一电离能比同周期相邻元素的小 |
| B.原子半径:r(X)<r(Y)<r(Z)<r(W) |
| C.工业上电解熔融化合物ZY制备单质Z |
| D.W的最高价氧化物不可能是非极性分子 |
您最近一年使用:0次
2022-03-03更新
|
821次组卷
|
4卷引用:山东省济宁市2022届高三下学期3月一模考试化学试题
山东省济宁市2022届高三下学期3月一模考试化学试题(已下线)提升卷05-【新高考新题型】2022年高考化学选择题标准化练习20卷(山东专用)(已下线)必刷卷05-2022年高考化学考前信息必刷卷(山东专用)贵州省瓮安中学2022-2023学年高二下学期3月月考化学试题
名校
9 . 常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物溶液(浓度均为0.01mol·L-1)的pH和原子半径、原子序数的关系如图所示。下列说法错误的是


| A.第一电离能:W>Z>Y>X |
| B.简单离子的半径:Y>Z>W>X |
| C.W的氢化物空间构型不一定是三角锥形 |
| D.Z的单质具有强氧化性和漂白性 |
您最近一年使用:0次
2021-05-15更新
|
1516次组卷
|
9卷引用:山东省济宁市2021届高三下学期二模考试化学试题
山东省济宁市2021届高三下学期二模考试化学试题天津市和平区2022届高三第二次质量调查化学试题(已下线)专题06 物质结构 元素周期律-备战2022年高考化学真题及地市好题专项集训【山东专用】山东省济南市山东师范大学附属中学2021-2022学年高三上学期期中考试化学试题黑龙江省鸡西实验中学2021-2022学年高二下学期第一次月考化学试题选择性必修第二册 期末学业水平检测(已下线)题型9 元素“位—构-性”关系的综合应用-高考必备50个题型陕西省西安市陕西师范大学附属中学渭北中学2022-2023学年高二下学期5月月考化学试题山东省泰安市新泰第一中学老校区(新泰中学)2023-2024学年高二下学期第一次月考化学试题
名校
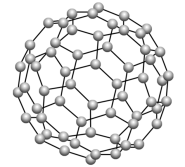
10 . C60具有完美的球形结构,如图所示。之后Si60、N60等球形分子被不断制备出来。下列选项正确的是

| A.Si 的核外电子排布式为3s23p2 |
| B.C 和 N 元素中第一电离能较大的是C |
| C.C60属于共价晶体,C 原子的杂化类型为sp2 |
| D.一个 N60的分子中含有 90 个共价单键 |
您最近一年使用:0次



