1 . 血红蛋白结合 后的结构如图所示,
后的结构如图所示, 也可与血红蛋白结合。下列说法错误的是
也可与血红蛋白结合。下列说法错误的是
 后的结构如图所示,
后的结构如图所示, 也可与血红蛋白结合。下列说法错误的是
也可与血红蛋白结合。下列说法错误的是
A.血红蛋白中心离子 与卟啉环形成6个螯合键 与卟啉环形成6个螯合键 |
B. 与血红蛋白结合时, 与血红蛋白结合时, 原子提供孤电子对 原子提供孤电子对 |
C.第一电离能: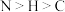 |
D.基态 含有4个未成对电子 含有4个未成对电子 |
您最近一年使用:0次
名校
2 . N-杂环取代修饰的菲啰啉- 催化剂(M)结构如图。已知
催化剂(M)结构如图。已知 原子序数为75,M中五元环含有大
原子序数为75,M中五元环含有大 键。下列说法错误的是
键。下列说法错误的是
 催化剂(M)结构如图。已知
催化剂(M)结构如图。已知 原子序数为75,M中五元环含有大
原子序数为75,M中五元环含有大 键。下列说法错误的是
键。下列说法错误的是
A. 基态原子价电子排布式为 基态原子价电子排布式为 | B.M中元素的第一电离能: |
C.配体中 的键长比 的键长比 分子中的键长短 分子中的键长短 | D.M中一个五元环 电子数为6 电子数为6 |
您最近一年使用:0次
2024-05-21更新
|
125次组卷
|
2卷引用:2024届山东省潍坊市四县联考高三下学期三模化学试题
3 . 某储氢材料前驱体结构如下图,M、W、X、Y、Z五种元素原子序数依次增大,基态Z原子的电子填充了3个能级,其中有2个未成对电子。下列说法正确的是
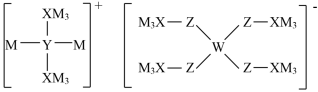
| A.氢化物沸点高低:X<Y |
| B.Y和W位于同一主族 |
| C.同周期主族元素中,第一电离能比Y大的元素有2种 |
| D.阴、阳离子中均有配位键 |
您最近一年使用:0次
4 . 已知W、X、Y、Z是原子序数依次增大的短周期主族元素,W、Y、Z分别处于不同周期,W、X、Y、Z形成的化合物 是核酸采样管中红色液体的主要成分之一,其结构如图所示。下列说法正确的是
是核酸采样管中红色液体的主要成分之一,其结构如图所示。下列说法正确的是
 是核酸采样管中红色液体的主要成分之一,其结构如图所示。下列说法正确的是
是核酸采样管中红色液体的主要成分之一,其结构如图所示。下列说法正确的是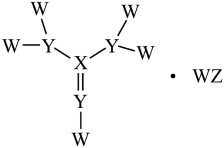
| A.W、X、Y、Z的单质在常温下均为气体 |
| B.W分别与X、Y、Z结合均可以形成含有相同电子数的分子 |
| C.Y的氧化物对应的水化物为强酸 |
| D.元素的第一电离能:X>Y>W |
您最近一年使用:0次
名校
解题方法
5 . 一种有机物催化剂由原子序数依次递增的前20号元素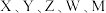 组成,结构式如下图。下列说法正确的是
组成,结构式如下图。下列说法正确的是
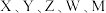 组成,结构式如下图。下列说法正确的是
组成,结构式如下图。下列说法正确的是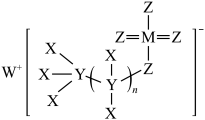
A.简单离子半径: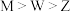 |
B.简单气态氢化物稳定性: |
C. 元素所在周期中,第一电离能大于 元素所在周期中,第一电离能大于 的元素有2种 的元素有2种 |
D.基态 原子电子占据的最高能层有9个原子轨道 原子电子占据的最高能层有9个原子轨道 |
您最近一年使用:0次
2024-03-15更新
|
1075次组卷
|
6卷引用:山东省潍坊市2023-2024学年高三下学期一模化学试题
山东省潍坊市2023-2024学年高三下学期一模化学试题(已下线)化学(山东卷02)-2024年高考押题预测卷2024届山东省邹城市北大新世纪高级中学高三下学期第三次模拟考试化学试题山东省枣庄市第十六中学等校2023-2024学年高三下学期5月(一模)考试化学试题(已下线)第一章 原子结构与性质(B卷) 四川省成都市石室中学2023-2024学年高二下学期4月月考化学试卷
名校
解题方法
6 . 过渡元素在生活、生产和科技等方面有广泛的用途。现代污水处理工艺中常利用聚合铁{简称PFS,化学式为:[Fe2(OH)n(SO4)3-n/2]m,n<5,m<10}在水体中形成絮状物,以吸附重金属离子。下列说法中不正确的是
| 元素 | Mn | Fe | |
| 电离能(kJ·mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
| A.PFS中铁显+3价 |
| B.二价铁离子的价电子排布式是3d44s2 |
| C.由FeSO4溶液制PFS需经过氧化、水解和聚合的过程 |
| D.由表可知气态Fe2+再失去一个电子比气态Mn2+再失去一个电子难 |
您最近一年使用:0次
2024-02-08更新
|
342次组卷
|
2卷引用:2024届山东省潍坊市昌乐二中高三模拟预测化学试题
名校
7 . 对下列一些实验事实的理论解释,错误的是
| 选项 | 实验事实 | 理论解释 |
| A | P原子的第一电离能大于S原子 | 磷原子的半径比硫原子的半径大 |
| B | 乙烯的化学性质比乙烷活泼 | 乙烯分子结构中存在π键 |
| C | 向加入过量氨水的硫酸铜溶液中加入乙醇,将析出深蓝色晶体 | 乙醇的加入降低了[Cu(NH3)4]SO4·H2O的溶解度 |
| D | HCl气体极易溶于水 | HCl和H2O均为极性分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
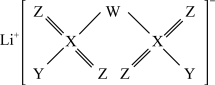
8 . 一种用作锂电池离子导体的锂盐结构如图所示,其中W满足8e-稳定结构,X位于第3周期,X原子的电子数为Z原子电子数的两倍,W、Z、Y位于同一周期。下列叙述正确的是

| A.原子半径:X>Y>Z |
| B.氢化物的沸点:X>Z |
| C.同周期中第一电离能小于W的元素有5种 |
| D.W、X在其最高价含氧酸分子中的杂化方式相同 |
您最近一年使用:0次
解题方法
9 . 有机—无机复合钙钛矿( )型材料在太阳能电池及发光二极管等方面具有很好的应用前景,一种复合材料和
)型材料在太阳能电池及发光二极管等方面具有很好的应用前景,一种复合材料和 (立方晶系)的晶胞结构如图所示。
(立方晶系)的晶胞结构如图所示。
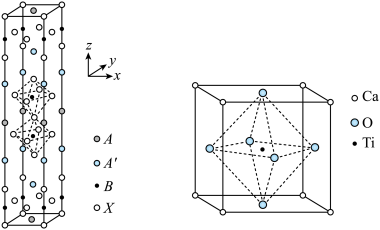
已知:A为间隔的阳离子,例如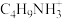 、
、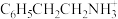 等;A'为单一组分钙钛阳离子,例如
等;A'为单一组分钙钛阳离子,例如 、
、 、
、 等;B为单一组分钙钛矿中心离子
等;B为单一组分钙钛矿中心离子 、
、 等,X为单一组分钙钛矿的阴离子,例如
等,X为单一组分钙钛矿的阴离子,例如 、
、 或
或 等卤素离子。
等卤素离子。
回答下列问题:
(1)基态Ti原子的价电子排布式为___________ 。
(2)H、C、N、O四种元素电负性由大到小的顺序为___________ ;第一电离能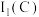 、
、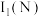 、
、 由大到小的顺序为
由大到小的顺序为___________ 。
(3) 中C的杂化方式为
中C的杂化方式为___________ ;正丁胺(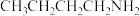 )的沸点为77.8℃,正丁醇(
)的沸点为77.8℃,正丁醇( )的沸点为117.6℃,正丁胺沸点低的原因是
)的沸点为117.6℃,正丁胺沸点低的原因是___________ 。
(4) 中Ca的配位数为
中Ca的配位数为___________ ;A为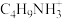 ,A'为
,A'为 ,B为
,B为 ,X为
,X为 ,晶胞参数为a nm和c nm,该晶体的密度为
,晶胞参数为a nm和c nm,该晶体的密度为___________  。
。
 )型材料在太阳能电池及发光二极管等方面具有很好的应用前景,一种复合材料和
)型材料在太阳能电池及发光二极管等方面具有很好的应用前景,一种复合材料和 (立方晶系)的晶胞结构如图所示。
(立方晶系)的晶胞结构如图所示。
已知:A为间隔的阳离子,例如
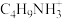 、
、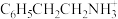 等;A'为单一组分钙钛阳离子,例如
等;A'为单一组分钙钛阳离子,例如 、
、 、
、 等;B为单一组分钙钛矿中心离子
等;B为单一组分钙钛矿中心离子 、
、 等,X为单一组分钙钛矿的阴离子,例如
等,X为单一组分钙钛矿的阴离子,例如 、
、 或
或 等卤素离子。
等卤素离子。回答下列问题:
(1)基态Ti原子的价电子排布式为
(2)H、C、N、O四种元素电负性由大到小的顺序为
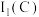 、
、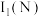 、
、 由大到小的顺序为
由大到小的顺序为(3)
 中C的杂化方式为
中C的杂化方式为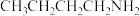 )的沸点为77.8℃,正丁醇(
)的沸点为77.8℃,正丁醇( )的沸点为117.6℃,正丁胺沸点低的原因是
)的沸点为117.6℃,正丁胺沸点低的原因是(4)
 中Ca的配位数为
中Ca的配位数为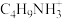 ,A'为
,A'为 ,B为
,B为 ,X为
,X为 ,晶胞参数为a nm和c nm,该晶体的密度为
,晶胞参数为a nm和c nm,该晶体的密度为 。
。
您最近一年使用:0次
名校
解题方法
10 . 某种天然沸石的化学式为 ,其中元素X、Y、Z、R、W原子序数依次增大,且占据四个不同周期。Y在地壳中含量最高,在该化合物中R显示其最高价态,基态W原子的核外电子恰好填满10个原子轨道。下列说法错误的是
,其中元素X、Y、Z、R、W原子序数依次增大,且占据四个不同周期。Y在地壳中含量最高,在该化合物中R显示其最高价态,基态W原子的核外电子恰好填满10个原子轨道。下列说法错误的是
 ,其中元素X、Y、Z、R、W原子序数依次增大,且占据四个不同周期。Y在地壳中含量最高,在该化合物中R显示其最高价态,基态W原子的核外电子恰好填满10个原子轨道。下列说法错误的是
,其中元素X、Y、Z、R、W原子序数依次增大,且占据四个不同周期。Y在地壳中含量最高,在该化合物中R显示其最高价态,基态W原子的核外电子恰好填满10个原子轨道。下列说法错误的是A.简单离子半径: | B.第一电离能: |
C.最简单氢化物稳定性: | D.氯化物熔点: |
您最近一年使用:0次
2023-03-31更新
|
489次组卷
|
2卷引用:山东省潍坊市2023届高三下学期学科核心素养测评化学试题



