1 . 按要求回答下列问题:
(1)消毒液的组成元素中,基态O原子的电子排布式是______ ,基态Cl原子未成对电子数为_____ 个。
(2)与氧元素相邻的氮元素的第一电离能的大小顺序为_______ (填元素符号),氧元素和氮元素的非金属性的大小顺序为________ (填元素符号)
(3)某元素原子的最外层电子构型为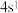 ,元素周期表的位置第
,元素周期表的位置第____ 周期,第_____ 族,它属于____ 区元素。
(1)消毒液的组成元素中,基态O原子的电子排布式是
(2)与氧元素相邻的氮元素的第一电离能的大小顺序为
(3)某元素原子的最外层电子构型为
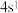 ,元素周期表的位置第
,元素周期表的位置第
您最近一年使用:0次
2 . 依据原子结构知识回答下列问题。
(1)下列有关说法错误的是___________。
(2)基态V原子中具有___________ 种不同能量的电子,具有___________ 种不同空间运动状态的电子,具有___________ 种不同运动状态的电子。
(3)基态Cu原子的简化电子排布式为___________ ,基态Se原子的价电子轨道表示式为___________ ,基态Mn2+的价电子排布式为___________ 。
(1)下列有关说法错误的是___________。
| A.简单离子的还原性:P3->O2->F- |
| B.在元素周期表第二周期中元素原子的第一电离能介于硼和氮之间的元素有两种 |
| C.焰色试验与电子跃迁有关 |
| D.基态铝原子占据的最高能级的电子云轮廓图的形状为球形 |
(3)基态Cu原子的简化电子排布式为
您最近一年使用:0次
3 . 按要求回答下列问题:
(1)已知A和B为第三周期元素,其第一至第四电离能如表所示:
A通常显___________ 价,B的基态原子核外电子排布式为___________ 。
(2)如图为元素周期表中部分元素某种性质(X值)随原子序数变化的关系:___________ (填元素符号)。
②同主族内不同元素的X值变化的特点是___________ ;同周期内,随着原子序数的增大,X值的变化总趋势是___________ 。周期表中X值的这种变化特点体现了元素性质的___________ 变化规律。
③X值较小的元素集中在元素周期表的___________ (填字母)。
a.左下角 b.右上角 c.分界线附近
④下列关于元素此性质的说法正确的是___________ (填字母)。
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱
(1)已知A和B为第三周期元素,其第一至第四电离能如表所示:
电离能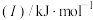 |  | 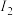 | 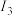 | 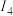 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
(2)如图为元素周期表中部分元素某种性质(X值)随原子序数变化的关系:
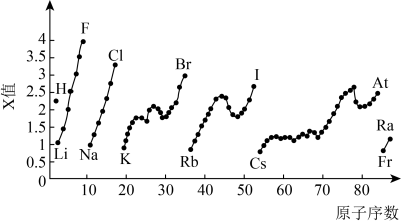
②同主族内不同元素的X值变化的特点是
③X值较小的元素集中在元素周期表的
a.左下角 b.右上角 c.分界线附近
④下列关于元素此性质的说法正确的是
a.X值可反映元素最高正化合价的变化规律
b.X值可反映原子在分子中吸引电子的能力
c.X值的大小可用来衡量元素金属性和非金属性的强弱
您最近一年使用:0次
2024-04-27更新
|
38次组卷
|
2卷引用:黑龙江省绥化市绥棱县第一中学2023-2024学年高二上学期1月期末化学试题
4 . 硫代硫酸盐是一类具有应用前景的浸金试剂。硫代碳酸根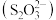 可看作是
可看作是 中的一个O原子被S原子取代的产物。
中的一个O原子被S原子取代的产物。
(1)基态S原子价层电子排布式是_______ 。
(2)比较S原子和O原子的第一电离能大小,从原子结构的角度说明理由:_______ 。
(3) 的空间结构是
的空间结构是_______ 。
(4)浸金时, 作为配体可提供孤电子对与
作为配体可提供孤电子对与 形成
形成 。分别判断
。分别判断 中的中心S原子和端基S原子能否做配位原子并说明理由:
中的中心S原子和端基S原子能否做配位原子并说明理由:_______ 。
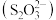 可看作是
可看作是 中的一个O原子被S原子取代的产物。
中的一个O原子被S原子取代的产物。(1)基态S原子价层电子排布式是
(2)比较S原子和O原子的第一电离能大小,从原子结构的角度说明理由:
(3)
 的空间结构是
的空间结构是(4)浸金时,
 作为配体可提供孤电子对与
作为配体可提供孤电子对与 形成
形成 。分别判断
。分别判断 中的中心S原子和端基S原子能否做配位原子并说明理由:
中的中心S原子和端基S原子能否做配位原子并说明理由:
您最近一年使用:0次
5 . 回答下列问题:
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是______(填标号)。
(2)Fe在元素周期表中的位置是___ ,基态 与
与 中未成对的电子数之比为
中未成对的电子数之比为______ 。
(3)原子中运动的电子有两种相反的自旋扶态,若一种子旋状态用 表示,与之相反的用
表示,与之相反的用 表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为
表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为______ 。
(4)下列曲线表示氧族元素性质随核电荷数的突化趋势,正确的是______ 。
a. b.
b.
c. d.
d.
(5)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能( )。第二周期部分元素
)。第二周期部分元素 的变化趋势如图所示,其中除氮元素外,其他元素的
的变化趋势如图所示,其中除氮元素外,其他元素的 自左而右依次增大。而氮元素的
自左而右依次增大。而氮元素的 呈现异常的原因是
呈现异常的原因是______ 。

(6) 是离子化合物,如图是Born-Haber循环。
是离子化合物,如图是Born-Haber循环。

可知,Li原子的第一电离能为______  .
.
(7)如表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据:
下列说法正确的是______(填字母)。
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是______(填标号)。
A. | B. |
C. | D. |
(2)Fe在元素周期表中的位置是
 与
与 中未成对的电子数之比为
中未成对的电子数之比为(3)原子中运动的电子有两种相反的自旋扶态,若一种子旋状态用
 表示,与之相反的用
表示,与之相反的用 表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为
表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为(4)下列曲线表示氧族元素性质随核电荷数的突化趋势,正确的是
a.
 b.
b.
c.
 d.
d.
(5)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(
 )。第二周期部分元素
)。第二周期部分元素 的变化趋势如图所示,其中除氮元素外,其他元素的
的变化趋势如图所示,其中除氮元素外,其他元素的 自左而右依次增大。而氮元素的
自左而右依次增大。而氮元素的 呈现异常的原因是
呈现异常的原因是
(6)
 是离子化合物,如图是Born-Haber循环。
是离子化合物,如图是Born-Haber循环。
可知,Li原子的第一电离能为
 .
.(7)如表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据:
| 元素 |  |  |  |
| 甲 | 5.7 | 47.1 | 71.8 |
| 乙 | 7.7 | 15.1 | 80.3 |
| 丙 | 13.0 | 23.9 | 40.0 |
| 丁 | 15.7 | 27.6 | 40.7 |
| A.甲的金属性比乙强 | B.乙的化合价为+1价 |
| C.丙不可能为非金属元素 | D.丁一定为金属元素 |
您最近一年使用:0次
6 . 北宋卷轴画《千里江山图》,颜色绚丽,由石绿、雌黄、赭石、阵磲、朱砂等颜料绘制而成,颜料中含有硫、砷、铜、锌、钛、铁等元素。
(1)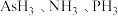 热稳定性由大到小的顺序为
热稳定性由大到小的顺序为_____ 。
(2) 属于元素周期表中的
属于元素周期表中的_____ 区;基态 原子的电子排布式为
原子的电子排布式为_____ ;基态硫原子核外电子的空间运动状态有_____ 种;基态 的价层电子的轨道表示式为
的价层电子的轨道表示式为_____ 。
(3) 的第二电离能
的第二电离能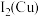
_____  的第二电离能
的第二电离能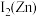 (填“>”或“<”),理由为
(填“>”或“<”),理由为_____ 。
(1)
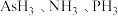 热稳定性由大到小的顺序为
热稳定性由大到小的顺序为(2)
 属于元素周期表中的
属于元素周期表中的 原子的电子排布式为
原子的电子排布式为 的价层电子的轨道表示式为
的价层电子的轨道表示式为(3)
 的第二电离能
的第二电离能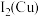
 的第二电离能
的第二电离能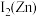 (填“>”或“<”),理由为
(填“>”或“<”),理由为
您最近一年使用:0次
7 . 按要求解答下列各题。
(1)黄铜是人类最早使用的合金之一,主要由 和
和 组成。基态
组成。基态 原子的核外价层电子排布图为
原子的核外价层电子排布图为_______ ;第二电离能
_______ (填“<”“>”或“=”)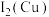 。
。
(2) 和
和 中
中 之间以双键结合,
之间以双键结合, 之间以单键结合。请你预测
之间以单键结合。请你预测 和
和 分子的空间结构为
分子的空间结构为_______ 。 分子中
分子中
_______  分子中
分子中 (选填“<”“>”或“=”)。
(选填“<”“>”或“=”)。
(3)甲醇的沸点(64.7℃)介于水和甲硫醇 ,其原因是
,其原因是_______ 。
(1)黄铜是人类最早使用的合金之一,主要由
 和
和 组成。基态
组成。基态 原子的核外价层电子排布图为
原子的核外价层电子排布图为
 。
。(2)
 和
和 中
中 之间以双键结合,
之间以双键结合, 之间以单键结合。请你预测
之间以单键结合。请你预测 和
和 分子的空间结构为
分子的空间结构为 分子中
分子中
 分子中
分子中 (选填“<”“>”或“=”)。
(选填“<”“>”或“=”)。(3)甲醇的沸点(64.7℃)介于水和甲硫醇
 ,其原因是
,其原因是
您最近一年使用:0次
8 . Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题
(1)钠在火焰上灼烧的黄光是一种___________ (填字母)。
A.吸收光谱 B.发射光谱
钠元素原子核外最外层电子的排布图是___________ ;能量最高的电子有___________ 个,其电子云形状为___________ 。
(2)下列Mg原子的核外电子排布式中,能量最高的是___________ ,能量最低的是___________ (填序号)。
a. b.
b.
c. d.
d.
(3) 所含的化学键类型:
所含的化学键类型:___________ ;属于___________ 分子(填极性或非极性)
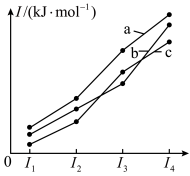
(4)磷及其化合物与人类生产、生活密切相关。如图表示碳、硅、磷元素的四级电离能(失去第四个电子)变化趋势,其中表示磷的曲线是___________ (填标号)。
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
钠元素原子核外最外层电子的排布图是
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.
 b.
b.
c.
 d.
d.
(3)
 所含的化学键类型:
所含的化学键类型:(4)磷及其化合物与人类生产、生活密切相关。如图表示碳、硅、磷元素的四级电离能(失去第四个电子)变化趋势,其中表示磷的曲线是

您最近一年使用:0次
9 . 填空
(1)基态铜原子价层电子排布图为______ ﹔已知Cu第一电离能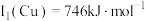 ,Fe第一电离能
,Fe第一电离能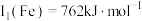 ,则
,则
______  (填“>”、“=”或“<”),其主要原因是
(填“>”、“=”或“<”),其主要原因是______ ;
(2) 和
和 的中心原子的杂化轨道类型分别为
的中心原子的杂化轨道类型分别为______ ,试判断 和
和 的键角大小关系:
的键角大小关系:
______  ,说明原因:
,说明原因:______
(3)比较 和
和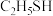 的酸性:
的酸性:
______ 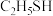 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(1)基态铜原子价层电子排布图为
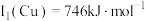 ,Fe第一电离能
,Fe第一电离能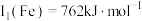 ,则
,则
 (填“>”、“=”或“<”),其主要原因是
(填“>”、“=”或“<”),其主要原因是(2)
 和
和 的中心原子的杂化轨道类型分别为
的中心原子的杂化轨道类型分别为 和
和 的键角大小关系:
的键角大小关系:
 ,说明原因:
,说明原因:(3)比较
 和
和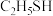 的酸性:
的酸性:
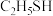 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
您最近一年使用:0次
10 . 回答下列问题
(1)①写出小苏打的化学式___________ ;
②写出Fe2+的价电子排布式___________ 。
(2)实验室用软锰矿和浓盐酸制氯气,写出该反应的化学方程式___________ 。
(3)在常温下,0.1mol/LCH3COONa溶液的pH=9,则溶液中由水电离出来的c(OH-)=___________
(4)火箭发射可以用肼(N2H4,液态)作燃料,NO2作氧化剂,两者反应生成N2和水蒸气。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+66.4kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol
请写出N2H4(l)与NO2反应的热化学方程式___________
(5)下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示)。
关于元素R的下列推断中,正确的是___________ (用相应的编号填写)
①R元素基态原子的电子排布式为1s22s2
②R元素位于元素周期表中第ⅡA族
③R元素的最高正化合价为+2价
④R元素的第一电离能高于同周期相邻元素的第一电离能
(1)①写出小苏打的化学式
②写出Fe2+的价电子排布式
(2)实验室用软锰矿和浓盐酸制氯气,写出该反应的化学方程式
(3)在常温下,0.1mol/LCH3COONa溶液的pH=9,则溶液中由水电离出来的c(OH-)=
(4)火箭发射可以用肼(N2H4,液态)作燃料,NO2作氧化剂,两者反应生成N2和水蒸气。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+66.4kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol
请写出N2H4(l)与NO2反应的热化学方程式
(5)下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示)。
| 元素 | 电离能/(kJ·mol-1) | |||||
| I1 | I2 | I3 | I4 | I5 | …… | |
| R | 740 | 1500 | 7700 | 10500 | 13630 | …… |
①R元素基态原子的电子排布式为1s22s2
②R元素位于元素周期表中第ⅡA族
③R元素的最高正化合价为+2价
④R元素的第一电离能高于同周期相邻元素的第一电离能
您最近一年使用:0次



