1 . 硫代硫酸盐是一类具有应用前景的浸金试剂。硫代碳酸根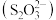 可看作是
可看作是 中的一个O原子被S原子取代的产物。
中的一个O原子被S原子取代的产物。
(1)基态S原子价层电子排布式是_______ 。
(2)比较S原子和O原子的第一电离能大小,从原子结构的角度说明理由:_______ 。
(3) 的空间结构是
的空间结构是_______ 。
(4)浸金时, 作为配体可提供孤电子对与
作为配体可提供孤电子对与 形成
形成 。分别判断
。分别判断 中的中心S原子和端基S原子能否做配位原子并说明理由:
中的中心S原子和端基S原子能否做配位原子并说明理由:_______ 。
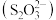 可看作是
可看作是 中的一个O原子被S原子取代的产物。
中的一个O原子被S原子取代的产物。(1)基态S原子价层电子排布式是
(2)比较S原子和O原子的第一电离能大小,从原子结构的角度说明理由:
(3)
 的空间结构是
的空间结构是(4)浸金时,
 作为配体可提供孤电子对与
作为配体可提供孤电子对与 形成
形成 。分别判断
。分别判断 中的中心S原子和端基S原子能否做配位原子并说明理由:
中的中心S原子和端基S原子能否做配位原子并说明理由:
您最近一年使用:0次
2 . 回答下列问题:
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是______(填标号)。
(2)Fe在元素周期表中的位置是___ ,基态 与
与 中未成对的电子数之比为
中未成对的电子数之比为______ 。
(3)原子中运动的电子有两种相反的自旋扶态,若一种子旋状态用 表示,与之相反的用
表示,与之相反的用 表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为
表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为______ 。
(4)下列曲线表示氧族元素性质随核电荷数的突化趋势,正确的是______ 。
a. b.
b.
c. d.
d.
(5)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能( )。第二周期部分元素
)。第二周期部分元素 的变化趋势如图所示,其中除氮元素外,其他元素的
的变化趋势如图所示,其中除氮元素外,其他元素的 自左而右依次增大。而氮元素的
自左而右依次增大。而氮元素的 呈现异常的原因是
呈现异常的原因是______ 。

(6) 是离子化合物,如图是Born-Haber循环。
是离子化合物,如图是Born-Haber循环。

可知,Li原子的第一电离能为______  .
.
(7)如表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据:
下列说法正确的是______(填字母)。
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是______(填标号)。
A. | B. |
C. | D. |
(2)Fe在元素周期表中的位置是
 与
与 中未成对的电子数之比为
中未成对的电子数之比为(3)原子中运动的电子有两种相反的自旋扶态,若一种子旋状态用
 表示,与之相反的用
表示,与之相反的用 表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为
表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为(4)下列曲线表示氧族元素性质随核电荷数的突化趋势,正确的是
a.
 b.
b.
c.
 d.
d.
(5)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(
 )。第二周期部分元素
)。第二周期部分元素 的变化趋势如图所示,其中除氮元素外,其他元素的
的变化趋势如图所示,其中除氮元素外,其他元素的 自左而右依次增大。而氮元素的
自左而右依次增大。而氮元素的 呈现异常的原因是
呈现异常的原因是
(6)
 是离子化合物,如图是Born-Haber循环。
是离子化合物,如图是Born-Haber循环。
可知,Li原子的第一电离能为
 .
.(7)如表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据:
| 元素 |  |  |  |
| 甲 | 5.7 | 47.1 | 71.8 |
| 乙 | 7.7 | 15.1 | 80.3 |
| 丙 | 13.0 | 23.9 | 40.0 |
| 丁 | 15.7 | 27.6 | 40.7 |
| A.甲的金属性比乙强 | B.乙的化合价为+1价 |
| C.丙不可能为非金属元素 | D.丁一定为金属元素 |
您最近一年使用:0次
3 . Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题
(1)钠在火焰上灼烧的黄光是一种___________ (填字母)。
A.吸收光谱 B.发射光谱
钠元素原子核外最外层电子的排布图是___________ ;能量最高的电子有___________ 个,其电子云形状为___________ 。
(2)下列Mg原子的核外电子排布式中,能量最高的是___________ ,能量最低的是___________ (填序号)。
a. b.
b.
c. d.
d.
(3) 所含的化学键类型:
所含的化学键类型:___________ ;属于___________ 分子(填极性或非极性)
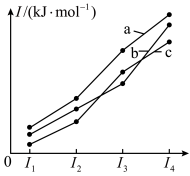
(4)磷及其化合物与人类生产、生活密切相关。如图表示碳、硅、磷元素的四级电离能(失去第四个电子)变化趋势,其中表示磷的曲线是___________ (填标号)。
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
钠元素原子核外最外层电子的排布图是
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.
 b.
b.
c.
 d.
d.
(3)
 所含的化学键类型:
所含的化学键类型:(4)磷及其化合物与人类生产、生活密切相关。如图表示碳、硅、磷元素的四级电离能(失去第四个电子)变化趋势,其中表示磷的曲线是

您最近一年使用:0次
4 . 回答下列问题
(1)①写出小苏打的化学式___________ ;
②写出Fe2+的价电子排布式___________ 。
(2)实验室用软锰矿和浓盐酸制氯气,写出该反应的化学方程式___________ 。
(3)在常温下,0.1mol/LCH3COONa溶液的pH=9,则溶液中由水电离出来的c(OH-)=___________
(4)火箭发射可以用肼(N2H4,液态)作燃料,NO2作氧化剂,两者反应生成N2和水蒸气。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+66.4kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol
请写出N2H4(l)与NO2反应的热化学方程式___________
(5)下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示)。
关于元素R的下列推断中,正确的是___________ (用相应的编号填写)
①R元素基态原子的电子排布式为1s22s2
②R元素位于元素周期表中第ⅡA族
③R元素的最高正化合价为+2价
④R元素的第一电离能高于同周期相邻元素的第一电离能
(1)①写出小苏打的化学式
②写出Fe2+的价电子排布式
(2)实验室用软锰矿和浓盐酸制氯气,写出该反应的化学方程式
(3)在常温下,0.1mol/LCH3COONa溶液的pH=9,则溶液中由水电离出来的c(OH-)=
(4)火箭发射可以用肼(N2H4,液态)作燃料,NO2作氧化剂,两者反应生成N2和水蒸气。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+66.4kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol
请写出N2H4(l)与NO2反应的热化学方程式
(5)下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示)。
| 元素 | 电离能/(kJ·mol-1) | |||||
| I1 | I2 | I3 | I4 | I5 | …… | |
| R | 740 | 1500 | 7700 | 10500 | 13630 | …… |
①R元素基态原子的电子排布式为1s22s2
②R元素位于元素周期表中第ⅡA族
③R元素的最高正化合价为+2价
④R元素的第一电离能高于同周期相邻元素的第一电离能
您最近一年使用:0次
5 . 回答下列问题:
(1)下列原子或离子的电子排布式或轨道表示式正确的是___________ (填序号)
①K+:
②Fe2+: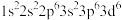
③P:
④O: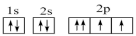
⑤Cu: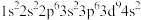
(2)基态原子的核外电子填充在6个轨道中的元素有___________ 种;
(3)C、N、O第一电离能从大到小的顺序为:___________ ;
(4)已知电负性H2.1、Si1.8,则SiH4中Si元素的化合价为___________ 。
(5)第四周期元素中,未成对电子数最多的元素是:___________ (写元素符号)。
(1)下列原子或离子的电子排布式或轨道表示式正确的是
①K+:

②Fe2+:
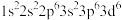
③P:

④O:
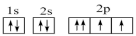
⑤Cu:
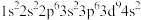
(2)基态原子的核外电子填充在6个轨道中的元素有
(3)C、N、O第一电离能从大到小的顺序为:
(4)已知电负性H2.1、Si1.8,则SiH4中Si元素的化合价为
(5)第四周期元素中,未成对电子数最多的元素是:
您最近一年使用:0次
6 . 按要求完成以下填空
(1)写出基态Cu2+的核外电子排布式:___________ 。
(2)丙烯中碳原子的杂化方式为:___________ 。
(3)已知铁的电离能数据如下:
则,铁的第四电离能( )大于第三电离能(
)大于第三电离能( )的可能原因是:
)的可能原因是:___________ 。
(4)两种三角锥形气态氢化物:膦(PH3)和氨(NH3)的键角分别为 93.6o和 107o ,分析PH3的键角小于NH3的原因:___________ 。
(1)写出基态Cu2+的核外电子排布式:
(2)丙烯中碳原子的杂化方式为:
(3)已知铁的电离能数据如下:
电离能/( ) ) |  |  |  |  | …… |
| Fe | 759 | 1561 | 2597 | 5290 | …… |
 )大于第三电离能(
)大于第三电离能( )的可能原因是:
)的可能原因是:(4)两种三角锥形气态氢化物:膦(PH3)和氨(NH3)的键角分别为 93.6o和 107o ,分析PH3的键角小于NH3的原因:
您最近一年使用:0次
7 . 回答下列问题。
(1)自然界中存在的碘的稳定性核素是碘-127(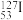 )。日本福岛第一核电站事故释放出的放射性物质中,含有人工放射性核素碘-131(
)。日本福岛第一核电站事故释放出的放射性物质中,含有人工放射性核素碘-131(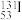 )。碘-131一旦被人体吸入,就可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是___________(填字母)。
)。碘-131一旦被人体吸入,就可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是___________(填字母)。
(2)核电站为防止发生核辐射事故,通常用含有铅的水泥做成屏蔽罩,内衬钢板,反应的压力容器用铁、铜、锰等具有反辐射合金材料制成。
①水泥中通常含有碳、氧、硅、铝等元素,则四种元素中3p能级上存在电子的是___________ (填元素符号)。
②写出二价铜离子的基态电子排布式:___________ 。
③铅的核电荷数为82,在周期表中___________ (填能级符号)区。
④基态锰原子价电子轨道表示式为___________ ,锰原子中能量最低的电子为___________ 轨道上的电子,其轨道呈___________ 形。
(1)自然界中存在的碘的稳定性核素是碘-127(
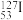 )。日本福岛第一核电站事故释放出的放射性物质中,含有人工放射性核素碘-131(
)。日本福岛第一核电站事故释放出的放射性物质中,含有人工放射性核素碘-131(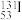 )。碘-131一旦被人体吸入,就可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是___________(填字母)。
)。碘-131一旦被人体吸入,就可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是___________(填字母)。A.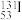 和 和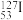 的价电子排布不相同 的价电子排布不相同 |
B.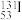 和 和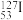 的电负性不相等 的电负性不相等 |
C.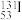 的基态电子排布式中只有1个能级未充满电子 的基态电子排布式中只有1个能级未充满电子 |
| D.碘元素的第一电离能大于氯元素 |
①水泥中通常含有碳、氧、硅、铝等元素,则四种元素中3p能级上存在电子的是
②写出二价铜离子的基态电子排布式:
③铅的核电荷数为82,在周期表中
④基态锰原子价电子轨道表示式为
您最近一年使用:0次
2024-03-12更新
|
60次组卷
|
2卷引用:黑龙江省绥化市绥棱县第一中学2023-2024学年高二上学期12月月考化学试题
8 . 硼及其化合物在制造、化工等领域都有广泛应用,回答下列问题:
(1)基态硼原子的价电子排布图为__________ ,其占据最高能级电子的电子云轮廓图形状为__________ ,基态硼原子比基态氮原子的第一电离能 小,其原因为
小,其原因为__________ 。
(2) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得:
反应制得:
① 由
由 和
和 构成,
构成, 的空间结构为
的空间结构为__________ 。
② 中B原子的杂化轨道类型为
中B原子的杂化轨道类型为__________ 。
③ 的键角为
的键角为__________ 。
(3)写出B与 溶液反应的离子方程式:
溶液反应的离子方程式:__________ 。
(4) 为一元弱酸[常温下,
为一元弱酸[常温下,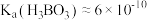 ]:
]:
① 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为__________ 。
②常温下, 的硼酸的pH约为
的硼酸的pH约为__________ (已知: ,
, )。
)。
(1)基态硼原子的价电子排布图为
 小,其原因为
小,其原因为(2)
 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得:
反应制得:①
 由
由 和
和 构成,
构成, 的空间结构为
的空间结构为②
 中B原子的杂化轨道类型为
中B原子的杂化轨道类型为③
 的键角为
的键角为(3)写出B与
 溶液反应的离子方程式:
溶液反应的离子方程式:(4)
 为一元弱酸[常温下,
为一元弱酸[常温下,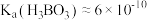 ]:
]:①
 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为②常温下,
 的硼酸的pH约为
的硼酸的pH约为 ,
, )。
)。
您最近一年使用:0次
2024-03-07更新
|
128次组卷
|
2卷引用:河北省邢台市四校联盟2023-2024学年高二上学期11月月考化学试题
9 . 深入研究物质的微观结构,有利于理解物质变化的本质。请回答下列问题:
(1)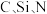 的电负性由大到小的顺序是
的电负性由大到小的顺序是___________ 。
(2)C、N、O、F的第一电离能由大到小的顺序是___________ 。
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为 或
或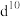 排布时,无颜色;为
排布时,无颜色;为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,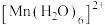
_________ 颜色(填“无”或“有”)。
(4)L的原子核外电子占有9个轨道,而且有一个未成对电子,L是___________ (填元素符号)。
(5) 能与
能与 形成正四面体形的配合物
形成正四面体形的配合物 ,
,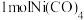 中含有
中含有__________  键。
键。
(1)
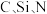 的电负性由大到小的顺序是
的电负性由大到小的顺序是(2)C、N、O、F的第一电离能由大到小的顺序是
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为
 或
或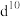 排布时,无颜色;为
排布时,无颜色;为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,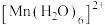
(4)L的原子核外电子占有9个轨道,而且有一个未成对电子,L是
(5)
 能与
能与 形成正四面体形的配合物
形成正四面体形的配合物 ,
,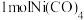 中含有
中含有 键。
键。
您最近一年使用:0次
10 . 根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1) 元素基态原子次外层电子数是最外层电子数的
元素基态原子次外层电子数是最外层电子数的 ,其价电子轨道表示式是
,其价电子轨道表示式是___________ 。
(2)Y是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是___________ ,在元素周期表中的位置是___________ 。
(3)Z元素基态原子的轨道表示式是图中的___________ (填写序号),

另一轨道表示式不能作为基态原子的轨道表示式是因为它不符合___________ 。
a.能量最低原理 b.泡利不相容原理 c.洪特规则
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能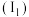 。如图所示:
。如图所示:

①同周期内,随着原子序数的增大, 值变化的总趋势是
值变化的总趋势是___________ 。
②根据第一电离能的含义和元素周期律,可推断出
___________  。
。
(1)
 元素基态原子次外层电子数是最外层电子数的
元素基态原子次外层电子数是最外层电子数的 ,其价电子轨道表示式是
,其价电子轨道表示式是(2)Y是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是
(3)Z元素基态原子的轨道表示式是图中的

另一轨道表示式不能作为基态原子的轨道表示式是因为它不符合
a.能量最低原理 b.泡利不相容原理 c.洪特规则
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能
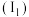 。如图所示:
。如图所示:
①同周期内,随着原子序数的增大,
 值变化的总趋势是
值变化的总趋势是②根据第一电离能的含义和元素周期律,可推断出

 。
。
您最近一年使用:0次



