23-24高二上·全国·课前预习
名校
1 . 现有四种元素的基态原子的电子排布式:①1s22s22p63s23p2 ②1s22s22p63s23p3③1s22s22p3 ④1s22s22p4。则下列有关比较正确的是
| A.原子半径:③>②>① | B.电负性:④>③>②>① |
| C.第一电离能:④>③>②>① | D.最高正化合价:④>③>②>① |
您最近一年使用:0次
2023-08-16更新
|
334次组卷
|
5卷引用:选择题1-5
23-24高三上·云南昆明·阶段练习
名校
2 . ZnS荧光材料的研究从1868年法国化学家Sidot发现至今已有近150年的历史。其中立方ZnS的晶胞如图所示,其晶胞参数为 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是
| A.电负性:Zn>S |
| B.S元素在元素周期表中位于s区 |
C.基态Zn原子的价层电子排布式为 |
D.立方ZnS晶体密度为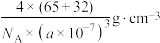 |
您最近一年使用:0次
17-18高一下·重庆·期中
名校
解题方法
3 . 已知:元素的电负性和元素的化合价一样,也是元素的一种基本性质;两成键元素间电负性差值大于1.7时,通常形成离子键,两成键元素间电负性差值小于1.7时,通常形成共价键。下表给出了14种元素的电负性,则下列说法错误的是
| 元素 | Al | B | Be | C | Cl | F | Li |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 |
| 元素 | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
| A.随着原子序数递增,元素的电负性呈周期性变化 |
| B.元素电负性越大,其非金属性越强 |
| C.根据电负性数据可知Mg3N2中含有离子键 |
| D.BeCl2含金属元素铍,故属于离子化合物 |
您最近一年使用:0次
2023-07-29更新
|
99次组卷
|
6卷引用:第38练 原子结构与元素的性质-2023年高考化学一轮复习小题多维练(全国通用)
(已下线)第38练 原子结构与元素的性质-2023年高考化学一轮复习小题多维练(全国通用)【全国百强校】重庆市第一中学2017-2018学年高一下学期期中考试化学试题江西省赣州市石城县石城中学2020-2021学年高一下学期3月月考化学试题第一章 本章复习提升1云南省龙陵县第一中学2022-2023学年高二下学期期末考试化学试题陕西省西安交通大学附属中学2023-2024学年高二上学期期中考试化学试题
22-23高三下·辽宁大连·阶段练习
名校
4 . 离子液体是室温下呈液态的离子化合物。由原子序数依次增大的短周期主族元素X、Y、Z、W、R组成的一种离子液体的结构如图所示,W的简单氢化物易液化,可用作制冷剂,R的简单阴离子含10个电子。下列说法正确的是
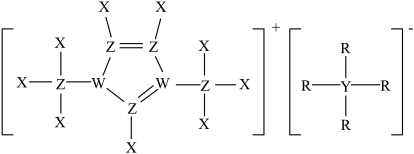
| A.简单氢化物的沸点:R>W | B.电负性:Z>Y>X |
| C.分子YR3的空间构型为三角锥形 | D.含氧酸的酸性:W>Z |
您最近一年使用:0次
名校
5 . 碳、硫、氧、氮是中学常见元素,下列说法不正确的是
A. 、 、 、 、 都是直线形分子 都是直线形分子 |
B. 、 、 、 、 的键角依次减小 的键角依次减小 |
C. 、 、 分子的中心原子都是 分子的中心原子都是 化 化 |
| D.C、N、F元素的电负性依次增大 |
您最近一年使用:0次
2023-06-08更新
|
145次组卷
|
5卷引用:广东省东莞市东华高级中学2021-2022 学年高二下学期专题测试化学试题
2023·河北邢台·三模
名校
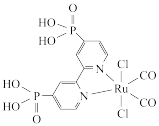
6 . 近年来,光催化剂的研究是材料领域的热点。一种Ru配合物(如图所示)复合光催化剂可将 转化为HCOOH。下列说法
转化为HCOOH。下列说法错误 的是
 转化为HCOOH。下列说法
转化为HCOOH。下列说法
| A.Ru配合物中第二周期元素的电负性:O>N>C |
B.吡啶(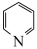 ,原子在同一平面)中C、N原子的杂化方式分别为 ,原子在同一平面)中C、N原子的杂化方式分别为 、 、 |
| C.该配合物中Ru的配位数是6 |
D. 中P的价层电子对数为4,空间结构为正四面体形 中P的价层电子对数为4,空间结构为正四面体形 |
您最近一年使用:0次
2023·江苏扬州·三模
名校
解题方法
7 . 软钾镁矾(化学式为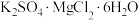 )是一种重要的钾肥。下列说法正确的是
)是一种重要的钾肥。下列说法正确的是
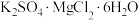 )是一种重要的钾肥。下列说法正确的是
)是一种重要的钾肥。下列说法正确的是A.半径大小: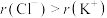 | B.电负性大小: |
C.电离能大小: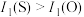 | D.碱性强弱: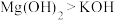 |
您最近一年使用:0次
2023-06-02更新
|
886次组卷
|
5卷引用:专题突破卷06 物质结构与性质?-2024年高考化学一轮复习考点通关卷(新教材新高考)
(已下线)专题突破卷06 物质结构与性质?-2024年高考化学一轮复习考点通关卷(新教材新高考)(已下线)考点巩固卷06 物质结构与性质(4大考点55题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)选择题1-5江苏省扬州市2023届高三下学期三模化学试题江苏省东台市安丰中学等六校2024届高三下学期4月联考模拟化学试题
2023·江苏徐州·三模
解题方法
8 . 向海水中加入石灰乳可得到氢氧化镁沉淀,进而提取镁。下列说法正确的是
A.离子半径大小: | B.电离能大小: |
| C.电负性大小:χ(H)>χ(Cl) | D.金属性强弱:Na>Mg>Ca |
您最近一年使用:0次
2023·天津和平·三模
9 . 下列说法不正确 的是
| A.Cu在周期中的ds区 |
| B.第一电离能:S<P<Cl |
| C.电负性:Na<H<B<C |
| D.杂化轨道可用于形成共价键 |
您最近一年使用:0次
22-23高二下·黑龙江哈尔滨·期中
名校
解题方法
10 . 解释下列现象的原因不正确的是
| 选项 | 现象 | 原因 |
| A |  中含有共价键 中含有共价键 | Al与Cl元素间的电负性差值小于1.7 |
| B | 碘在 中的溶解度比在水中大 中的溶解度比在水中大 | 碘和 均为非极性分子,水是极性分子 均为非极性分子,水是极性分子 |
| C | 对羟基苯甲醛的熔沸点比邻羟基苯甲醛的高 | 对羟基苯甲醛形成分子间氢键,而邻羟基苯甲醛形成分子内氢键 |
| D | HF的稳定性强于HCl | HF分子之间除了范德华力以外还存在氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



