真题
解题方法
1 . 三氯甲硅烷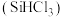 是制取高纯硅的重要原料,常温下为无色液体,沸点为
是制取高纯硅的重要原料,常温下为无色液体,沸点为 ,熔点为
,熔点为 ,易水解。实验室根据反应
,易水解。实验室根据反应 ,利用如下装置制备
,利用如下装置制备 粗品(加热及夹持装置略)。回答下列问题:
粗品(加热及夹持装置略)。回答下列问题:
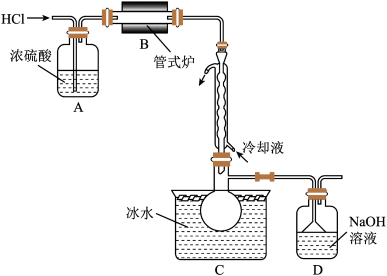
(1)制备 时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入
时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入 ,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为
,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为_____ ;判断制备反应结束的实验现象是_____ 。图示装置存在的两处缺陷是_____ 。
(2)已知电负性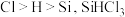 在浓
在浓 溶液中发生反应的化学方程式为
溶液中发生反应的化学方程式为_____ 。
(3)采用如下方法测定溶有少量 的
的 纯度。
纯度。
 样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①
样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①_____ ,②_____ (填操作名称),③称量等操作,测得所得固体氧化物质量为 ,从下列仪器中选出①、②中需使用的仪器,依次为
,从下列仪器中选出①、②中需使用的仪器,依次为_____ (填标号)。测得样品纯度为_____ (用含 、
、 的代数式表示)。
的代数式表示)。

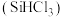 是制取高纯硅的重要原料,常温下为无色液体,沸点为
是制取高纯硅的重要原料,常温下为无色液体,沸点为 ,熔点为
,熔点为 ,易水解。实验室根据反应
,易水解。实验室根据反应 ,利用如下装置制备
,利用如下装置制备 粗品(加热及夹持装置略)。回答下列问题:
粗品(加热及夹持装置略)。回答下列问题:
(1)制备
 时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入
时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入 ,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为
,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为(2)已知电负性
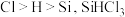 在浓
在浓 溶液中发生反应的化学方程式为
溶液中发生反应的化学方程式为(3)采用如下方法测定溶有少量
 的
的 纯度。
纯度。 样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①
样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:① ,从下列仪器中选出①、②中需使用的仪器,依次为
,从下列仪器中选出①、②中需使用的仪器,依次为 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2023-06-19更新
|
10715次组卷
|
16卷引用:2024届河北省实验中学高三年级上学期第一次月考化学试题
2024届河北省实验中学高三年级上学期第一次月考化学试题2023年高考山东卷化学真题(已下线)2023年高考山东卷化学真题变式题(实验综合题)(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点12 硅及其无机非金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第10讲 硅及其化合物(已下线)T26-工业流程题(已下线)专题15 化学实验综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点13 硅及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点46 定量分析实验(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)题型17 化学实验综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
2 . 化合物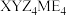 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E在地壳中含量最多。下列说法正确的是
,X与M同周期,E在地壳中含量最多。下列说法正确的是
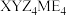 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E在地壳中含量最多。下列说法正确的是
,X与M同周期,E在地壳中含量最多。下列说法正确的是A.元素电负性: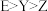 | B.氢化物沸点: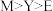 |
C.第一电离能: | D.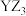 和 和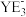 的空间结构均为三角锥形 的空间结构均为三角锥形 |
您最近一年使用:0次
2023-07-04更新
|
8036次组卷
|
15卷引用:河北省石家庄二中教育集团2023-2024学年高二年级上学期期末考试化学试题
河北省石家庄二中教育集团2023-2024学年高二年级上学期期末考试化学试题2023年高考广东卷化学真题(已下线)2023年广东卷高考真题变式题(选择题11-16)(已下线)第19讲元素周期律与元素周期表江西省宜春市宜丰中学2023-2024学年高三上学期开学考试化学试题(已下线)考点18 元素周期律与元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)广东省江门市第一中学2023-2024学年高二上学期第一次段考化学试题(已下线)选择题1-5陕西师范大学附属中学2023-2024学年高二上学期期中考试化学试题(已下线)题型20 物质结构与性质基础-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)重庆市第七中学校2023-2024学年高三上学期月考(12月)化学试题安徽省合肥市第七中学2023-2024学年高二下学期第一次段考化学试卷 四川省南充市阆中中学校2023-2024学年高二下学期3月月考化学试卷福建省南安市侨光中学2023-2024学年高二下学期4月月考化学试题甘肃省白银市靖远县第四中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
3 . 硒化锌是一种重要的半导体材料;其晶胞结构如图甲所示,已知晶胞参数为pnm,乙图为晶胞的俯视图,下列说法正确的是
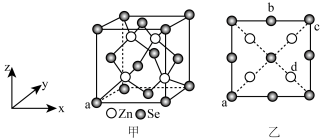
| A.晶胞中硒原子的配位数为12 |
B.晶胞中d点原子分数坐标为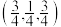 |
C.相邻两个Zn原子的最短距离为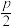 nm nm |
| D.电负性:Zn>Se |
您最近一年使用:0次
2023-03-03更新
|
1854次组卷
|
10卷引用:河北省张家口市宣化第一中学2023届高三模拟试题(三)化学试题
河北省张家口市宣化第一中学2023届高三模拟试题(三)化学试题山东省济宁市2023届高三一模考试(3月)化学试题山东省德州市第一中学2022-2023学年高二下学期3月月考化学试题(已下线)湖北省七市(州)2023届高三3月联合统一调研测试化学试题变式题(选择题11-15)河南省郑州市六校联盟2022-2023学年高二下学期4月期中考试化学试题(已下线)专题十 晶胞示意图(练)福建省龙岩市连城县第一中学2022-2023学年高二下学期5月月考化学试题河南省驻马店市环际大联考2022-2023学年高二下学期4月期中考试化学试题(已下线)热点08 金属晶体和离子晶体山东省烟台市第一中学2023-2024学年高三下学期3月月考化学试题
22-23高三上·北京石景山·期末
4 . 下列事实的解释不正确 的是
| 事实 | 解释 | |
| A | 气态 再失去一个电子比气态 再失去一个电子比气态 再失去一个电子更难 再失去一个电子更难 |  的价层电子排布为 的价层电子排布为 , , 轨道为半充满比较稳定; 轨道为半充满比较稳定; 的价层电子排布为 的价层电子排布为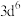 ,再失去一个电子可达到 ,再失去一个电子可达到 轨道半充满的比较稳定状态 轨道半充满的比较稳定状态 |
| B |  中H-O-H键角比 中H-O-H键角比 中的大 中的大 |  的中心原子的孤电子对数为1, 的中心原子的孤电子对数为1, 的中心原子的孤电子对数为2,孤电子对之间的斥力<孤电子对与成键电子对之间的斥力<成键电子对之间的斥力 的中心原子的孤电子对数为2,孤电子对之间的斥力<孤电子对与成键电子对之间的斥力<成键电子对之间的斥力 |
| C | 晶体熔点: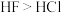 |  分子间能形成氢键 分子间能形成氢键 |
| D | 酸性: | 氟的电负性大于氯的电负性, 的极性大于 的极性大于 的极性,使 的极性,使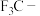 的极性大于 的极性大于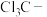 的极性,导致 的极性,导致 的羧基中的羟基的极性更大,更易电离出 的羧基中的羟基的极性更大,更易电离出 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-05更新
|
1438次组卷
|
10卷引用:选择题6-10
(已下线)选择题6-10北京市石景山区2022-2023学年高三上学期期末考试化学试题黑龙江省富锦市第一中学2022-2023学年高二下学期第一次考试化学试题北京师范大学附属实验中学2022-2023学年高二下学期3月月考化学试题广东省揭阳市惠来县第一中学2022-2023学年高二下学期第一次月考化学试题山西省孝义市2022-2023学年高二4月月考化学试卷广东省东莞市东华高级中学2022-2023学年高二下学期3月月考化学试题广东省深圳外国语学校2022-2023学年高二下学期3月月考化学试题北京市第一七一中学2023-2024学年高三上学期10月考化学试题湖北省武昌实验中学2023-2024学年高三上学期12月月考化学试题
名校
解题方法
5 . 某锂盐的结构如图所示,其阴离子是由原子序数依次增大的短周期主族元素X、Y,Z、W形成,X,Y与Z同一周期,Y与W同族。下列说法正确的是( )
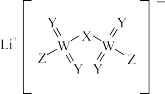
A.元素的电负性: | B.第一电离能: |
C.简单气态氢化物的热稳定性: | D.简单离子的半径: |
您最近一年使用:0次
2022-05-05更新
|
2589次组卷
|
16卷引用:河北省沧州市泊头市第一中学2023-2024学年高二上学期12月月考化学试题
河北省沧州市泊头市第一中学2023-2024学年高二上学期12月月考化学试题山东省济南市2022届高三第二次模拟化学试题安徽省怀宁中学2021-2022学年高二下学期5月阶段考试化学试题山东省济南第一中学2023届高三上学期开学考试化学试题辽宁省沈阳市第十中学2022-2023学年高二上学期期末综合测评化学试题新疆乌鲁木齐市第八中学2022-2023学年高二上学期期末考试化学试题贵州省江口中学2022-2023学年高二下学期3月份月考化学试题第一章 原子结构与性质(B卷·能力提升练)-2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修2)云南省楚雄彝族自治州民族中学2022-2023学年高二下学期5月月考化学试题(已下线)2023年湖南卷高考真题变式题(选择题6-10)(已下线)选择题1-5湖南省邵阳市武冈市2023-2024学年高三上学期期中考试化学试题河南省驻马店市确山县第一高级中学2023~2024学年高二上学期第二次月考化学试题黑龙江省大兴安岭实验中学2023-2024学年高二下学期开学考试化学试卷宁夏石嘴山市第三中学2023-2024学年高二下学期3月月考化学试题山东省临沂市平邑县第一中学西校区2023-2024学年高二上学期1月份阶段性考试化学试题
6 . X、Y、Z、Q、W是原子序数依次增大的前四周期元素,X、Z的基态原子2p能级上各有两个未成对电子,Y与Q同主族,W原子N能层只有一个电子,其余能层全充满。下列说法错误的是

| A.电负性为Z>Y>X |
| B.原子半径为r(Q)>r(Y)>r(Z) |
| C.X与Z可以形成含极性键的非极性分子 |
| D.W与Z形成的化合物晶胞如图,其化学式为WZ |
您最近一年使用:0次
2023-04-11更新
|
802次组卷
|
3卷引用:河北省保定市2023届一模考试化学试题
名校
7 . 部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图所示,下列说法正确的是


| A.离子半径的大小顺序:e>f>g>h | B.与x形成简单化合物的沸点:y>z>d |
| C.y、z、d三种元素第一电离能和电负性的大小顺序不一致 | D.e、f、g、h四种元素对应最高价氧化物的水化物相互之间均能发生反应 |
您最近一年使用:0次
2021-01-09更新
|
2094次组卷
|
8卷引用:河北省沧州市东光县等3地河北省盐山中学等2校2022-2023学年高二下学期3月月考化学试题
名校
解题方法
8 . X、Y、Z、M是电负性逐渐减小的短周期非金属元素。X、Z、M位于三个不同周期,Y与Z的价电子数目之和为M价电子数的两倍;化合物 的电子总数为18个。下列说法错误的是
的电子总数为18个。下列说法错误的是
 的电子总数为18个。下列说法错误的是
的电子总数为18个。下列说法错误的是| A.原子半径:Z<X<Y<M | B.简单氢化物的稳定性:X>Y>M |
| C.Z与M形成的化合物具有较强的还原性 | D.Y的含氧酸为弱酸 |
您最近一年使用:0次
2023-04-10更新
|
741次组卷
|
5卷引用:河北省石家庄市部分学校2023届高中毕业年级教学质量检测(二)(一模)化学试题
河北省石家庄市部分学校2023届高中毕业年级教学质量检测(二)(一模)化学试题(已下线)专题06 物质结构与性质江西省吉安市吉州区部分学校联考2022-2023学年高二下学期期末考试化学试题(已下线)2019年高考江苏卷化学试题变式题(单选题6-10)江苏省江阴市华士高级中学2023-2024学年高二上学期10月学情调研化学(选修)试题
名校
9 . 三苯胺及其衍生物可用于新型电致发光材料、特种染料和医药的合成,一种三苯胺单醛的修饰路线如图所示,下列说法错误的是

| A.电负性:H<C<O | B.甲中所有碳原子一定在同一平面 |
| C.乙的核磁共振氢谱有7组峰 | D.该反应发生了 键的断裂 键的断裂 |
您最近一年使用:0次
名校
10 . 卤素钙钛矿已经被广泛应用于太阳能电池、发光二极体等领域,其中合成二维/三维(2D/3D)的钙钛矿异质结是提升器件稳定性和转换效率的一个策略,近期化学工作者在气相合成的单晶三维钙钛矿CsPbBr3上合成外延生长的水平和垂直的二维钙钛矿(PEA)2PbBr4(PEA+代表 )异质结。回答下列问题:
)异质结。回答下列问题:
(1)基态Br原子的价电子排布式为___ 。
(2)PEA+中N的价层电子对数为___ ,杂化轨道类型为___ ,PEA+中涉及元素的电负性由大到小的顺序为___ ,1molPEA+中存在___ molσ键。
(3)已知铅卤化合物中存在正四面体构型的[PbCl4]2-、[PbBr4]2-、[PbI4]2-,三者中半径最小的配体为___ 。已知[Pb2I6]2-中每个Pb均采用四配位模式,则[Pb2I6]2-的结构式为___ 。
(4)Br2和碱金属单质形成的MBr熔点如表:
等量NaBr、KBr、RbBr、CsBr同时开始加热优先导电的是____ (填化学式),熔点呈现表中趋势的原因是____ 。
(5)已知三维立方钙钛矿CsPbBr3中三种离子在晶胞(a)中占据正方体顶点、面心、体心位置,图(b)显示的是三种离子在xz面、yz面、xy面上的位置:

若晶胞边长为apm,阿伏加德罗常数的值为NA,晶体的密度为___ g·cm-3 (写出表达式)。
②上述晶胞沿体对角线方向的投影图为___ (填标号)。
A. B.
B. C.
C. D.
D.
 )异质结。回答下列问题:
)异质结。回答下列问题:(1)基态Br原子的价电子排布式为
(2)PEA+中N的价层电子对数为
(3)已知铅卤化合物中存在正四面体构型的[PbCl4]2-、[PbBr4]2-、[PbI4]2-,三者中半径最小的配体为
(4)Br2和碱金属单质形成的MBr熔点如表:
| MBr | NaBr | KBr | RbBr | CsBr |
| 熔点/℃ | 747 | 734 | 693 | 636 |
等量NaBr、KBr、RbBr、CsBr同时开始加热优先导电的是
(5)已知三维立方钙钛矿CsPbBr3中三种离子在晶胞(a)中占据正方体顶点、面心、体心位置,图(b)显示的是三种离子在xz面、yz面、xy面上的位置:

若晶胞边长为apm,阿伏加德罗常数的值为NA,晶体的密度为
②上述晶胞沿体对角线方向的投影图为
A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
2021-09-10更新
|
1506次组卷
|
4卷引用:河北省省级联测2021-2022学年高三上学期第一次考试化学试题
河北省省级联测2021-2022学年高三上学期第一次考试化学试题(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-讲义四川省遂宁市射洪中学校2021-2022学年高二下学期期中考试化学试题第三章 晶体结构与性质(B卷·能力提升练)-2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修2)



