1 . 砷化镓( )是一种性能优良的半导体材料,工业上可通过如下的两个反应制取:
)是一种性能优良的半导体材料,工业上可通过如下的两个反应制取: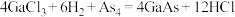 或
或 。
。
(1)基态砷原子的价层电子排布图为_______。氯元素的下列几种微粒中,若再失去一个电子,需要的能量最多的是_______(填标号)。
(2) 的中心原子轨道杂化类型为
的中心原子轨道杂化类型为_______ , 中的三个碳原子和中心原子镓原子构成的空间构型是
中的三个碳原子和中心原子镓原子构成的空间构型是_______ ,写出一种与甲烷互为等电子体的离子的化学式:_______ 。
(3)上述反应涉及的几种元素中,电负性最大的元素是_______ ,砷可形成多种卤化物,其中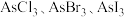 的沸点由低到高的原因为
的沸点由低到高的原因为_______ 。
(4) 晶胞图及部分原子的分数坐标如下:
晶胞图及部分原子的分数坐标如下:
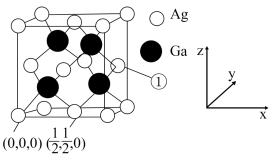
则①处原子的分数坐标为_______ ,已知紧邻的 原子之间的距离为
原子之间的距离为 ,紧邻的
,紧邻的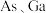 原子之间的距离为
原子之间的距离为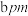 ,则
,则
_______ b,该晶胞的密度为_______  (用含a、阿伏加德罗常数
(用含a、阿伏加德罗常数 的式子表示)。
的式子表示)。
 )是一种性能优良的半导体材料,工业上可通过如下的两个反应制取:
)是一种性能优良的半导体材料,工业上可通过如下的两个反应制取: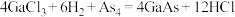 或
或 。
。(1)基态砷原子的价层电子排布图为_______。氯元素的下列几种微粒中,若再失去一个电子,需要的能量最多的是_______(填标号)。
A.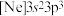 | B. | C.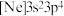 | D.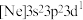 |
 的中心原子轨道杂化类型为
的中心原子轨道杂化类型为 中的三个碳原子和中心原子镓原子构成的空间构型是
中的三个碳原子和中心原子镓原子构成的空间构型是(3)上述反应涉及的几种元素中,电负性最大的元素是
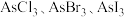 的沸点由低到高的原因为
的沸点由低到高的原因为(4)
 晶胞图及部分原子的分数坐标如下:
晶胞图及部分原子的分数坐标如下:
则①处原子的分数坐标为
 原子之间的距离为
原子之间的距离为 ,紧邻的
,紧邻的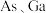 原子之间的距离为
原子之间的距离为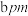 ,则
,则
 (用含a、阿伏加德罗常数
(用含a、阿伏加德罗常数 的式子表示)。
的式子表示)。
您最近一年使用:0次
解题方法
2 . 有A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。A、B、C、D、E五种元素的电负性分别为2.1,3.5,1.5,2.5,0.8,请回答下列问题:
(1)A是_______ ,B是_______ ,C是_______ ,D是_______ ,E是_______ (用化学符号填空,下同)。
(2)由电负性判断,以上五种元素中金属性最强的是_______ ,非金属性最强的是_______ 。
(3)当B与A、C、D分别形成化合物时,B显_______ 价(填“正”或“负”或“零”,下同),其他元素显_______ 价。
(4)当B与A、C、D、E(与E形成E2B)分别形成化合物时,化合物中有离子键的是_______ (填化学式)。
(1)A是
(2)由电负性判断,以上五种元素中金属性最强的是
(3)当B与A、C、D分别形成化合物时,B显
(4)当B与A、C、D、E(与E形成E2B)分别形成化合物时,化合物中有离子键的是
您最近一年使用:0次
3 . 某抗癌药物的结构简式如图所示,其中W、X、Y、Z是原子序数依次增大的短周期主族元素,W、Y同主族,Z的最外层电子数等于W的核外电子数。下列叙述正确的是
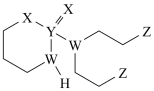

| A.W位于第二周期IIIA族 |
| B.基态Y原子只有1个未成对电子 |
| C.W、Z的最简单氢化物混合物的沸点,前者小于后者 |
| D.电负性:W>Y |
您最近一年使用:0次
2022-06-03更新
|
192次组卷
|
2卷引用:江西省丰城中学2023-2024学年高三上学期12月月考化学试题
名校
解题方法
4 . 金属钛有“生物金属、海洋金属、太空金属”的美称。有些含钛的化合物在耐高温、环保或者抑菌方面有着重要的应用,钛元素也被称为“健康钛”。
(1)Ti元素位于元素周期表的_______ 区,基态原子电子排布式为_______ 。
(2)TiCl4与SiCl4互为等电子体。SiCl4可以与N-甲基咪唑
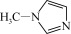
 发生反应。
发生反应。
①TiCl4分子的空间构型为_______ 。
②N-甲基咪唑分子中碳原子的杂化轨道类型为_______ ,C、N、Si的电负性由大到小的顺序为_______ ,1个 含有
含有_______ 个π键。
(3)TiCl4可以与胺形成配合物,如TiCl4(CH3NH2)2、TiCl4(H2NCH2CH2NH2)。
① TiCl4 (H2NCH2CH2NH2)中提供电子对形成配位键的原子是_______ 。
②乙二胺(H2NCH2CH2NH2)能与Mg2+、Cu2+等金属离子形成稳定环状离子,其中与乙二胺形成的化合物稳定性较差的是_______ (填“Mg2+”或“Cu2+”)。
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似(如图),其中阴离子(N3-)采用面心立方最密堆积方式,X-射线衍射实验测得氮化钛的晶胞参数(晶胞边长)为a pm,则r(N3-)为_______ pm。该氮化钛的密度为_______ g·cm-3(NA为阿伏加德罗常数的值,只列计算式)。

(1)Ti元素位于元素周期表的
(2)TiCl4与SiCl4互为等电子体。SiCl4可以与N-甲基咪唑


 发生反应。
发生反应。①TiCl4分子的空间构型为
②N-甲基咪唑分子中碳原子的杂化轨道类型为
 含有
含有(3)TiCl4可以与胺形成配合物,如TiCl4(CH3NH2)2、TiCl4(H2NCH2CH2NH2)。
① TiCl4 (H2NCH2CH2NH2)中提供电子对形成配位键的原子是
②乙二胺(H2NCH2CH2NH2)能与Mg2+、Cu2+等金属离子形成稳定环状离子,其中与乙二胺形成的化合物稳定性较差的是
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似(如图),其中阴离子(N3-)采用面心立方最密堆积方式,X-射线衍射实验测得氮化钛的晶胞参数(晶胞边长)为a pm,则r(N3-)为

您最近一年使用:0次
2021-11-18更新
|
909次组卷
|
7卷引用:江西省重点校2022-2023学年高三上学期第二次联考化学试题.
江西省重点校2022-2023学年高三上学期第二次联考化学试题.黑龙江省大庆市2022届高三上学期第一次教学质量检测化学试题(已下线)备战2022年高考化学精准检测卷【全国卷】17(已下线)一轮巩固卷8-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)宁夏吴忠市2022届高三4月模拟联考(二模)理科综合化学试题山东省威海乳山市银滩高级中学2021-2022学年高二12月月考化学试题黑龙江省大庆市2023-2024学年高三上学期第一次模拟考试化学试题
解题方法
5 . 锌及其化合物在工农业生产及科学研究中具有广泛的用途。回答下列问题:
(1)Zn位于元素周期表的___________ 区,基态Zn2+的核外电子排布式为___________ 。
(2)氨基酸锌是研究最早和使用最广泛的第三代锌添加剂,该添加剂具有优良的营养功能。如图1是氨基酸锌的结构简式。
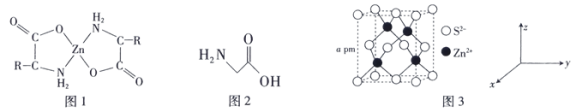
①组成氨基酸锌的C、N、O的电负性由大到小的顺序是___________ 。
②氨基酸锌的Zn2+形成配位键,其中提供空轨道的原子是___________ 。
③最简单的氨基酸是甘氨酸(结构简式如图2),其结构中π键与σ键的数量比为___________ 。
(3)ZnS可用于制白色颜料、玻璃、发光粉、橡胶、塑料、发光油漆等。ZnS的晶胞如图3所示。
①上图中 的坐标有
的坐标有 、
、 ,与
,与 距离最近的
距离最近的 还有
还有___________ (填坐标)。
②Zn2+占据___________ (填“八面体”或“四面体”)空隙,空隙利用率为___________ %。
③ZnS的密度为___________  。
。
(1)Zn位于元素周期表的
(2)氨基酸锌是研究最早和使用最广泛的第三代锌添加剂,该添加剂具有优良的营养功能。如图1是氨基酸锌的结构简式。

①组成氨基酸锌的C、N、O的电负性由大到小的顺序是
②氨基酸锌的Zn2+形成配位键,其中提供空轨道的原子是
③最简单的氨基酸是甘氨酸(结构简式如图2),其结构中π键与σ键的数量比为
(3)ZnS可用于制白色颜料、玻璃、发光粉、橡胶、塑料、发光油漆等。ZnS的晶胞如图3所示。
①上图中
 的坐标有
的坐标有 、
、 ,与
,与 距离最近的
距离最近的 还有
还有②Zn2+占据
③ZnS的密度为
 。
。
您最近一年使用:0次
2021-07-05更新
|
127次组卷
|
2卷引用:江西省赣抚吉名校2022届高三上学期8月联合考试化学试题
名校
解题方法
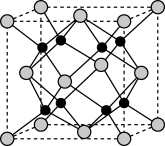
6 . 据媒体报道,法国一家公司Tiamat日前研发出比当前广泛使用的锂电池成本更低、寿命更长、充电速度更快的钠离子电池,预计从2020年开始实现工业生产。该电池的负极材料为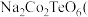 制备原料为
制备原料为 、
、 和
和 ,电解液为
,电解液为 的碳酸丙烯酯溶液。
的碳酸丙烯酯溶液。
回答下列问题:
(1)Te属于元素周期表中______ 区元素,其基态原子的价电子排布式为______ 。
(2)基态Na原子中,核外电子占据的原子轨道总数为______ 。
(3)结合题中信息判断:C、O、Cl的电负性由大到小的顺序为______  用元素符号表示
用元素符号表示 。
。
(4)碳酸丙烯酯的结构简式如下图所示,则其中碳原子的杂化轨道类型为______ ,1mol碳酸丙烯酯中σ键的数目为______ 。
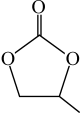
 的几何构型为正八面体形,配体是
的几何构型为正八面体形,配体是______ ,该配离子包含的作用力为______  填选项字母
填选项字母 。
。
A.离子键 B. 极性键 C. 配位键 D.氢键 E. 金属键
(6)Na和O形成的离子化合物的晶胞结构如下图所示,该晶胞的密度为ρg/ ,阿伏加 德罗常数的值为
,阿伏加 德罗常数的值为 ,则Na与O之间的最短距离为
,则Na与O之间的最短距离为_______________________ 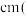 用含ρ、
用含ρ、 的代数式表示
的代数式表示 。
。
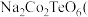 制备原料为
制备原料为 、
、 和
和 ,电解液为
,电解液为 的碳酸丙烯酯溶液。
的碳酸丙烯酯溶液。回答下列问题:
(1)Te属于元素周期表中
(2)基态Na原子中,核外电子占据的原子轨道总数为
(3)结合题中信息判断:C、O、Cl的电负性由大到小的顺序为
 用元素符号表示
用元素符号表示 。
。(4)碳酸丙烯酯的结构简式如下图所示,则其中碳原子的杂化轨道类型为

 的几何构型为正八面体形,配体是
的几何构型为正八面体形,配体是 填选项字母
填选项字母 。
。A.离子键 B. 极性键 C. 配位键 D.氢键 E. 金属键
(6)Na和O形成的离子化合物的晶胞结构如下图所示,该晶胞的密度为ρg/
 ,阿伏加 德罗常数的值为
,阿伏加 德罗常数的值为 ,则Na与O之间的最短距离为
,则Na与O之间的最短距离为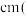 用含ρ、
用含ρ、 的代数式表示
的代数式表示 。
。
您最近一年使用:0次
名校
解题方法
7 . 图1是元素周期表的一部分,已知A、B、C、D、E、F、G都是周期表中的前四周期元素,它们在周期表中的位置如图1所示。
试回答下列问题:
(1)F元素基态原子的核外电子排布式为_________________ 。
(2)ABC的第一电离能由大到小的顺序______________ (用元素符号表示)。
(3)B元素单质分子中的_______ 个π键,与其互为等电子体的阴离子为____________________ 。
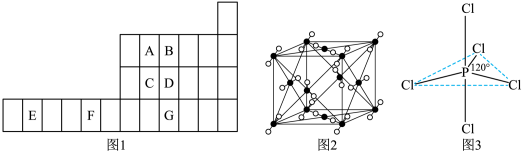
(4)图2为A元素某种氧化物的晶胞,其分子中心原子采用________ 杂化,每个分子周围有_____ 个分子与之距离相等且最近。若晶胞棱长为a pm,则该晶体密度的表达式为________ g·cm-3。
(5)G元素的氢化物分子的空间构型为________ ,其沸点与B元素的氢化物相比________ (填高或低),其原因是________ 。
(6)向CuSO4溶液中滴加入B 元素氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解,得到深蓝色透明溶液,请写出沉淀溶解的离子方程式________ 。
(7)知道B 的电负性大于氯,则B 与F2或Cl2形成的化合物水解,产物是否相同__________ ?(填“相同”或“不同”)。

试回答下列问题:
(1)F元素基态原子的核外电子排布式为
(2)ABC的第一电离能由大到小的顺序
(3)B元素单质分子中的
(4)图2为A元素某种氧化物的晶胞,其分子中心原子采用
(5)G元素的氢化物分子的空间构型为
(6)向CuSO4溶液中滴加入B 元素氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解,得到深蓝色透明溶液,请写出沉淀溶解的离子方程式
(7)知道B 的电负性大于氯,则B 与F2或Cl2形成的化合物水解,产物是否相同
您最近一年使用:0次



