解题方法
1 . 冠醚因分子结构形如皇冠而得名,基于18-冠-6(结构如图所示)的吸附剂可用于分离 (锶离子)。下列说法正确的是
(锶离子)。下列说法正确的是
 (锶离子)。下列说法正确的是
(锶离子)。下列说法正确的是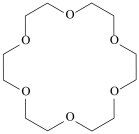
| A.电负性:O>C>Sr>H |
B.18-冠-6(空穴适配 )可增加KI在苯中的溶解度 )可增加KI在苯中的溶解度 |
| C.18-冠-6中C和O原子的杂化轨道类型不同 |
D.18-冠-6可与 形成超分子,该超分子中存在配位键、氢键等化学键 形成超分子,该超分子中存在配位键、氢键等化学键 |
您最近一年使用:0次
解题方法
2 . 某天然矿石的晶体由原子序数依次增大的三种前四周期元素X、Y、Z组成,该晶体结构如图所示。其中Y元素的一种氧化物具有磁性,Z元素只有一个4s电子。下列说法正确的是
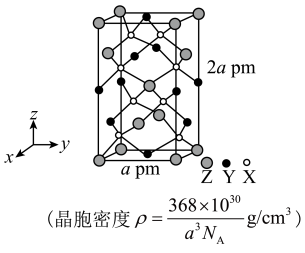
| A.Y、Z均位于元素周期表的ds区 |
| B.晶胞中各原子的配位数不相同 |
| C.该天然矿石的化学式ZYX₂ |
| D.电负性:Y>X |
您最近一年使用:0次
3 . X、Y、Z、W是原子序数依次增大的短周期主族元素,X原子有两个单电子且电负性是四种元素中最大的,Y原子的最外层电子数是X原子内层电子数的2倍,Z原子s能级上电子数与p能级上电子数之比为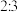 ,W第一电离能大于Z。下列说法正确的是
,W第一电离能大于Z。下列说法正确的是
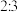 ,W第一电离能大于Z。下列说法正确的是
,W第一电离能大于Z。下列说法正确的是A.电负性: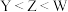 |
B.原子半径: |
C.四种元素基态原子的未成对电子数: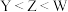 |
D.简单氢化物的键角: |
您最近一年使用:0次
4 . 阴离子 和二脲基分子能通过一种弱相互作用形成超分子阴离子配合物,如下图所示(图中省略阴离子配合物中部分原子)。下列关于该阴离子配合物的说法正确的是
和二脲基分子能通过一种弱相互作用形成超分子阴离子配合物,如下图所示(图中省略阴离子配合物中部分原子)。下列关于该阴离子配合物的说法正确的是
 和二脲基分子能通过一种弱相互作用形成超分子阴离子配合物,如下图所示(图中省略阴离子配合物中部分原子)。下列关于该阴离子配合物的说法正确的是
和二脲基分子能通过一种弱相互作用形成超分子阴离子配合物,如下图所示(图中省略阴离子配合物中部分原子)。下列关于该阴离子配合物的说法正确的是
A.二脲基分子中N-H的H和 离子的O形成氢键 离子的O形成氢键 |
| B.所含元素电负性、第一电离能最大的均是N |
| C.二脲基分子中C、N均只有一种杂化方式 |
| D.所含元素的基态原子未成对电子数为2的只有1种 |
您最近一年使用:0次
5 .  为原子序数依次增大的短周期元素,其中仅
为原子序数依次增大的短周期元素,其中仅 位于同一周期,X的s轨道电子数是p轨道电子数的2倍,
位于同一周期,X的s轨道电子数是p轨道电子数的2倍,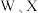 的最外层电子数之和等于Y的最外层电子数,基态Z原子有1个未成对电子。下列说法错误的是
的最外层电子数之和等于Y的最外层电子数,基态Z原子有1个未成对电子。下列说法错误的是
 为原子序数依次增大的短周期元素,其中仅
为原子序数依次增大的短周期元素,其中仅 位于同一周期,X的s轨道电子数是p轨道电子数的2倍,
位于同一周期,X的s轨道电子数是p轨道电子数的2倍,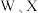 的最外层电子数之和等于Y的最外层电子数,基态Z原子有1个未成对电子。下列说法错误的是
的最外层电子数之和等于Y的最外层电子数,基态Z原子有1个未成对电子。下列说法错误的是A.电负性: |
| B.X与Z形成的化合物空间构型是三角锥形 |
| C.Y的第一电离能大于同周期相邻元素 |
| D.只有W元素处于s区 |
您最近一年使用:0次
6 . X、Y、Z、Q是原子序数依次增大的前四周期非稀有气体元素,且分别处于不同的周期。Y元素基态原子的价层电子排布是 ;Z、Q元素原子的最外层均只有1个电子,Z元素原子中只有两种形状的电子云,Q元素基态原子内层轨道均排满电子。下列说法正确的是
;Z、Q元素原子的最外层均只有1个电子,Z元素原子中只有两种形状的电子云,Q元素基态原子内层轨道均排满电子。下列说法正确的是
 ;Z、Q元素原子的最外层均只有1个电子,Z元素原子中只有两种形状的电子云,Q元素基态原子内层轨道均排满电子。下列说法正确的是
;Z、Q元素原子的最外层均只有1个电子,Z元素原子中只有两种形状的电子云,Q元素基态原子内层轨道均排满电子。下列说法正确的是| A.电负性:Y>X>Z>Q | B.ZX属于共价化合物 |
C. 的阴阳离子数之比为1∶1 的阴阳离子数之比为1∶1 | D.Q元素位于元素周期表的ds区 |
您最近一年使用:0次
名校
7 . 脱羧反应是有机化学中的重要反应,制备氰化物的脱羧反应如图所示。下列说法正确的是
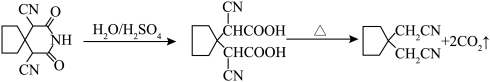
| A.电负性:S>O>N>C>H | B. 的空间填充模型为 的空间填充模型为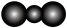 |
C.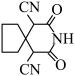 分子中有两个手性碳原子 分子中有两个手性碳原子 | D. 分子中C有2种杂化方式 分子中C有2种杂化方式 |
您最近一年使用:0次
8 . 已知X、Y、Z、W为原子序数依次递增的主族元素,只有Y、Z同周期,W元素原子的4p轨道上有3个未成对电子,Y元素原子的2p轨道上有2个未成对电子,W与Y可形成化合物 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是| A.电负性:X>Y>Z |
| B.原子半径:W>Z>Y |
C. 的VSEPR模型和空间结构一致 的VSEPR模型和空间结构一致 |
| D.W元素的第一电离能高于同周期相邻元素的 |
您最近一年使用:0次
9 .  是原子序数依次增大的短周期主族元素,其中
是原子序数依次增大的短周期主族元素,其中 原子的电子只有一种自旋取向,基态
原子的电子只有一种自旋取向,基态 原子的
原子的 轨道上有1个空轨道,
轨道上有1个空轨道, 的单质可通过分离液态空气制取,
的单质可通过分离液态空气制取, 是短周期中原子半径最大的主族元素。下列说法正确的是
是短周期中原子半径最大的主族元素。下列说法正确的是
 是原子序数依次增大的短周期主族元素,其中
是原子序数依次增大的短周期主族元素,其中 原子的电子只有一种自旋取向,基态
原子的电子只有一种自旋取向,基态 原子的
原子的 轨道上有1个空轨道,
轨道上有1个空轨道, 的单质可通过分离液态空气制取,
的单质可通过分离液态空气制取, 是短周期中原子半径最大的主族元素。下列说法正确的是
是短周期中原子半径最大的主族元素。下列说法正确的是A.原子半径: |
B.第一电离能: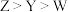 |
C.简单氢化物的沸点: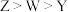 |
D. 与 与 形成的 形成的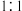 型化合物中不可能含有双键 型化合物中不可能含有双键 |
您最近一年使用:0次
10 . 下列关于物质结构与性质的叙述错误的是
A. 键的极性大于 键的极性大于 ,因此 ,因此 分子的极性大于 分子的极性大于 |
B. 的电负性大于 的电负性大于 ,因此 ,因此 的键角小于 的键角小于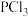 |
C. 键的键能大于 键的键能大于 ,因此 ,因此 的稳定性高于 的稳定性高于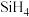 |
D.甲基是推电子基团,羟基是吸电子基团,因此 的碱性强于 的碱性强于 |
您最近一年使用:0次



