1 . 氰基丙烯酸乙酯是一种粘合剂的主要成分,其结构式如图1所示。 (过硫酸钾)是一种强氧化剂,其中
(过硫酸钾)是一种强氧化剂,其中 的结构式如图2所示。下列说法正确的是
的结构式如图2所示。下列说法正确的是
 (过硫酸钾)是一种强氧化剂,其中
(过硫酸钾)是一种强氧化剂,其中 的结构式如图2所示。下列说法正确的是
的结构式如图2所示。下列说法正确的是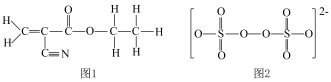
| A.1mol氰基丙烯酸乙酯分子中含3molπ键 |
B.氰基丙烯酸乙酯分子中 、 、 杂化的碳原子数之比为 杂化的碳原子数之比为 |
C. 中 中 元素的化合价为 元素的化合价为 价 价 |
D. 结构中“ 结构中“ ”的4个原子处于同一条直线 ”的4个原子处于同一条直线 |
您最近一年使用:0次
解题方法
2 . 下列说法中正确的是
| A.非极性分子中只含有非极性键 |
B.可燃冰( )中甲烷分子与水分子间存在氢键 )中甲烷分子与水分子间存在氢键 |
C.杂化轨道只用于形成 键或用于容纳未参与成键的孤电子对 键或用于容纳未参与成键的孤电子对 |
| D.基态原子变为激发态原子时要释放能量 |
您最近一年使用:0次
解题方法
3 . 氯及其化合物应用广泛。 易液化,可储存于钢瓶中。氯气可用于生产
易液化,可储存于钢瓶中。氯气可用于生产 、
、 、
、 、
、 等化工产品。
等化工产品。 和
和 的化学性质相似,能与
的化学性质相似,能与 反应生成两种酸。
反应生成两种酸。 (其中
(其中 为
为 价)可用于漂白和杀菌消毒,其水解可生成
价)可用于漂白和杀菌消毒,其水解可生成 和
和 。下列物质的结构与性质或物质的性质与用途具有对应关系的是
。下列物质的结构与性质或物质的性质与用途具有对应关系的是
 易液化,可储存于钢瓶中。氯气可用于生产
易液化,可储存于钢瓶中。氯气可用于生产 、
、 、
、 、
、 等化工产品。
等化工产品。 和
和 的化学性质相似,能与
的化学性质相似,能与 反应生成两种酸。
反应生成两种酸。 (其中
(其中 为
为 价)可用于漂白和杀菌消毒,其水解可生成
价)可用于漂白和杀菌消毒,其水解可生成 和
和 。下列物质的结构与性质或物质的性质与用途具有对应关系的是
。下列物质的结构与性质或物质的性质与用途具有对应关系的是A. 的键能大于 的键能大于 , , 的热稳定性大于 的热稳定性大于 |
B. 分子间存在氢键, 分子间存在氢键, 不易分解 不易分解 |
C. 具有弱酸性,可用于杀菌消毒 具有弱酸性,可用于杀菌消毒 |
D. 溶液呈棕黄色,可用于蚀刻铜制印刷电路板 溶液呈棕黄色,可用于蚀刻铜制印刷电路板 |
您最近一年使用:0次
4 . 下列说法正确的是
A.原子轨道的能量: | B.元素最高正化合价: |
C. 的键角: 的键角: | D. 中 中 键与 键与 键的数目比为 键的数目比为 |
您最近一年使用:0次
名校
5 . W、X、Y、Q、R为前四周期元素且原子序数依次增大。W的基态原子有3个不同能级,各能级中的电子数相等;Y原子核外电子有8种不同的运动状态,Q和 具有相同数目的未成对电子,
具有相同数目的未成对电子, 的价电子数是
的价电子数是 的二分之一,
的二分之一, 的核外电子充满三个电子层。请回答下列问题:
的核外电子充满三个电子层。请回答下列问题:
(1)基态X原子的核外电子轨道表示式为___________ 。
(2)W、X、Y的第一电离能由小到大的顺序是___________ 。(用对应元素符号作答)
(3)X、Y的气态氢化物的稳定性由大到小的顺序是___________ 。(用对应化学式作答)
(4)基态Q原子核外有___________ 种能量不同的电子,R元素在周期表中处于___________ 区。
(5) 分子中
分子中 键与
键与 键的个数比为
键的个数比为___________ 。
 具有相同数目的未成对电子,
具有相同数目的未成对电子, 的价电子数是
的价电子数是 的二分之一,
的二分之一, 的核外电子充满三个电子层。请回答下列问题:
的核外电子充满三个电子层。请回答下列问题:(1)基态X原子的核外电子轨道表示式为
(2)W、X、Y的第一电离能由小到大的顺序是
(3)X、Y的气态氢化物的稳定性由大到小的顺序是
(4)基态Q原子核外有
(5)
 分子中
分子中 键与
键与 键的个数比为
键的个数比为
您最近一年使用:0次
名校
6 . 砷化镓 是第二代半导体材料的代表,主要用于制作高速、高频、大功率和抗辐射电子器件。一种制备砷化镓的方法为
是第二代半导体材料的代表,主要用于制作高速、高频、大功率和抗辐射电子器件。一种制备砷化镓的方法为 。
。
(1)基态As原子的核外电子排布式为___________ 。
(2)As、Ga、Se的电负性由大到小的顺序为___________ 。
(3) 中
中 键的数目为
键的数目为___________ 。
 是第二代半导体材料的代表,主要用于制作高速、高频、大功率和抗辐射电子器件。一种制备砷化镓的方法为
是第二代半导体材料的代表,主要用于制作高速、高频、大功率和抗辐射电子器件。一种制备砷化镓的方法为 。
。(1)基态As原子的核外电子排布式为
(2)As、Ga、Se的电负性由大到小的顺序为
(3)
 中
中 键的数目为
键的数目为
您最近一年使用:0次
7 . 如图是某无机化合物的二聚分子,该分子中A、B两种元素都只有3个能层,分子中所有原子的最外层都达到8个电子的稳定结构。下列说法不正确 的是
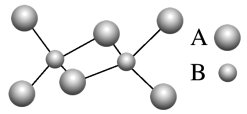
| A.元素B位于元素周期表第三周期ⅢA族 |
| B.该化合物是共价化合物,在熔融状态下能导电 |
| C.该化合物在固态时所形成的晶体是分子晶体 |
| D.该化合物中存在极性共价键,无非极性共价键 |
您最近一年使用:0次
名校
解题方法
8 .  具有还原性,一种催化氧化乙醇的反应为:
具有还原性,一种催化氧化乙醇的反应为: 。下列有关叙述正确的是
。下列有关叙述正确的是
 具有还原性,一种催化氧化乙醇的反应为:
具有还原性,一种催化氧化乙醇的反应为: 。下列有关叙述正确的是
。下列有关叙述正确的是A. 原子中的中子数为16 原子中的中子数为16 |
B. 的空间构型是直线型 的空间构型是直线型 |
C. 与 与 互溶是因为 互溶是因为 存在分子间氢键 存在分子间氢键 |
D. 分子中 分子中 键和 键和 键的数目之比为 键的数目之比为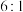 |
您最近一年使用:0次
解题方法
9 . 下列说法正确的是
| A.金属钠燃烧时火焰呈黄色与电子跃迁有关 |
B.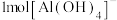 中含有 中含有 键 键 |
C.金属元素Ti位于周期表中 区 区 |
D. 中 中 原子采取 原子采取 杂化 杂化 |
您最近一年使用:0次
2024-04-23更新
|
118次组卷
|
2卷引用:2024届江苏省新高考基地学校高三下学期第五次大联考化学试题
名校
10 . 氯元素具有多种化合价,可形成 、
、 、
、 、
、 、
、 和
和 等多种粒子。下列关于含氯微粒的说法正确的是
等多种粒子。下列关于含氯微粒的说法正确的是
 、
、 、
、 、
、 、
、 和
和 等多种粒子。下列关于含氯微粒的说法正确的是
等多种粒子。下列关于含氯微粒的说法正确的是A. 中心原子轨道杂化类型为 中心原子轨道杂化类型为 | B. 为非极性分子 为非极性分子 |
C. 的键角为 的键角为 | D. 的空间构型为直线形 的空间构型为直线形 |
您最近一年使用:0次



