1 . 下列描述正确的是
| A.日常生活、生产中,钢铁的腐蚀多以析氢腐蚀为主 |
B.下列分子或离子中键角的大小顺序为:BeCl2> >NH3>NF3 >NH3>NF3 |
| C.在铁表面镀锡,既可隔绝环境防腐,当镀层破损还可以起“牺牲阴极的阳极保护” |
| D.邻羟基苯甲醛的沸点高于对羟基苯甲醛 |
您最近半年使用:0次
2 . 认真做作业一定会有收获,试试看,成功就在眼前。
(1)已知 晶体原子间均以单键结合成空间网状结构,下列关于
晶体原子间均以单键结合成空间网状结构,下列关于 晶体的说法正确的是___________。
晶体的说法正确的是___________。
(2)下列有关共价化合物的说法一定正确的是___________。
①具有较低的熔沸点②不是电解质③固态时是分子晶体④都是由分子构成的⑤液态时不导电
(3)分类方法在化学学科的发展中起到了重要的作用,下列说法合理的是___________。
(4)实验室制取氯化氢的化学方程式为___________ ;在标准状况下,甲乙两同学用两瓶纯度不同的氯化氢气体,进行喷泉实验,实验后,甲同学溶液充满整个烧瓶,乙同学溶液充满烧瓶的三分之二,则甲乙同学得到盐酸的物质的量浓度比为___________ (假设溶质不扩散,装置不漏气)
(5)向 溶液中逐滴加入稀硫酸,请完成下列问题:
溶液中逐滴加入稀硫酸,请完成下列问题:
①写出反应的离子方程式___________ 。
②下列三种情况下,离子方程式与①不相同的是___________ (填序号)。
A.向 溶液中,逐滴加入
溶液中,逐滴加入 溶液至溶液显中性
溶液至溶液显中性
B.向 溶液中,逐滴加入
溶液中,逐滴加入 溶液至
溶液至 恰好完全沉淀
恰好完全沉淀
C.向 溶液中,逐滴加入
溶液中,逐滴加入 溶液至过量
溶液至过量
(1)已知
 晶体原子间均以单键结合成空间网状结构,下列关于
晶体原子间均以单键结合成空间网状结构,下列关于 晶体的说法正确的是___________。
晶体的说法正确的是___________。A. 晶体是分子晶体 晶体是分子晶体 |
B. 晶体中,C—N键的键长比金刚石中的C—C键的键长长 晶体中,C—N键的键长比金刚石中的C—C键的键长长 |
C. 晶体熔点比金刚石更高 晶体熔点比金刚石更高 |
D. 晶体中每个C原子连接3个N原子,而每个N原子连接4个C原子 晶体中每个C原子连接3个N原子,而每个N原子连接4个C原子 |
①具有较低的熔沸点②不是电解质③固态时是分子晶体④都是由分子构成的⑤液态时不导电
| A.①③④ | B.②⑤ | C.①②③④⑤ | D.⑤ |
| A.根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸、三元酸等 |
| B.根据其水溶液是否能导电,将物质分为电解质和非电解质 |
| C.根据溶于水的酸碱性将氧化物分为酸性氧化物和碱性氧化物 |
| D.金属置换金属,非金属置换非金属,金属置换非金属,非金属置换金属四类置换反应均存在 |
(5)向
 溶液中逐滴加入稀硫酸,请完成下列问题:
溶液中逐滴加入稀硫酸,请完成下列问题:①写出反应的离子方程式
②下列三种情况下,离子方程式与①不相同的是
A.向
 溶液中,逐滴加入
溶液中,逐滴加入 溶液至溶液显中性
溶液至溶液显中性B.向
 溶液中,逐滴加入
溶液中,逐滴加入 溶液至
溶液至 恰好完全沉淀
恰好完全沉淀C.向
 溶液中,逐滴加入
溶液中,逐滴加入 溶液至过量
溶液至过量
您最近半年使用:0次
名校
解题方法
3 . 下列说法正确的是
A.基态 的核外电子排布式为 的核外电子排布式为 |
B. 中心原子为 中心原子为 杂化,空间构型为三角锥形 杂化,空间构型为三角锥形 |
C. 和 和 都是正四面体形微粒,其键角都为 都是正四面体形微粒,其键角都为 |
D.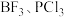 分子中所有原子的最外层都满足8电子稳定结构 分子中所有原子的最外层都满足8电子稳定结构 |
您最近半年使用:0次
2023-12-26更新
|
227次组卷
|
3卷引用:贵州省黔西南布依族苗族自治州2023-2024学年高一上学期1月期末化学试题
名校
4 . 下列关于物质结构的说法错误的是
A. 的空间结构为四面体形 的空间结构为四面体形 |
B.熔点: |
C.甲醛( 分子中 分子中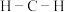 的键角小于光气 的键角小于光气 分子中 分子中 的键角 的键角 |
| D.基态氮原子有三种能量不同的电子 |
您最近半年使用:0次
2023-08-22更新
|
82次组卷
|
2卷引用:江苏省昆山中学2022-2023学年高一下学期5月月考化学试题
名校
解题方法
5 . 铜是人类最早使用的金属之一,铜的化合物丰富多彩。
(1)Cu在周期表中位于___________ 区,Cu2+价电子排布式为___________ 。
(2)邻氨基吡啶( )的铜配合物在有机合成中有重要作用。C、N、O的第一电离能由大到小的顺序为
)的铜配合物在有机合成中有重要作用。C、N、O的第一电离能由大到小的顺序为___________ ;1mol 中σ键的数目为
中σ键的数目为___________ 。邻氨基吡啶的铜配合物结构简式如下图所示,C原子轨道杂化类型为___________ 。
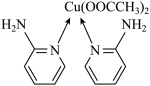
(3)向CuSO4溶液中加入过量氨水再加少许乙醇可以析出蓝色晶体[Cu(NH3)4]SO4∙H2O。
①NH3分子中H-N-H键角为107°,在[Cu(NH3)4]2+中H-N-H键角近似109.5°,键角变大的原因是___________ 。
②NF3与NH3均为三角锥形分子,NF3分子中的氮原子不易与Cu2+形成配离子,请从电负性角度分析其原因是___________ 。
(1)Cu在周期表中位于
(2)邻氨基吡啶(
 )的铜配合物在有机合成中有重要作用。C、N、O的第一电离能由大到小的顺序为
)的铜配合物在有机合成中有重要作用。C、N、O的第一电离能由大到小的顺序为 中σ键的数目为
中σ键的数目为
(3)向CuSO4溶液中加入过量氨水再加少许乙醇可以析出蓝色晶体[Cu(NH3)4]SO4∙H2O。
①NH3分子中H-N-H键角为107°,在[Cu(NH3)4]2+中H-N-H键角近似109.5°,键角变大的原因是
②NF3与NH3均为三角锥形分子,NF3分子中的氮原子不易与Cu2+形成配离子,请从电负性角度分析其原因是
您最近半年使用:0次
2023-07-05更新
|
151次组卷
|
2卷引用:江苏省泰州中学2022-2023学年高一下学期期末考试化学试题
名校
解题方法
6 . N、P、Sb原子的最外层电子数都是5,与卤素原子形成的化合物有广泛用途。 是液晶显示器生产过程中常用的化学清洗剂,
是液晶显示器生产过程中常用的化学清洗剂, 可用于面粉的漂白和杀菌,
可用于面粉的漂白和杀菌, 广泛应用于农药、杀虫剂的制造,
广泛应用于农药、杀虫剂的制造, 常用于有机反应催化剂。
常用于有机反应催化剂。
(1)几种化学键的键能如下表所示:
由两种单质化合形成1mol  ,焓变
,焓变
___________  。
。
(2)已知: 常温常压下为无色气体,熔点-129℃,沸点-207℃;
常温常压下为无色气体,熔点-129℃,沸点-207℃; 为黄色油状液体,熔点-40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:
为黄色油状液体,熔点-40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:
① 热稳定性高于
热稳定性高于 :
:___________ 。
② 熔、沸点高于
熔、沸点高于 :
:___________ 。
(3) 在水中溶解度不大,而
在水中溶解度不大,而 在水中溶解度较大,由此判断是
在水中溶解度较大,由此判断是
___________ 分子, 是
是___________ 分子。(填“极性”或“非极性”)
 是液晶显示器生产过程中常用的化学清洗剂,
是液晶显示器生产过程中常用的化学清洗剂, 可用于面粉的漂白和杀菌,
可用于面粉的漂白和杀菌, 广泛应用于农药、杀虫剂的制造,
广泛应用于农药、杀虫剂的制造, 常用于有机反应催化剂。
常用于有机反应催化剂。(1)几种化学键的键能如下表所示:
| 化学键 |  |  |  |
键能/ | 941.6 | 154.8 | 283.0 |
 ,焓变
,焓变
 。
。(2)已知:
 常温常压下为无色气体,熔点-129℃,沸点-207℃;
常温常压下为无色气体,熔点-129℃,沸点-207℃; 为黄色油状液体,熔点-40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:
为黄色油状液体,熔点-40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:①
 热稳定性高于
热稳定性高于 :
:②
 熔、沸点高于
熔、沸点高于 :
:(3)
 在水中溶解度不大,而
在水中溶解度不大,而 在水中溶解度较大,由此判断是
在水中溶解度较大,由此判断是
 是
是
您最近半年使用:0次
2023-06-20更新
|
204次组卷
|
3卷引用:上海交通大学附属中学2022-2023学年高一下学期期末考试(等级考)化学试题
上海交通大学附属中学2022-2023学年高一下学期期末考试(等级考)化学试题上海交通大学附属中学2022-2023学年高一下学期期末考试(等级考)化学试题(已下线)专题02 反应热的测量和计算-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)
名校
7 . 结合下表中数据,判断下列说法不正确 的是(氢键键长定义为 的长度)
的长度)
 的长度)
的长度)| 微粒间作用 | 键能/ | 键长/ |
晶体 中 中 | 452 | 162 |
晶体 中 中 | 222 | 235 |
 中 中 | 463 | 96 |
 中 中 | 18.8 | 276 |
 中 中 | 25.9 | 266 |
A.依据键长: ,推测原子半径: ,推测原子半径: |
B.依据键能: ,推测沸点: ,推测沸点: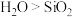 |
C.依据键长,推测水分子间 距离大于分子内 距离大于分子内 键长 键长 |
| D.依据氢键键能及沸点,推测等物质的量水或乙醇中,水中氢键数目多 |
您最近半年使用:0次
2023-05-07更新
|
590次组卷
|
3卷引用:北京市十一学校2022-2023学年高一下学期期末考试化学试题
名校
8 . 下列排序不正确的是
A.熔点: |
B.酸性: |
C.键角: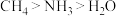 |
D.分子的极性: |
您最近半年使用:0次
2023-04-22更新
|
282次组卷
|
3卷引用:浙江省温州市2022-2023学年高一上学期期末教学质量统一检测(A卷)化学试题
9 . 下列说法不正确的是
| A.电负性的大小可以作为判断元素非金属性强弱的依据 |
| B.由玻璃制成规则的玻璃球体现了晶体的自范性 |
| C.键长和键角的数值可通过晶体的X射线衍射实验获得 |
D.冠醚是皇冠状的分子,可用于识别 、 、 、 、 等碱金属离子 等碱金属离子 |
您最近半年使用:0次
名校
解题方法
10 . 下列说法正确的是
| A.SCl2属于极性分子 |
| B.XeF4中心原子的价层电子对数为4 |
| C.H—O—H的键角:H3O+<H2O |
D.NO 的VSEPR模型、空间结构均为平面三角形 的VSEPR模型、空间结构均为平面三角形 |
您最近半年使用:0次
2023-02-11更新
|
370次组卷
|
2卷引用:山东省潍坊市临朐县第一中学2023-2024学年高一上学期12月月考化学试题



