解题方法
1 . “中国天眼”建造的关键材料之一是SiC,工业制备SiC的原理:Ⅰ.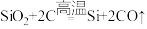 ,Ⅱ.
,Ⅱ. 。
。 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
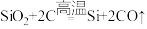 ,Ⅱ.
,Ⅱ. 。
。 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.6.0g 含Si-O键数目为0.4 含Si-O键数目为0.4 |
B.高温下,生成11.2LCO时转移的电子数为 |
C. 中氧化剂、还原剂质量比为1:1 中氧化剂、还原剂质量比为1:1 |
D.每生成1molSiC,总反应中转移的电子数为2 |
您最近一年使用:0次
7日内更新
|
51次组卷
|
3卷引用:2024届河南省百所名校仿真模拟大联考三模考试理综试题-高中化学
真题
名校
2 . 一种可在较高温下安全快充的铝-硫电池的工作原理如图,电解质为熔融氯铝酸盐(由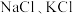 和
和 形成熔点为
形成熔点为 的共熔物),其中氯铝酸根
的共熔物),其中氯铝酸根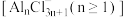 起到结合或释放
起到结合或释放 的作用。电池总反应:
的作用。电池总反应: 。下列说法
。下列说法错误 的是
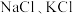 和
和 形成熔点为
形成熔点为 的共熔物),其中氯铝酸根
的共熔物),其中氯铝酸根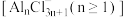 起到结合或释放
起到结合或释放 的作用。电池总反应:
的作用。电池总反应: 。下列说法
。下列说法
A. 含 含 个 个 键 键 |
B. 中同时连接2个 中同时连接2个 原子的 原子的 原子有 原子有 个 个 |
C.充电时,再生 单质至少转移 单质至少转移 电子 电子 |
D.放电时间越长,负极附近熔融盐中n值小的 浓度越高 浓度越高 |
您最近一年使用:0次
2023-11-16更新
|
3388次组卷
|
4卷引用:2024届河南省郑州市宇华实验学校高三一模化学试题
3 . Rh(铑)催化苯乙烯的不对称氢硒化反应历程如图所示。
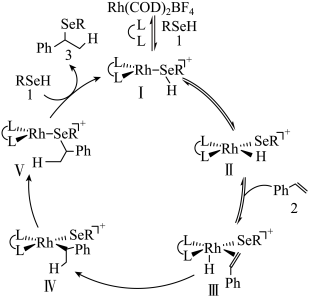
已知:与四个互不相同的原子或基团直接连接的碳原子叫手性碳原子,含手性碳原子的分子叫手性分子。Ph-代表苯基(C6H5-)。下列叙述错误的是

已知:与四个互不相同的原子或基团直接连接的碳原子叫手性碳原子,含手性碳原子的分子叫手性分子。Ph-代表苯基(C6H5-)。下列叙述错误的是
| A.该反应历程的总反应是最理想的绿色化学工艺 |
| B.Rh(COD)2BF4是总反应的催化剂 |
| C.上述循环中,Rh原子形成化学键数目保持不变 |
| D.有机物3是手性分子 |
您最近一年使用:0次
解题方法
4 . 过渡金属在生产、生活、科技等方面有着广泛的应用。例如仿生簇化合物Mn4XO4(X=Ca2+/Y3+/Gd3+)有望为实现利用太阳能和水获取清洁能源(氢能)开辟新途径,MnOx·Na2WO4·SiO2、钴(Co)的合金及其化合物材料等广泛应用于化工催化剂等领域。
请回答下列问题:
(1)基态钇(39Y)的价层电子排布式为_______ 。
(2)基态Co原子核外有_______ 种运动状态不同的电子,其3d能级上有_______ 对成对电子。
(3)[Co(NO2)6]3-中三种元素的第一电离能由大到小的顺序是_______ (填元素符号)。已知:[Co(CN)6]4-是强还原剂,与水反应能生成[Co(CN)6]3-。[Co(CN)6]4-中含有σ键与π键的数目之比为_______ ,[Co(CN)6]3-中C的杂化方式为_______ 。
(4)[Mn(NH3)2]2+中配体分子的立体构型是_______ 。[Mn(NH3)2]2+中键角∠HNH_______ (填“大于” 、“小于”或“等于”)NH3中键角∠HNH。
(5)MnF2、MnCl2晶体的熔点分别为856 °C、650 °C,二者熔点存在明显差异的主要原因是_______ 。
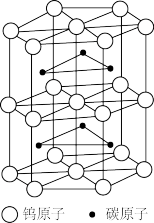
(6)碳化钨是一种由钨(W)和碳组成的晶体,其晶体结构如图所示,晶体的熔点为2870° C,硬度与金刚石相当。碳化钨的晶体类型是_______ ;已知:碳化钨晶体的密度为ρg·cm-3,NA为阿伏加德罗常数的值,六棱柱高为a cm,则底边长为_______ (用含ρ、a、N的表达式表示)nm。
请回答下列问题:
(1)基态钇(39Y)的价层电子排布式为
(2)基态Co原子核外有
(3)[Co(NO2)6]3-中三种元素的第一电离能由大到小的顺序是
(4)[Mn(NH3)2]2+中配体分子的立体构型是
(5)MnF2、MnCl2晶体的熔点分别为856 °C、650 °C,二者熔点存在明显差异的主要原因是
(6)碳化钨是一种由钨(W)和碳组成的晶体,其晶体结构如图所示,晶体的熔点为2870° C,硬度与金刚石相当。碳化钨的晶体类型是

您最近一年使用:0次
2022-05-27更新
|
410次组卷
|
5卷引用:河南省2022届高三下学期仿真模拟大联考理科综合化学试题
河南省2022届高三下学期仿真模拟大联考理科综合化学试题河北省秦皇岛市2022届高三三模化学试题(已下线)新疆博乐高级中学2022届高三第一次诊断性测试理科综合化学试卷广东省部分学校2022届高三下学期高考冲刺化学试题(已下线)专题17 物质结构与性质(综合题)-2022年高考真题模拟题分项汇编
名校
解题方法
5 . 12月 17日凌晨,嫦娥五号完成“ 挖土” 之旅返回地球。查阅资料,月球玄武岩是构成月球的岩石之一,主要由辉石(主要成分硅酸盐)和钛铁矿(主要成分 FeTiO3)等组成。回答下列问题:
(1)基态铁原子的价电子排布式为:______ 。
(2)与 Fe同周期,且最外层电子数相同的主族元素是______ (填元素符号)。
(3)基态 Ti原子核外电子占据的最高能层符号为______ ;其最外层电子的电子云轮廓图为______ 。
(4)1molFe3[Fe(CN)6]2中含有 σ键数为______ ,[Fe(CN)6]3-中配体为______ ,其中 C原子的杂化轨道类型为______ ,H、C、N、Si四种元素的电负性由大到小的顺序为______ 。
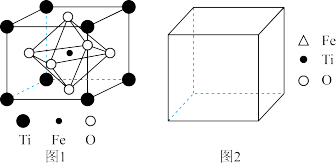
(5)FeTiO3的结构如图 1所示,其中由 O围成的______ (填“ 四面体空隙” 或“ 八面体空隙” )被 Fe占据。在图 2中画出 FeTiO3结构的另一种表示______ (要求:Fe处于晶胞的顶点),Ti的配位数为______ 。
(6)已知该晶胞的密度为 ρg/cm3,NA表示阿伏加德罗常数的值。计算晶胞参数 a=______ pm。(列出计算表达式)
(1)基态铁原子的价电子排布式为:
(2)与 Fe同周期,且最外层电子数相同的主族元素是
(3)基态 Ti原子核外电子占据的最高能层符号为
(4)1molFe3[Fe(CN)6]2中含有 σ键数为
(5)FeTiO3的结构如图 1所示,其中由 O围成的
(6)已知该晶胞的密度为 ρg/cm3,NA表示阿伏加德罗常数的值。计算晶胞参数 a=

您最近一年使用:0次
2021-03-14更新
|
854次组卷
|
3卷引用:河南省洛阳市2021届高三3月调研考试理综化学试题
河南省洛阳市2021届高三3月调研考试理综化学试题湖南省娄底市第五中学2021-2022学年高三下学期期中考试化学试题(已下线)01 物质结构与性质综合题型集训(1) (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
名校
6 . NA为阿伏伽德罗常数的值,下列说法正确的是
| A.2.4g镁在空气中充分燃烧,转移的电子数为0.2NA |
| B.0.1mol/L 的FeCl3溶液含Cl- 0.3NA |
| C.氢原子数为0.4NA的甲醇分子中含有的σ键数为0.4NA |
| D.0.1L 0.5mol/L CH3COOH溶液中含有的氢离子数为0.05NA |
您最近一年使用:0次
名校
解题方法
7 . 铜的相关化合物在生产生活中具有重要的作用。回答下列问题:
(1)铜元素在周期表中的位置是______________ ,基态铜原子中,核外电子占据最高能层的符号是_________________ ,占据该最高能层的电子数为__________________ 。
(2)在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、Cu5Zn8等。某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于__________ (填“晶体”或“非晶体”)。
(3)铜能与类卤素[(SCN)2]反应生成Cu(SCN)2,1mol(SCN)2分子中含有σ键的数目为______________ 。 (SCN)2对应的酸有硫氰酸(H-S-C N)、异硫氰酸(H-N=C=S)两种。理论上前者沸点低于后者,其原因是
N)、异硫氰酸(H-N=C=S)两种。理论上前者沸点低于后者,其原因是____________________________ 。
(4)铜晶体中铜原子的堆积方式为面心立方堆积,每个铜原子周围距离最近的铜原子个数为________ 。
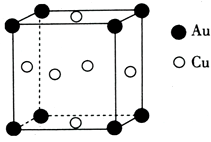
(5)铜与金形成的金属互化物的晶胞结构如图所示,其晶胞边长为a nm,该金属互化物的密度为____________ (用含a、NA的代数式表示)g·cm-3。
(1)铜元素在周期表中的位置是
(2)在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、Cu5Zn8等。某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于
(3)铜能与类卤素[(SCN)2]反应生成Cu(SCN)2,1mol(SCN)2分子中含有σ键的数目为
 N)、异硫氰酸(H-N=C=S)两种。理论上前者沸点低于后者,其原因是
N)、异硫氰酸(H-N=C=S)两种。理论上前者沸点低于后者,其原因是(4)铜晶体中铜原子的堆积方式为面心立方堆积,每个铜原子周围距离最近的铜原子个数为
(5)铜与金形成的金属互化物的晶胞结构如图所示,其晶胞边长为a nm,该金属互化物的密度为

您最近一年使用:0次
2018-05-01更新
|
280次组卷
|
3卷引用:【全国市级联考】河南省新乡市2018届高三第三次模拟测试理综化学试题
解题方法
8 . 溴化铜(II)甲基咪唑配合物是一种制备有机玻璃的催化剂,其合成方法如下:

(1)铜元素位于周期表中第_____ 族,写出基态Cu2+的电子排布式_______ 。
(2)与NH4+互为等电子体的阴离子为_______ 。
(3)SO42-中心原子的杂化方式为_________ 。
(4)Mlm中含σ键与π数目之比为__________ 。
(5)一种铜的溴化物晶胞结构如下图所示。
由图中P点和Q点的原子坐标参数,可确定R点的原子坐标参数为______ 。
(6)Cu晶体的堆积方式如图所示,设Cu原子半径为a,晶体中Cu原子的配位数为____ ,晶体的空间利用率为__________ 。(列式计算)

(1)铜元素位于周期表中第
(2)与NH4+互为等电子体的阴离子为
(3)SO42-中心原子的杂化方式为
(4)Mlm中含σ键与π数目之比为
(5)一种铜的溴化物晶胞结构如下图所示。

由图中P点和Q点的原子坐标参数,可确定R点的原子坐标参数为

(6)Cu晶体的堆积方式如图所示,设Cu原子半径为a,晶体中Cu原子的配位数为
您最近一年使用:0次
9 . NA代表阿伏加德罗常数。已知C2H4和C3H6的混合物的质量为m g,则该混合物
| A.所含碳原子总数为m NA/14 |
| B.所含碳氢键数目为3m NA/14 |
| C.所含共用电子对数目为(m/14+1)NA |
| D.完全燃烧时消耗的O2一定是33.6m/14 L |
您最近一年使用:0次



