名校
1 . I.以下物质中:①HF ②Cl2 ③H2O ④N2 ⑤C2H4
(1)既有极性键又有非极性键的是_______ 。
(2)只含有σ键的是_______ 。
(3)属于极性分子的是_______ 。
(4)属于非极性分子的是_______ 。
II.COCl2分子的结构式为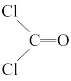
(5)COCl2分子内含有_______(填选项字母)。
III.超氧化钾的晶胞结构如图所示。

(6)则与K+等距离且最近的K+个数为_______ 。
(1)既有极性键又有非极性键的是
(2)只含有σ键的是
(3)属于极性分子的是
(4)属于非极性分子的是
II.COCl2分子的结构式为

(5)COCl2分子内含有_______(填选项字母)。
| A.4个σ键 | B.2个σ键、2个π键 |
| C.2个σ键、1个π键 | D.3个σ键、1个π键 |
III.超氧化钾的晶胞结构如图所示。

(6)则与K+等距离且最近的K+个数为
您最近一年使用:0次
名校
解题方法
2 . Ni元素在生产、生活中有着广泛的应用。 回答下列问题:
(1)基态Ni原子价层电子的排布式为____ 。
(2)科学家在研究金属矿物质组分的过程中,发现了Cu-Ni-Fe等多种金属互化物。确定某种金属互化物是晶体还是非晶体最可靠的科学方法是对固体进行_____ 。
(3)Ni能与类卤素(SCN)2反应生成Ni(SCN)2。Ni(SCN)2中,第一电离能最大的元素是____ ;(SCN)2分子中,硫原子的杂化方式是____ ,σ键和π键数目之比为_____ 。
(4)[Ni(NH3)6](NO3)2中,不存在的化学键为____ (填标号)。
a.离子键 b.金属键 c.配位键 d.氢键
(5)镍合金储氢的研究已取得很大进展。
①图甲是一种镍基合金储氢后的晶胞结构示意图。 该合金储氢后,含1molLa的合金可吸附H2的数目为_____ 。
②Mg2NiH4是一种贮氢的金属氢化物。在Mg2NiH4晶胞中,Ni原子占据如图乙的顶点和面心,Mg2+处于乙图八个小立方体的体心。Mg2+位于Ni原子形成的___ (填“八面体空隙”或“四面体空隙”)。 若晶体的密度为dg/cm3,Mg2NiH4的摩尔质量为Mg/mol,则Mg2+和Ni原子的最短距离为 ___ nm(用含d、M、NA的代数式表示)。

(1)基态Ni原子价层电子的排布式为
(2)科学家在研究金属矿物质组分的过程中,发现了Cu-Ni-Fe等多种金属互化物。确定某种金属互化物是晶体还是非晶体最可靠的科学方法是对固体进行
(3)Ni能与类卤素(SCN)2反应生成Ni(SCN)2。Ni(SCN)2中,第一电离能最大的元素是
(4)[Ni(NH3)6](NO3)2中,不存在的化学键为
a.离子键 b.金属键 c.配位键 d.氢键
(5)镍合金储氢的研究已取得很大进展。
①图甲是一种镍基合金储氢后的晶胞结构示意图。 该合金储氢后,含1molLa的合金可吸附H2的数目为
②Mg2NiH4是一种贮氢的金属氢化物。在Mg2NiH4晶胞中,Ni原子占据如图乙的顶点和面心,Mg2+处于乙图八个小立方体的体心。Mg2+位于Ni原子形成的

您最近一年使用:0次
2020-04-14更新
|
360次组卷
|
3卷引用:黑龙江省牡丹江市阳明区2022-2023学年高三上学期第四次阶段考试化学试题



