1 . 铜基催化剂(包括铜、氧化物、铜合金、单原子和复合材料)因其效率高、成本低和对生态友好而受到重视。
(1)基态铜原子的核外电子有______ 种不同的空间运动状态;第二周期元素中,第一电离能比 大的有
大的有______ 种。
(2)研究发现,以掺有镁的铜纳米合金电还原催化 制
制 有较高的选择性,与氮气相比,
有较高的选择性,与氮气相比, 的键能较低
的键能较低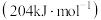 使其成为
使其成为 合成的理想来源。
合成的理想来源。
① 的中心原子的杂化类型为
的中心原子的杂化类型为______ 。
②将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。
______ (填“属于”或“不属于”)顺磁性物质, 中
中 键角
键角______ (填“>”或“<”) 中
中 键角。
键角。
(3)铜基单原子催化剂能将 转化为
转化为 。
。
① 分子中含有
分子中含有______ 个 键。
键。
②沸点:
______  (填“>”或“<”)。
(填“>”或“<”)。
(4)一种镁铜合金的晶胞结构如图所示,晶胞参数为 ,该晶胞可看成由8个小立方体构成,其中4个小立方体的体心填入
,该晶胞可看成由8个小立方体构成,其中4个小立方体的体心填入 ,另外4个小立方体的体心填入以四面体方式排列的
,另外4个小立方体的体心填入以四面体方式排列的 ,其余
,其余 占据晶胞的顶点和面心。
占据晶胞的顶点和面心。 与
与 的最短距离为
的最短距离为______  (用含
(用含 的代数式表示);若阿伏加德罗常数的值为
的代数式表示);若阿伏加德罗常数的值为 ,该合金晶体的密度为
,该合金晶体的密度为______  (列出含
(列出含 ,
, 的计算式)。
的计算式)。
(1)基态铜原子的核外电子有
 大的有
大的有(2)研究发现,以掺有镁的铜纳米合金电还原催化
 制
制 有较高的选择性,与氮气相比,
有较高的选择性,与氮气相比, 的键能较低
的键能较低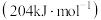 使其成为
使其成为 合成的理想来源。
合成的理想来源。①
 的中心原子的杂化类型为
的中心原子的杂化类型为②将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。

 中
中 键角
键角 中
中 键角。
键角。(3)铜基单原子催化剂能将
 转化为
转化为 。
。①
 分子中含有
分子中含有 键。
键。②沸点:

 (填“>”或“<”)。
(填“>”或“<”)。(4)一种镁铜合金的晶胞结构如图所示,晶胞参数为
 ,该晶胞可看成由8个小立方体构成,其中4个小立方体的体心填入
,该晶胞可看成由8个小立方体构成,其中4个小立方体的体心填入 ,另外4个小立方体的体心填入以四面体方式排列的
,另外4个小立方体的体心填入以四面体方式排列的 ,其余
,其余 占据晶胞的顶点和面心。
占据晶胞的顶点和面心。
 与
与 的最短距离为
的最短距离为 (用含
(用含 的代数式表示);若阿伏加德罗常数的值为
的代数式表示);若阿伏加德罗常数的值为 ,该合金晶体的密度为
,该合金晶体的密度为 (列出含
(列出含 ,
, 的计算式)。
的计算式)。
您最近一年使用:0次
名校
解题方法
2 . 已知:含 的酸性溶液
的酸性溶液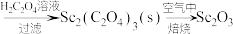 。下列说法正确的是
。下列说法正确的是
 的酸性溶液
的酸性溶液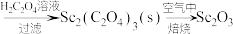 。下列说法正确的是
。下列说法正确的是A.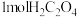 (乙二酸)含有 (乙二酸)含有 键 键 |
B.沸点: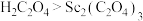 |
C.生成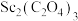 的离子方程式为 的离子方程式为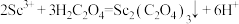 |
D.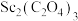 在足量空气中焙烧,消耗 在足量空气中焙烧,消耗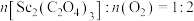 |
您最近一年使用:0次
名校
3 .  是阿伏加德罗常数的值,下列说法正确的是
是阿伏加德罗常数的值,下列说法正确的是
 是阿伏加德罗常数的值,下列说法正确的是
是阿伏加德罗常数的值,下列说法正确的是A.将0.1molNaF溶于稀氢氟酸溶液中使溶液呈中性,溶液中F-数目小于 |
B.6g石墨烯中含有六元环的个数为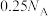 |
C. 中 中 键的个数为 键的个数为 |
D.11.2L乙烷和丙烯的混合气体中所含碳氢键数为 |
您最近一年使用:0次
7日内更新
|
290次组卷
|
2卷引用:2024届辽宁省实验中学高三下学期考前模拟训练(五模)化学试卷
解题方法
4 . “中国天眼”建造的关键材料之一是SiC,工业制备SiC的原理:Ⅰ.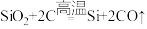 ,Ⅱ.
,Ⅱ. 。
。 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
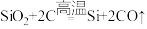 ,Ⅱ.
,Ⅱ. 。
。 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.6.0g 含Si-O键数目为0.4 含Si-O键数目为0.4 |
B.高温下,生成11.2LCO时转移的电子数为 |
C. 中氧化剂、还原剂质量比为1:1 中氧化剂、还原剂质量比为1:1 |
D.每生成1molSiC,总反应中转移的电子数为2 |
您最近一年使用:0次
7日内更新
|
51次组卷
|
3卷引用:2024届河南省百所名校仿真模拟大联考三模考试理综试题-高中化学
名校
5 . 一定条件下, ,设
,设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 ,设
,设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.标准状况下,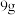 水中的中子数目为 水中的中子数目为 |
B.常温常压下, 正丙醇中 正丙醇中 杂化的原子数目为 杂化的原子数目为 |
C.标准状况下, 丙烯中 丙烯中 键的数目为 键的数目为 |
D. 的正丙醇溶液中氧原子的数目为 的正丙醇溶液中氧原子的数目为 |
您最近一年使用:0次
名校
6 . γ-丁内酯(BL)广泛应用于医药、染料等领域。
Ⅰ.γ-羟基丁酸发生酯化反应合成BL。_______ 。
(2)已知:②
 。平衡常数K与ΔG关系为
。平衡常数K与ΔG关系为 (R为气体常数,T为温度),ΔH1和ΔH2近似相等,但是在相同条件下,反应①的限度显著大于反应②,其原因是
(R为气体常数,T为温度),ΔH1和ΔH2近似相等,但是在相同条件下,反应①的限度显著大于反应②,其原因是_______ 。
(3)298K下,水溶液中物质浓度随时间变化如图所示。_______ ,为了提高平衡转化率,除改变温度外,还可以采取的措施有_______ 。
②298K时,该反应的平衡常数K为_______ 。
Ⅱ.1,4-丁二醇(BD)脱氢法合成BL。有关反应如下: 。
。
(4)在493K,3.0×103kPa的高压H2氛围下,分别以0.01mol BD或BL为初始原料,在密闭容器中进行反应。达到平衡时,以BD为原料,体系从环境吸收a kJ热量;以BL为原料,体系向环境放出b kJ热量。忽略ⅱ、ⅲ反应的热效应。在此条件下,ⅰ反应的ΔH(493K,3.0×103kPa)=_______ kJ·mol-1。
(5)在标准大气压下,选择CuO/ZnO/Al2O3作催化剂,氢醇比 为5,分别探究温度和流速(BD和H2通过催化剂表面的速率)对三种产物选择性的影响,所得关系曲线如图2和图3所示。
为5,分别探究温度和流速(BD和H2通过催化剂表面的速率)对三种产物选择性的影响,所得关系曲线如图2和图3所示。
(6)在体积固定的刚性容器中充入5.0×10-3mol BL,在493K、3.0×103kPa条件下,在高压H2氛围中反应生成BD(伴随反应ⅱ和ⅲ)。已知:物质的量分数(xa)表示体系中物质a的物质的量与除H2外所有物质的物质的量总和之比。该条件下达到平衡时, ,
,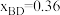 ,则
,则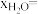
_______ 。
Ⅰ.γ-羟基丁酸发生酯化反应合成BL。
①
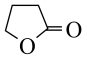

 ΔH1。
ΔH1。
(2)已知:②

 。平衡常数K与ΔG关系为
。平衡常数K与ΔG关系为 (R为气体常数,T为温度),ΔH1和ΔH2近似相等,但是在相同条件下,反应①的限度显著大于反应②,其原因是
(R为气体常数,T为温度),ΔH1和ΔH2近似相等,但是在相同条件下,反应①的限度显著大于反应②,其原因是(3)298K下,水溶液中物质浓度随时间变化如图所示。

②298K时,该反应的平衡常数K为
Ⅱ.1,4-丁二醇(BD)脱氢法合成BL。有关反应如下:
ⅰ.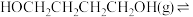

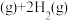 ;
;
ⅱ.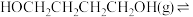
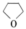
 ;
;
 。
。(4)在493K,3.0×103kPa的高压H2氛围下,分别以0.01mol BD或BL为初始原料,在密闭容器中进行反应。达到平衡时,以BD为原料,体系从环境吸收a kJ热量;以BL为原料,体系向环境放出b kJ热量。忽略ⅱ、ⅲ反应的热效应。在此条件下,ⅰ反应的ΔH(493K,3.0×103kPa)=
(5)在标准大气压下,选择CuO/ZnO/Al2O3作催化剂,氢醇比
 为5,分别探究温度和流速(BD和H2通过催化剂表面的速率)对三种产物选择性的影响,所得关系曲线如图2和图3所示。
为5,分别探究温度和流速(BD和H2通过催化剂表面的速率)对三种产物选择性的影响,所得关系曲线如图2和图3所示。
| A.题给条件下,制备BL反应的最优温度为320℃,最优流速为1.6 L·min-1 |
| B.流速较小时,发生副反应导致BL选择性不高 |
| C.280℃后,温度升高,BL的选择性降低的原因可能是催化剂活性降低 |
| D.实际工业生产时流速选择2.0 L·min-1的原因是所得BL产品杂质含量少 |
(6)在体积固定的刚性容器中充入5.0×10-3mol BL,在493K、3.0×103kPa条件下,在高压H2氛围中反应生成BD(伴随反应ⅱ和ⅲ)。已知:物质的量分数(xa)表示体系中物质a的物质的量与除H2外所有物质的物质的量总和之比。该条件下达到平衡时,
 ,
,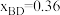 ,则
,则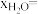
您最近一年使用:0次
7 . 设 为阿伏加德罗常数的值。下列叙述错误的是
为阿伏加德罗常数的值。下列叙述错误的是
 为阿伏加德罗常数的值。下列叙述错误的是
为阿伏加德罗常数的值。下列叙述错误的是A.1mol锗(Ge)含共价键数目为2 |
B.60g异丙醇含 杂化的原子数目为3 杂化的原子数目为3 |
C.氢氧燃料电池中,负极上1mol气体参与反应时转移电子数目为2 |
D.1mol  含 含 键的数目为12 键的数目为12 |
您最近一年使用:0次
8 . 设 为阿伏加德罗常数的值。砷化镓
为阿伏加德罗常数的值。砷化镓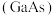 是半导体材料,气相生长法制备
是半导体材料,气相生长法制备 的原理如下:
的原理如下:
①
②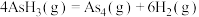
③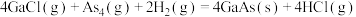
下列叙述正确的是
 为阿伏加德罗常数的值。砷化镓
为阿伏加德罗常数的值。砷化镓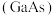 是半导体材料,气相生长法制备
是半导体材料,气相生长法制备 的原理如下:
的原理如下:①

②
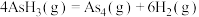
③
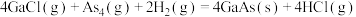
下列叙述正确的是
A.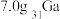 的最外层电子数为 的最外层电子数为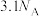 |
B.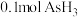 中含共价键数目为 中含共价键数目为 |
C.标准状况下,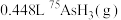 含中子的数目为 含中子的数目为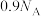 |
D.反应③中每生成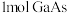 转移的电子数目为 转移的电子数目为 |
您最近一年使用:0次
名校
9 .  代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是A.11.2L  含π键数目为 含π键数目为 |
B.NaCl和 的混合物中含1mol 的混合物中含1mol  ,则混合物中质子数为28 ,则混合物中质子数为28 |
C.电解熔融 ,阴极增重6.4g,外电路中通过电子的数目为0.1 ,阴极增重6.4g,外电路中通过电子的数目为0.1 |
D.1.7g  完全溶于1L 完全溶于1L  所得的溶液中, 所得的溶液中, 微粒的数目为0.1 微粒的数目为0.1 |
您最近一年使用:0次
7日内更新
|
246次组卷
|
3卷引用:广东省揭阳市2024届高三下学期二模考试化学试题
10 . 已知反应:2HNO2+CO(NH2)2=2N2↑+CO2↑+3H2O,若NA为阿伏加德罗常数的值,下列叙述错误的是
| A.消耗1molHNO2时,生成氧化产物的分子数为NA |
| B.消耗60gCO(NH2)2时,生成产物中σ键数目为10NA |
| C.生成1molH2O时,生成产物中非极性分子数目为NA |
| D.生成11.2L(标准状况下)CO2时,转移电子数目为3NA |
您最近一年使用:0次



