名校
1 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.3.2g  、 、 混合气体所含质子的数目为 混合气体所含质子的数目为 |
B.25℃,101kPa下,56L  所含中子的数目为 所含中子的数目为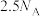 |
C.1L pH=1的 溶液中所含 溶液中所含 数目为 数目为 |
D.0.1mol环己烷(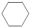 )中所含σ键数目为 )中所含σ键数目为 |
您最近一年使用:0次
2 .  表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是
 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是A.1L0.1mol/L的 溶液中含有 溶液中含有 的数目为 的数目为 |
B.常温常压下,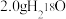 和 和 的混合物中含有的电子数一定为 的混合物中含有的电子数一定为 |
C.常温常压下,31g白磷燃烧生成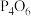 时,断裂P-P键的数目为 时,断裂P-P键的数目为 |
D.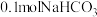 晶体中含有阴、阳离子总数为 晶体中含有阴、阳离子总数为 |
您最近一年使用:0次
3 .  表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是
 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是A.常温下, 的 的 溶液中水电离出 溶液中水电离出 数目为 数目为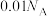 |
B.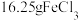 水解形成的 水解形成的 胶体粒子数为 胶体粒子数为 |
C.常温下,8.8g环氧乙烷(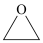 )中含有的共价键数目为 )中含有的共价键数目为 |
D.电解饱和食盐水时,若阴阳两极产生气体的总质量为7.3g,则转移电子数为 |
您最近一年使用:0次
解题方法
4 . 三草酸合铁酸钾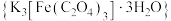 是制备铁触媒上的主要原料。在光照下分解:
是制备铁触媒上的主要原料。在光照下分解: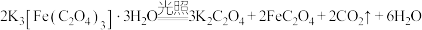 。回答下列问题:
。回答下列问题:
(1)基态 原子的电子排布式为
原子的电子排布式为___________ ,基态 与
与 中未成对电子的数目之比为
中未成对电子的数目之比为___________ 。
(2)三草酸合铁酸钾所含元素中,第一电离能最大的是___________ (填元素符号,下同),电负性最大的是___________ 。
(3)1个 与1个
与1个 分子中
分子中 键数目之比为
键数目之比为___________ , 分子的立体构型为
分子的立体构型为___________ 。
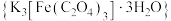 是制备铁触媒上的主要原料。在光照下分解:
是制备铁触媒上的主要原料。在光照下分解: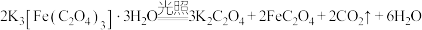 。回答下列问题:
。回答下列问题:(1)基态
 原子的电子排布式为
原子的电子排布式为 与
与 中未成对电子的数目之比为
中未成对电子的数目之比为(2)三草酸合铁酸钾所含元素中,第一电离能最大的是
(3)1个
 与1个
与1个 分子中
分子中 键数目之比为
键数目之比为 分子的立体构型为
分子的立体构型为
您最近一年使用:0次
名校
5 . 下列模型分别表示C2H2、S8、SF6的结构,下列说法错误的是



| A.1 mol C2H2分子中有3 mol σ键和2 mol π键 |
| B.SF6是由极性键构成的非极性分子 |
| C.32 g S8分子中含有0.125 mol σ键 |
| D.1 mol S8中含有8 mol S—S |
您最近一年使用:0次
6 . 用 表示阿伏加德罗常数的值,下列叙述中正确的是
表示阿伏加德罗常数的值,下列叙述中正确的是
 表示阿伏加德罗常数的值,下列叙述中正确的是
表示阿伏加德罗常数的值,下列叙述中正确的是A.标准状况下,11.2 L 中含原子数目为 中含原子数目为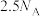 |
B.常温常压下,1mol分子式为 的有机物中,含有 的有机物中,含有 键的数目为 键的数目为 |
C.14g由乙烯和环丙烷( )组成的混合气体中,含有的原子总数为 )组成的混合气体中,含有的原子总数为 |
D.100 g 46%乙醇溶液中含有的 键的数目为 键的数目为 |
您最近一年使用:0次
名校
7 . 在CoOx/MnO2催化下醇的氧化氰化反应如图所示。下列叙述正确的是

| A.物质的沸点:I>Ⅱ | B.I和Ⅱ分子中碳原子的杂化方式相同 |
C.I和Ⅱ分子中 键数目相同 键数目相同 | D.Ⅱ含有的元素中N的电负性最大 |
您最近一年使用:0次
解题方法
8 . 乙炔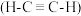 是有机合成工业的一种重要原料。下列两种方法可生产乙炔。
是有机合成工业的一种重要原料。下列两种方法可生产乙炔。
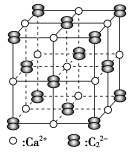
碳化钙晶胞示意图: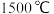 电弧中经极短时间加热分解产生乙炔。
电弧中经极短时间加热分解产生乙炔。
①反应的化学方程式为_______ 。
②上述反应中碳原子轨道杂化类型的变化为_______ 。
③乙炔分子中 键和
键和 键数目之比为
键数目之比为_______ 。
(2)工业上曾用电石(主要成分为碳化钙)与水反应生成乙炔。
① 基态核外电子排布式为
基态核外电子排布式为_______ 。
②碳化钙晶体中哑铃形 的存在,使晶胞沿一个方向拉长。碳化钙晶体中1个
的存在,使晶胞沿一个方向拉长。碳化钙晶体中1个 周围距离
周围距离最近 的 围成的几何图形为
围成的几何图形为_______ (填正方形、正四面体或正八面体)。
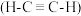 是有机合成工业的一种重要原料。下列两种方法可生产乙炔。
是有机合成工业的一种重要原料。下列两种方法可生产乙炔。碳化钙晶胞示意图:
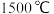 电弧中经极短时间加热分解产生乙炔。
电弧中经极短时间加热分解产生乙炔。①反应的化学方程式为
②上述反应中碳原子轨道杂化类型的变化为
③乙炔分子中
 键和
键和 键数目之比为
键数目之比为(2)工业上曾用电石(主要成分为碳化钙)与水反应生成乙炔。
①
 基态核外电子排布式为
基态核外电子排布式为②碳化钙晶体中哑铃形
 的存在,使晶胞沿一个方向拉长。碳化钙晶体中1个
的存在,使晶胞沿一个方向拉长。碳化钙晶体中1个 周围距离
周围距离 围成的几何图形为
围成的几何图形为
您最近一年使用:0次
解题方法
9 . 设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.常温常压下,乙烯和丙烯的混合气体共14g,含原子数为3 |
B.1mol苯分子含碳碳双键数目为3 |
C.常温常压下,28g乙烯含σ键数目为6 |
D.1mol羟基所含电子数为10 |
您最近一年使用:0次
10 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.7.8gNa2O2与二氧化碳充分反应,转移电子的数目为0.2NA |
| B.标准状况下,11.2LSO3含有1.5NA个氧原子 |
| C.28gC2H4分子含有的σ键数目为4NA |
| D.1.8g18O中含有的中子数为NA |
您最近一年使用:0次
2024-03-11更新
|
83次组卷
|
2卷引用:湖北省仙桃市田家炳实验高级中学2023-2024学年高三上学期11月月考化学试题



